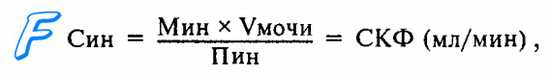что влияет на скорость клубочковой фильтрации
Скорость клубочковой фильтрации, как способ оценки состояния почек
Врач лабораторной диагностики
(заведующий клинико-
диагностической лабораторией)
Лавицкая Т.В.
Почка состоит из миллиона единиц – нефронов, которые представляют собой клубочек сосудов и канальцы для прохождения жидкости. Нефроны с мочой удаляют продукты обмена из крови. За сутки через них проходит до 120 литров жидкости. Очищенная вода всасывается в кровь для осуществления процессов обмена. Вредные вещества выводятся из организма в виде концентрированной мочи. Из капилляра под давлением, образующимся работой сердца, в капсулу клубочка проталкивается жидкая плазма. Белок и другие крупные молекулы остаются в капиллярах. Если почки больны, нефроны погибают, а новые не образуются, почки плохо выполняют свою очистительную миссию. От повышенной нагрузки здоровые нефроны выходят из строя в ускоренном темпе.
Методы, позволяющие оценить работу почек
Фильтрация жидкости проходит через гломерулярный фильтр. Он представляет собой капилляры, базальную мембрану и капсулу.
Через капиллярный индотелий, точнее, через его отверстия поступает вода с растворенными веществами. Базальная мембрана не дает проникнуть белкам в почечную жидкость. Фильтрация быстро изнашивает мембрану. Ее клетки постоянно обновляются.
Очищенная через базальную мембрану жидкость поступает в полость капсулы. Процесс отсорбирования осуществляется за счет отрицательно заряда фильтра и давления. Под давлением происходит продвижение жидкости с содержащимися в ней веществами из крови в капсулу клубочка. СКФ – основной показатель работы почек, а значит, и их состояния. Она показывает объем образования первичной мочи за единицу времени. Скорость клубочковой фильтрации зависит от: количества плазмы, проникающей в почки. Нормой этого показателя является 600 мл в минуту у здорового человека средней комплекции; фильтрационного давления; площади фильтрующей поверхности. В нормальном состоянии СКФ находится на постоянном уровне.
Расчет скорости клубочковой фильтрации возможен по нескольким методикам и формулам. Процесс определения сводится к сравнению содержания контрольного вещества в плазме и моче больного.
Нормальные показатели СКФ показывает работоспособность нефронов и общее состояние почек.
Скорость клубочковой фильтрации почек в норме составляет 125 мл/мин у мужчин, а у женщин — 11о мл/мин.
Для клинических исследований измерения производят по клиренсу креатинина. Образование и удаление его постоянны и находятся в прямой зависимости от объема мышечной массы тела.У мужчин, ведущих активную жизнь, выработка креатинина выше, чем у детей и женщин.
В основном это вещество выводится методом клубочковой фильтрации. Но 5-10% его проходит через проксимальные канальцы. Поэтому получается некоторая погрешность показателей. При замедлении фильтрации содержание вещества резко увеличивается. По сравнению с СКФ он составляет до 70%. Это признаки почечной недостаточности.
Картину показаний может исказить содержание в крови лекарственных препаратов. И все же клиренс креатинина – более доступный и общепринятый анализ.
Для исследования берется вся суточная моча за исключением первой утренней порции. Содержание вещества в моче у мужчин должно составить 18-21 мг/кг, у женщин – на 3 единицы меньше. Меньшие показания говорят о болезни почек или неправильном сборе мочи.
Простейший способ оценки работы почек – определение уровня креатинина в сыворотке. Насколько повышен этот показатель, настолько снижена СКФ. То есть, чем выше скорость фильтрации, тем меньше содержание креатинина в моче. Анализ клубочковой фильтрации делается при подозрении на почечную недостаточность.
Какие болезни позволяет выявить.
СКФ может помочь диагностировать различные формы заболевания почек. При уменьшении скорость фильтрации это может быть сигналом к проявлению хронической формы недостаточности. При этом растет концентрация мочевины и креатинина в моче. Почки не успевают очищать кровь от вредных веществ. При пиелонефрите поражаются канальцы нефронов. Уменьшение скорости клубочковой фильтрации наступает позднее. Определить данное заболевание поможет проба по Зимницкому.
Величина фильтрации повышается при сахарном диабете, гипертензии, красной волчанке и некоторых других заболеваниях. Снижение СКФ происходит при патологических изменениях, при массовой потере нефронов. Причиной могут стать снижение артериального давления, шок, сердечная недостаточность. Внутричерепное давление поднимается при плохом оттоке мочи. Из-за усиления венозного давления в почке процесс фильтрации замедляется.
При болях в спине, нарушении мочеиспускания следует обратиться к врачам специалистам — урологу и нефрологу.
Почки – важнейший очистительный орган нашего организма. При нарушении их функционирования происходит сбой в работе многих органов, кровь несет вредные вещества, происходит частичное отравление всех тканей. Поэтому при малейшем беспокойстве в области почек, следует сдать анализы, проконсультироваться с врачом, пройти необходимые обследования и начать своевременное лечение.
Как оценить работу почек? Что такое СКФ?
Как оценить работу почек? Что такое СКФ?
Здоровая почка состоит из 1-1,2 миллиона единиц почечной ткани — нефронов, функционально связанных с кровеносными сосудами. Каждый нефрон — длиной около 3 см, в свою очередь, состоит из сосудистого клубочка и системы канальцев, длина которых в нефроне 50 — 55 мм, а всех нефронов — около 100 км. В процессе образования мочи нефроны удаляют из крови продукты обмена, регулируют ее состав. За сутки профильтровывается 100–120 литров так называемой первичной мочи. Большая часть жидкости всасывается обратно в кровь – за исключением «вредных» и ненужных организму веществ. В мочевой пузырь попадает лишь 1–2 литра вторичной концентрированной мочи.
Из-за различных заболеваний нефроны один за другим выбывают из строя, по большей части безвозвратно. Функции погибших «собратьев» берут на себя другие нефроны, их же поначалу так много. Однако со временем нагрузка на работоспособные нефроны становится все больше – и они, перетрудившись, погибают все быстрее.
Как оценить работу почек? Если бы можно было точно подсчитывать количество здоровых нефронов, вероятно, это был бы один из наиболее точных показателей. Однако существуют и другие методы. Можно, например, собрать всю мочу больного за сутки и одновременно проанализировать его кровь – рассчитать клиренс креатинина, то есть скорость очищения крови от этого вещества.
Креатинин — конечный продукт обмена белков. Норма содержания креатинина в крови — 50-100 мкмоль/л у женщин и 60-115 мкмоль/л у мужчин, у детей эти показатели ниже в 2-3 раза. Есть и другие показатели нормы (не выше 88 мкмоль/л), такие расхождения частично зависят от используемых в лаборатории реактивов и от развития мышечной массы пациента. При хорошо развитой мускулатуре креатинин может достигать 133 мкмоль/л, при малой мышечной массе — 44 мкмоль/л. Креатинин образуется в мышцах, поэтому его некоторое повышение возможно при тяжелой мышечной работе и обширных травмах мышц. Почками выводится весь креатинин, за сутки примерно 1-2 г.
Впрочем, еще чаще для оценки степени хронической почечной недостаточности используется такой показатель, как СКФ — скорость клубочковой фильтрации (мл/мин).
В НОРМЕ СКФ составляет от 80 до 120 мл/мин, ниже у лиц старшего возраста. СКФ ниже 60 мл/мин считают началом хронической почечной недостаточности.
Приведем несколько формул, позволяющих оценить функцию почек. Они достаточно известны среди специалистов, я привожу их из книги, написанной специалистами отделения диализа С.-Петербургской городской Мариинской больницы (Земченков А.Ю., Герасимчук Р.П., Костылева Т.Г., Виноградова Л.Ю., Земченкова И.Г,. «Жизнь с хронической болезнью почек», 2011).
Это, например, формула расчета клиренса креатинина (формула Кокрофта-Голта, по фамилиям авторов формулы Cockcroft и Gault):
Ccr = (140 – возраст, годы) х вес кг/ (креатинин в ммоль/л) х 814,
Для женщин полученное значение умножается на 0,85
Между тем, справедливости ради надо сказать, что европейские медики не рекомендуют использовать эту формулу для оценки СКФ. Для более точного определения остаточной функции почек нефрологи используют так называемую формулу MDRD:
СКФ = 11,33 х Crк –1,154 х (возраст)–0,203 х 0,742 (для женщин),
где Crк – креатинин сыворотки крови (в ммоль/л). Если в результатах анализа креатинин дан в микромолях (мкмоль/л), эту величину следует разделить на 1000.
У формулы MDRD есть существенный недостаток: она плохо работает при высоких значениях СКФ. Поэтому в 2009 году нефрологи вывели новую формулу для оценки СКФ, формулу CKD-EPI. Результаты оценки СКФ по новой формуле совпадают с результатами MDRD при низких значениях, но дают более точную оценку при высоких значениях СКФ. Иногда бывает так, что человек потерял значительное количество функции почек, а креатинин у него все еще в норме. Формула эта слишком сложна, чтобы приводить ее здесь, но о том, что она существует, стоит знать.
А теперь о стадиях хронической болезни почек:
1 (СКФ больше 90). Нормальная или повышенная СКФ при наличии заболевания, поражающего почки. Требуется наблюдение у нефролога:диагностика и лечение основного заболевания, снижение риска развития сердечнососудистых осложнений
2 СКФ=89-60). Повреждение почек с умеренным снижением СКФ. Требуется оценка скорости прогрессирования ХБП, диагностика и лечение.
3 (СКФ=59-30). Средняя степень снижения СКФ. Необходимы профилактика, выявление и лечение осложнений
4 (СКФ=29-15). Выраженная степень снижения СКФ. Пора готовиться к заместительной терапии (необходим выбор метода).
5 (СКФ меньше 15). Почечная недостаточность. Начало заместительной почечной терапии.
Оценка скорости клубочковой фильтрации по уровню креатинина в крови (сокращенная формула MDRD):
Что влияет на скорость клубочковой фильтрации
Основной количественной характеристикой процесса фильтрации является скорость клубочковой фильтрации (СКФ). СКФ —это объем ультрафильтрата или первичной мочи, образующийся в почках за единицу времени. Эта величина зависит от нескольких факторов: 1) от объема крови, точнее плазмы, проходящей через корковое вещество почек в единицу времени, т. е. почечного плазмотока, составляющего в среднем у здорового человека массой 70 кг около 600 мл/мин; 2) фильтрационного давления, обеспечивающего сам процесс фильтрации; 3) фильтрационной поверхности, которая равна примерно 2—3 % от общей поверхности капилляров клубочка (1,6 м2) и может изменяться при сокращении подоцитов и мезан-гиальных клеток; 4) массы действующих нефронов, т. е. числа клубочков, осуществляющих процесс фильтрации в определенный промежуток времени.
В физиологических условиях СКФ поддерживается на довольно постоянном уровне (несмотря на изменения системного артериального давления) за счет механизмов ауторегуляции.
К их числу относятся:
1) миогенная ауторегуляция тонуса приносящих артериол по принципу феномена Остроумова— Бейлиса;
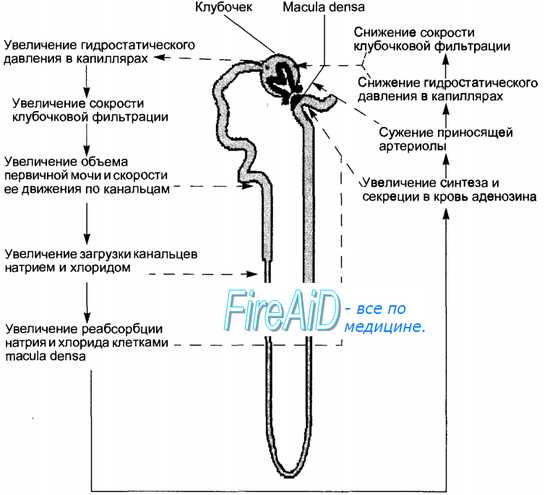
2) канальцево-клубочковая обратная связь, приводящая к изменению соотношения тонуса приносящих и выносящих артериол клубочка. Вовлечение в регуляцию механизма обратной связи обусловлено изменением доставки с фильтратом в область плотного пятна (macula densa) ионов натрия и хлора, что ведет к изменению продукции в ЮГА гуморальных регуляторов: аденозина (суживающий афферентные артериолы фактор), NO (дилатирующий артериолы фактор), ренина и ангиотензина-П, кининов и простагландинов (рис. 14.6);
3) изменения числа функционирующих нефронов. Первые два механизма поддерживают постоянство кровотока в клубочках и фильтрационное давление, гуморальные регуляторы могут менять площадь фильтрационной поверхности и функции подоцитов, третий механизм определяет конечный эффект ауторегуляции СКФ в органе, что в итоге обеспечивает постоянство объема образуемой первичной мочи.
СКФ определяют в результате сопоставления концентрации определенного вещества в плазме крови и моче. При этом используемое вещество должно выделяться вместе с водой только путем фильтрации и не всасываться в нефроне обратно в кровь. Таким условиям больше всего соответствует полисахарид фруктозы инулин. Исходя из концентрации инулина в плазме [Пин], и, определив его концентрацию в определенном объеме (V) конечной мочи [Мин], рассчитывают, какой объем первичной мочи соответствует найденной концентрации инулина. Насколько выросла концентрация инулина в конечной моче по сравнению с его концентрацией в плазме, во столько раз больше объем профильтровавшейся плазмы (т. е. первичной мочи) объема конечной мочи. Этот показатель получил название «клиренса» инулина или коэффициента очищения и рассчитывается по формуле:
показывающей, в каком объеме плазмы крови в единицу времени выделилось в мочу найденное количество инулина или какой объем плазмы «очистился» от инулина. По мере прохождения мочи по канальцам вода всасывается обратно в кровь и концентрация инулина растет, что и находят в конечной моче.
Поскольку инулин в организме отсутствует, для определения СКФ его необходимо капельно вводить в кровоток, создавая постоянную концентрацию. Это затрудняет исследование, поэтому в клинике обычно используют эндогенное вещество креатинин, концентрация которого в крови довольно стабильна.
Сравнивая клиренс инулина с клиренсом других веществ, определяют процессы, участвующие в выделении этих веществ с мочой. Если клиренс определенного вещества равен клиренсу инулина, значит вещество выделяется почками только путем фильтрации в клубочках. Если клиренс вещества больше клиренса инулина, следовательно, вещество выделяется не только за счет фильтрации, но и секрецией эпителием канальцев. Если клиренс вещества меньше, чем у инулина,— вещество после фильтрации реабсорбируется в канальцах.
В норме СКФ составляет у мужчин около 125 мл/мин, а у женщин — 110 мл/мин. В сутки образуется около 180 л первичной мочи, а за 25 мин фильтруется примерно 3 л плазмы крови, т. е. весь циркулирующий ее объем. За сутки этот объем плазмы крови фильтруется, т. е. очищается, примерно 60 раз. Так как объем конечной мочи составляет около 1,5 л в сутки, очевидно, что из объема первичной мочи за это время всасывается в канальцах обратно в кровь примерно 178,5 л жидкости.
Основные положения проекта рекомендаций Всероссийского научного общества кардиологов и научного общества нефрологов России по оценке функционального состояния почек у больных сердечно-сосудистыми заболеваниями или с повышенным риском их развития
1-Российский университет дружбы народов; 2- Московская медицинская академия им. И.М. Сеченова; 3-ФГУ Государственный научно-исследовательский центр профилактической медицины Росмедтехнологии. Москва, Россия
Введение
Нарушения функции почек встречаются часто у пациентов с сердечно-сосудистыми заболеваниями (ССЗ): артериальной гипертонией (АГ), особенно в сочетании с сахарным диабетом (СД), сердечной недостаточностью (СН) и др. Вовлечение почек при многих заболеваниях, в т.ч. исходно не считающихся нефропатиями, делает необходимой разработку унифицированных подходов к ведению пациентов с хронической почечной недостаточностью (ХПН), особенно в плане раннего предупреждения и лечения ее осложнений, например, анемии, нарушений фосфорно-кальциевого обмена, существенно ухудшающих прогноз других заболеваний.
Снижение скорости клубочковой фильтрации (СКФ) рассматривают в качестве маркера неблагоприятного прогноза распространенных в популяции заболеваний, прежде всего ССЗ, что вполне соответствует утвердившейся концепции кардиоре-нальных взаимоотношений [1—3]. Нарушения функции почек являются важным фактором риска (ФР) развития сердечно-сосудистых осложнений (ССО). Сердечно-сосудистая смертность в 10—30 раз выше у пациентов, находящихся на гемодиализе, чем в общей популяции. Результаты эпидемиологических и популяционных исследований свидетельствуют о том, что даже самые ранние субклинические нарушения функции почек являются независимым ФР сердечно-сосудистых событий и смерти, а также повторных событий у пациентов с ССЗ [4].
Частота умеренного, потенциально обратимого или, по крайней мере, стабилизируемого снижения СКФ значительно превосходит частоту терминальной хронической почечной недостаточности (ТХПН).
Назначение медикаментозной терапии способно снизить риск развития ССО и почечных осложнений, замедлить прогрессирование нарушения функции почек. Сохранение субклинических нарушений функции почек на фоне лечения, даже при достижении контроля ФР, например артериального давления (АД), и регрессе других органных поражений, может отрицательно сказываться на прогнозе пациента. Таким образом, оценка функционального состояния почек важна для выбора профилактических и терапевтических мероприятий [National Kidney Foundation. Clinical Practice Guidelines for chronic kidney disease — 2007 kDOQI] [5].
Целями настоящих рекомендаций являются: определение наиболее обоснованных с точки зрения доказательной медицины и применимых в широкой клинической практике методов оценки функции почек; гармонизация национальных рекомендаций с международными руководствами; стандартизация (унифицирование) терминологии для характеристики функционального состояния почек.
Основная область применения рекомендаций — оценка функционального состояния почек у пациентов с ССЗ или повышенным риском их развития с целью стратификации пациентов по риску и выбора медикаментозной терапии.
Основные определения
С целью характеристики функционального состояния почек предлагается использовать следующие термины [6—8]. Хроническая болезнь почек (ХБП) отражает наличие почечного повреждения и/или характеристику СКФ.
— Почечное повреждение > 3 месяцев, со снижением СКФ или без него, определяемое как
• патологические отклонения или
• маркеры повреждения, включая изменения в анализах крови и мочи или при визуализирующих исследованиях;
— СКФ 3 месяцев, с почечным повреждением или без него.
Почечное повреждение — это структурные или функциональные отклонения со стороны почек. Первоначально они могут иметь место при нормальной СКФ, но со временем могут привести к ее снижению. Маркеры почечного повреждения включают в себя изменения в составе крови или мочи и в результатах визуализирующих исследований. Все лица с почечным повреждением независимо от уровня СКФ рассматриваются как имеющие ХБП.
Таким образом, к лицам, имеющим ХБП, относятся:
Основным недостатком является недостаточная точность расчета СКФ по формуле MDRD у пациентов с нормальной или незначительно сниженной функцией почек. При скрининге использование формулы MDRD завышает количество пациентов с ХБП. Не установлена точность формулы у больных ССЗ. Однако у пациентов с дисфункцией левого желудочка (ЛЖ) продемонстрировано, что СКФ 2 положительными количественными тестами с интервалом от одной до двух недель следует рассматривать как имеющих персистирующую патологическую экскрецию белка с мочой; проводить их дальнейшее обследование и лечение. Мониторинг экскреции белка с мочой следует осуществлять количественными методами.
Для количественного определения экскреции Ал с мочой используются радиоиммунные, иммуноферментные и иммунотурбидиметрические методы. Определяется количество экскретируемого Ал за сутки, скорость экскреции, отношение Ал/Кр в произвольном образце мочи. Возможно использование аппаратов для экспресс-диагностики «HemoCue».
Измерение экскреции белка за 24 ч долгое время считалось «золотым стандартом» для количественной оценки протеинурии. По данным некоторых исследований экскрецию белка следует измерять в собранной за ночь порции мочи. Сравнение экскреции белка при ночном и дневном сборе мочи позволяет выявить ортостатическую протеинурию.
Сбор образцов мочи за определенное время неудобен, и может быть сопряжен с ошибками. Концентрация белка в произвольных пробах мочи является грубым показателем скорости экскреции белка; на нее также влияет степень гидратации. Альтернативным методом количественной оценки протеинурии служит измерение отношения содержания белка или Ал к содержанию
Кр в нефиксированном по времени произвольном образце мочи. Соотношения белок/Кр и Ал/Кр в моче дают точную оценку экскреции белков и Ал с мочой и не подвержены влиянию гидратации. Предпочтительна первая утренняя порция мочи, поскольку она лучше коррелирует с 24-часовой экскрецией белка. Если первая утренняя порция мочи недоступна, приемлем произвольный образец мочи.
Диагностические критерии микроальбуминурии (МАУ) и протеинурии. В зависимости от метода определения, диагностическими считают следующие показатели белка (таблица 5). Поскольку экскреция Кр у мужчин выше, чем у женщин, уровни отношения Ал/Кр в моче у мужчин ниже, чем у женщин. Прогностическое значение МАУ в отношении развития ССО позволило предложить термин «альбуминурия низкой степени», диктующий необходимость определения уровня экскреции Ал с мочой
Таблица 5. Определение альбуминурии и протеинурии..
Классификация хронической болезни почек
Классификация ХБП основана на величине СКФ, рассчитанной по формуле MDRD, и наличии почечного повреждения (таблицы 6 и 7) [6,14—16]. Расчет СКФ по формуле MDRD рекомендуется в качестве классифицирующего показателя функционального состояния почек, т.к. формула MDRD наиболее надежно валиди-рована для оценки СКФ у взрослых, для расчета СКФ этим методом используются легко доступные параметры (элементарные демографические данные и Кр сыворотки), показатель может быть рассчитан автоматически и представлен в лабораторном отчет
Таблица 6. Стадии хронической болезни почек.е

Таблица 7. Стадии хронической болезни почек в зависимости от наличия почечного повреждения.
Скрининг пациентов для выявления нарушения функции почек
Рекомендуется следующий алгоритм для выявления нарушения функции почек:
если значения СКФ 30 мг/г сохраняются, по крайней мере, 3 мес.:
Выявление почечного повреждения
У пациентов с ХБП следует оценить наличие почечного повреждения. МАУ/протеинурия являются чувствительными показателями гломеруляр-ной патологии. Для обнаружения других типов ХБП необходимо исследовать осадок мочи (возможно, тест-полосками на эритроциты и лейкоциты) и выполнить визуализирующие исследования: ультразвуковое исследование (УЗИ), внутривенная урография, компьютерная томография, магнито-резонансная томография, радиоизотопная ренография. Общий анализ мочи и УЗИ почек являются полезными неинвазивными методами диагностики почечного повреждения.
Рекомендации по выявлению нарушения функции почек у взрослых пациентов с ССЗ или повышенным риском их развития
Ведение пациентов с ХБП и мониторирование функции почек
Коррекция АД и общие принципы ведения пациентов с ХБП
План ведения пациентов с ХБП учитывает стадию нарушения функции почек (таблицы 9 и 10) [6
Таблица 9. План клинических действий в зависимости от стадии ХБП.]

Таблица 10. Тактика ведения пациентов в зависимости от степени снижения СКФ.
ХБП и ССЗ имеют ряд общих потенциально модифицируемых ФР; наиболее важные среди них — АГ и СД. Для предупреждения/замедления прогрес-сирования ХБП строгий контроль АД и гликемии имеют ключевое значение. Целевым уровнем АД у пациентов с ХБП 3—5 стадии следует считать 5 ммоль/л, уровнем Кр сыворотки
221 мкмоль/л (2,5 мг/дл) следует начинать с осторожностью. Назначение ИАПФ и АРА II пациентам с ХБП требует мониторирования функции почек (таблица 11). Транзиторное снижение СКФ в начале лечения является ожидаемым. Снижение СКФ >30 % от исходного уровня требует коррекции дозы. ИАПФ и АРА II отменить при уровне Кр сыворотки.
Таблица 11. Рекомендованные интервалы мониторирования побочных эффектов ИАПФ и АРАII после начала терапии, увеличения дозы или достижения целевого АД.
265 мкмоль/л (3 мг/дл) или при его повышении > 50 % от исходного, а также при гиперкалиемии (> 6 ммоль/л).
Коррекция анемии [22, 23]
Выявление и оценка степени тяжести анемии.
Уровень гемоглобина (Hb) следует контролировать у всех больных с ХБП не реже 1 раза в год, диагноз анемии устанавливается на основании снижения концентрации Hb согласно критериям ВОЗ:
В настоящее время недостаточно данных, чтобы рекомендовать поддерживать уровень Hb > 130 г/л у больных ХБП, получающих терапию эритропоэз-стимулирующими препаратами (ЭСП).
Не рекомендуется поддерживать уровень Hb > 120 г/л у больных с тяжелой сердечно-сосудистой патологией — III-IV функциональных классов ХСН по классификации Нью-йоркской ассоциации сердца (NYHA).
Не желательно добиваться повышения уровня НЬ > 120 г/л у больных СД 2 типа (СД-2), особенно при сопутствующем поражении периферических сосудов.
Возможно, для больных с хроническими заболеваниями легких допустимы более высокие значения НЬ.
Лечение анемии.
Коррекция дислипидемии (ДЛП) [24]
Выявление ДЛП.
Все больные ХБП должны быть обследованы на наличие ДЛП с определением липидного профиля (ЛП) натощак: общий холестерин (ОХС), липоп-ротеины низкой плотности (ЛНП), липопротеины высокой плотности (ЛВП) и триглицериды (ТГ).
Лечение ДЛП.
Больным > 18 лет ХБП стадии 5 и уровнем ТГ натощак > 5,65 ммоль/л показана коррекция образа жизни и, при необходимости, препараты, снижающие содержание ТГ.
Больным >18 лет ХБП стадии 5 и уровнем ЛНП > 2,59 ммоль/л, показана терапия для снижения ЛНП до 18 лет с ХБП стадии 5 и уровнем ЛНП 2,26 ммоль/л и холестерином-не-ЛВП (ХСЛВП) > 3,36 ммоль/л, показана терапия для снижения ХС-не-ЛВП до 133 мкмоль/л (1,5 мг/дл) у мужчин, > 124 мкмоль/л (1,4 мг/дл) у женщин, снижение СКФ 300 мг/г) свидетельствуют об очень высоком риске развития ССО.
Повышенное нормальное АД (130—139/85— 89 мм рт.ст.) предрасполагает к развитию МАУ: вероятность ее у этой категории пациентов увеличивается в 2,13 раза по сравнению со строго нормотензивными. Рост среднего АД на 10 мм рт.ст. увеличивает риск возникновения МАУ в 1,41 раза, САД в 1,27 раза, диастолического АД (ДАД) — в 1,29 раза. Повышение АД, особенно САД, является одной из наиболее значимых популяционных детерминант МАУ. У пациентов с АГ, не сочетающейся с инсули-норезистентностью (ИР) или СД-2, МАУ отражает гипертоническое поражение почек, конечным этапом которого станет глобальный нефроангиоскле-роз. У больных АГ следует отслеживать динамику МАУ при назначении АГТ. МАУ необходимо оценить после достижения адекватного контроля АД.
АГ при стенозе почечных артерий. Атеросклеротическая реноваскулярная гипертония (РВГ) — атеросклеротический стеноз почечных артерий — ишемическая болезнь почек (ИБП) занимает заметное место в структуре причин необратимого ухудшения почечной функции, особенно у пожилых. Больным атеросклеротической РВГ присуще сочетание сердечно-сосудистых ФР; характерна высокая частота курения. «Почечные» неблагоприятные последствия курения не исчерпываются только атеросклеротическим поражением почечных артерий: у курильщиков наблюдают неблагоприятную перестройку внутрипочечной гемодинамики с генерализованным нарушением микроциркуляции (МЦ), активацию процессов фиброгенеза и тромбогенеза в структурах ткани почки; поэтому курение рассматривают самостоятельным ФР ХБП.
Метаболический синдром
В настоящее время не вызывает сомнения тот факт, что именно сердечно-сосудистые ФР являются ключевыми с точки зрения формирования предрасположенности к стойкому ухудшению функции почек. Скринингу на наличие умеренной ПН подлежат те лица, у которых необходим прицельный поиск ССЗ, особенно у страдающих МС, который увеличивает вероятность развития ХБП не менее чем в 2,6 раза. Изучение взаимосвязей ХБП с МС позволяет утверждать, что высокая распространенность снижения СКФ в общей популяции определяется главным образом нефропатиями обменного генеза — диабетической, уратной, ассоциированной с ожирением, а также гипертоническим нефроангиосклерозом. Факторы, приводящие к их развитию, во многом связаны с особенностями образа жизни; их своевременное и, по возможности, полное устранение
Хроническая сердечная недостаточность
Хорошо известна высокая частота снижения СКФ при ХСН. Само по себе ухудшение фильтрационной функции почек при ХСН увеличивает риск смерти у больных как с умеренным, так и с выраженным снижением фракции выброса (ФВ) ЛЖ. При сниженной систолической функции ЛЖ риск смерти пациентов при наличии ПН возрастает в 3,8 раза, при неизмененной систолической функции — в 2,9 раза. В когорте лиц, включенных в три ветви хорошо известного исследования CHARM (Candesartan in Heart failure: Assessment of Reduction in Mortality and morbidity), снижение СКФ увеличивало частоту смерти и госпитализаций, связанных с ХСН.
У больных с ХСН нередко наблюдают дальнейшее нарастание уровня сывороточного Кр после назначения ИАПФ. Именно нарушение функции почек в наибольшей степени ограничивает возможность применения этого класса препаратов у больных с ХСН, что всегда приводит к значительному снижению эффективности лечения последней, особенно с позиции улучшения долгосрочного прогноза. Следует подчеркнуть высокий риск дальнейшего ухудшения функции почек при ХСН, обусловленной назначением ИАПФ в больших дозах без должного контроля Кр и калия сыворотки, передозировкой петлевых или тиазидных диуретиков, применением некоторых антибактериальных препаратов, рентген-контрастных агентов, а также нестероидных противовоспалительных препаратов, что делает необходимым мониторинг СКФ при ХСН.
При выраженных нарушениях сократимости миокарда ЛЖ снижение СКФ, как правило, совпадает с появлением другого неблагоприятного маркера — роста концентрации натрийуретических пептидов в плазме.
Острый коронарный синдром (ОКС) и инфаркт миокарда (ИМ)
При анализе большой (n=130099) группы пожилых больных острым ИМ (ОИМ) было установлено, что смертность в течение первого года среди больных с сохранной функцией почек составляет 24 %; при умеренном (Кр сыворотки 1,5—2,4 мг/дл) нарушении функции почек — 46 %; при величине сывороточного Кр 2,5—3,9 мг/дл — 66 % (р 0,5 мг/дл в течение суток в период госпитализации, связанной с ОИМ, существенно увеличивает риска смерти в течение последующих 12 мес.
Стойкое снижение СКФ ухудшает прогноз и при остром коронарном синдроме (ОКС). По данным канадского регистра GRACE (Global Registry of Acute Coronary Events) (n=11774) у больных ОИМ с подъемом сегмента ST, не Q-ИМ и нестабильной стенокардией, СКФ в диапазоне 30—60 мл/мин увеличивала риск смерти в 2,09 раза; при СКФ 15 лет) наблюдении за ними.
Заключение
Высокая распространенность стойкого снижения СКФ и неблагоприятный общий прогноз, свойственный этой категории лиц, определяют необходимость раннего выявления и, по возможности, предупреждения ХПН. Очевидна актуальность попыток популяцион-ного подхода к профилактике прогрессирующего необратимого ухудшения функции почек и связанных с ним осложнений, прежде всего, ССО. Констатация снижения СКФ требует активного отношения к предрасполагающим факторам, которые во многом аналогичны известным при ССЗ. Добиться увеличения продолжительности активной жизни этой категории больных возможно лишь при устранении обменных нарушений, курения, АГ, при постоянном приеме лекарственных препаратов, если необходимо — патогенетическом лечении диагностированных хронических нефропатий
Основные клинические исследования у больных с нарушением функции почек