что в печени превращается в гликоген
Что в печени превращается в гликоген
Факторы, определяющие выживаемость у пациентов с протоковой аденокарциномой поджелудочной железы
Как повысить частоту обнаружения аденом правых отделов толстой кишки?
Сравнение различных методов дренирования желчного пузыря при остром холецистите
Частота неполной резекции колоректальных полипов. Результаты систематического обзора и мета-анализа
Плюсы и минусы экстренного эндоскопического исследования у пациентов с острым кровотечением из верхних отделов ЖКТ
Эндометриоз
Эндометриоз – заболевание, при котором происходит разрастание ткани аналогичной эндометрию, и подвергающейся циклическим изменениям, за пределами слизистой оболочки тела матки. Различают генитальный (локализация процесса во внутренних и наружных половых органах), и экстрагенитальный (развитие эндометриоидной ткани в других органах и системах) эндометриоз.
Обычно заболевание встречается у женщин в возрасте 30-50 лет. Однако, в последнее время, эндометриоз помолодел и часто диагностируется и у 20-летних девушек. Около 5% бесплодных женщин страдают от эндометриоза яичника, прямой кишки, мочевого пузыря и других органов.
Причины и механизмы развития заболевания полностью не изучены. Этому могут способствовать много факторов: аномалии развития репродуктивной системы, способствующие забросу крови в брюшную полость и имплантации эндометриодных очагов; нарушение иммунного статуса, в результате чего происходят гормональные сдвиги, повышающие инвазивность эндометрия и способствующие внедрению эндометриоидных частиц в мышцы матки.
К клиническим симптомам эндометриоза относятся обильные менструальные выделения, боли, мажущие кровянистые выделения до и после менструации. Часто единственным симптомом пациенток с эндометриозом является бесплодие. Причинная связь между этими заболеваниями неясна. Существует несколько теорий, объясняющих причины бесплодия при эндометриозе. Определенное значение имеют морфологические изменения в яичниках, для которых характерны признаки дегенерации яйцеклеток, атрезия фолликулов и др. Ряд нарушений связан с наличием антител к ткани эндометрия в крови больных эндометриозом и увеличением уровня простагландинов в жидкости прямокишечно-маточного пространства.
Подходы к лечению эндометриоза подразделяют на консервативные, оперативные и комбинированные. Консервативная терапия основана на длительной гормональной терапии, включающей назначение гормональной контрацепции, производных андрогенов, агонистов гонадотропного релизинг-гормона. В случае неэффективности консервативной терапии прибегают к хирургическому лечению.
Всероссийская Образовательная Интернет-Сессия
Информация и материалы, представленные на настоящем сайте, носят научный, справочно-информационный и аналитический характер, предназначены исключительно для специалистов здравоохранения, не направлены на продвижение товаров на рынке и не могут быть использованы в качестве советов или рекомендаций пациенту к применению лекарственных средств и методов лечения без консультации с лечащим врачом.
Лекарственные препараты, информация о которых содержится на настоящем сайте, имеют противопоказания, перед их применением необходимо ознакомиться с инструкцией и проконсультироваться со специалистом.
Мнение Администрации может не совпадать с мнением авторов и лекторов. Администрация не дает каких-либо гарантий в отношении cайта и его cодержимого, в том числе, без ограничения, в отношении научной ценности, актуальности, точности, полноты, достоверности научных данных представляемых лекторами или соответствия содержимого международным стандартам надлежащей клинической практики и/или медицины основанной на доказательствах. Сайт не несет никакой ответственности за любые рекомендации или мнения, которые могут содержаться, ни за применимость материалов сайта к конкретным клиническим ситуациям. Вся научная информация предоставляется в исходном виде, без гарантий полноты или своевременности. Администрация прикладывает все усилия, чтобы обеспечить пользователей точной и достоверной информацией, но в то же время не исключает возможности возникновения ошибок.
Что в печени превращается в гликоген
Все биологические процессы, происходящие в окружающем мире, по своей сути являются химическими реакциями. Первую химическую реакцию человек осуществил, когда разжег костер – это реакция горения. Первое антибактериальное применение продуктов брожения и величайшее открытие в области медицины совершил Нострадамус. Большинство из нас знает его как предсказателя, но его основная заслуга состоит в том, что он нашел способ борьбы с чумой с помощью уксусной кислоты. История свидетельствует, чума лишила Нострадамуса и первой семьи, и друзей. С тех пор он искал средство борьбы от страшной болезни. Найдя чудо-лекарство, исследователь переезжал из города в город, где появлялась чума, спасая множество жизней [1].
Первым биохимиком была клетка, которая научилась энергетическому обмену: научилась поглощать свет и выделять энергию, необходимую для жизнеобеспечения. Таким образом, первый биохимик – это и есть сама жизнь. Все процессы, которые протекают в клетках живого организма, – это биохимические реакции.
Название «углеводы» появилось из-за того, что многие представители данного класса имеют общую формулу: Сn(Н2О)m, где n и m >= 4. Известно множество углеводов, не соответствующих этой формуле, но несмотря на это термин «углеводы» употребляется и по сей день. Другое общепринятое название этого класса соединений – сахара.
Все углеводы можно разделить на четыре больших класса.
Моносахариды – это гетерофункциональные соединения, содержащие оксогруппу и несколько гидроксильных групп. Они не могут быть гидролизованы до более простых форм углеводов и являются структурной единицей любых углеводов, например, глюкоза, фруктоза, рибулоза, рамноза. Содержатся в различных продуктах: фрукты, мёд, некоторые виды вина, шоколад.
Олигосахариды – это соединения, построенные из нескольких остатков моносахаридов, связанных между собой гликозидной связью. Они делятся по числу моносахаридов в молекуле на дисахариды, трисахариды и т.д. К биологически активным производным олигосахаридов относятся некоторые антибиотики, сердечные гликозиды.
Дисахариды – это углеводы, которые при гидролизе дают две одинаковые или различные молекулы моносахарида и связаны между собой гликозидной связью, например, лактоза, сахароза, мальтоза. При гидролизе из дисахаридов образуется глюкоза.
Полисахариды – имеют общий принцип строения с олигосахаридами, за исключением моносахаридных остатков – полисахариды могут содержать их сотни и даже тысячи. Примеры: крахмал, гликоген, хитин, целлюлоза [2].
Для лучшего понимания реакций расщепления углеводов в организме, рассмотрим более подробно глюкозу, участвующую в этих процессах.
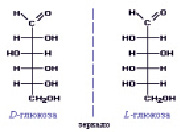
Глюкоза является одним из самых распространенных углеводов в природе, моносахарид, или гексоза С6Н12О6. Второе её название – виноградный сахар. Это растворимое в воде вещество белого цвета, сладкое на вкус. В молекуле глюкозы имеется четыре неравноценных асимметрических атома углерода (рис. 1):
Рис. 1. Строение молекулы глюкозы
Для такого соединения возможно 24 = 16 стереоизомеров, которые образуют 8 пар зеркальных оптических антиподов. Каждое из восьми соединений представляет собой диастереомер (диа – двойной) с присущими только ему физическими свойствами (растворимость, температура плавления и т.д.).
Глюкоза содержится в растительных и живых организмах. Велико ее содержание в виноградном соке, в меде, фруктах и ягодах, в семенах, листьях крапивы. Глюкоза повышает работоспособность мозга, благотворно влияет на нервную систему человека. Именно поэтому в стрессовых ситуациях люди иногда хотят чего-нибудь сладкого. Помимо этого, глюкоза применяется в медицине для приготовления лечебных препаратов, консервирования крови, внутривенного вливания и т.д. Она широко применяется в кондитерском производстве, производстве зеркал и игрушек (серебрение). Ее используют при окраске тканей и кож.
Биохимические реакции расщепления углеводов в организме человека
Для поддержания жизнедеятельности организма используется энергия, скрытая в химических связях продуктов питания. Во многих продуктах питания содержится значительное количество углеводов в виде полисахаридов (сахар, крахмал, клетчатка) и моноз (глюкоза, фруктоза, лактоза и др.). К примеру, в картофеле содержание крахмала составляет до 16 %, в рисе – 78 %, а в белом хлебе – 51 %.
Уже во рту человека начинается процесс расщепления углеводов. Происходит гидролиз крахмала под действием биологического катализатора – фермента амилазы, который содержится в пище. Под действием амилазы молекула крахмала расщепляется на довольно короткие цепочки, которые состоят из глюкозных звеньев. После этого углеводы попадают в желудок. Далее под действием желудочного сока заканчивается кислотный гидролиз крахмала. Крахмал распадается до отдельных глюкозных звеньев. Глюкоза попадает в кишечник и через стенки кишок поступает в кровь, разносящую её по всему человеческому организму.
Содержание глюкозы в крови поддерживается на постоянном уровне при помощи гормона инсулина, который выделяется поджелудочной железой. Инсулин полимеризует избыточную глюкозу в животный крахмал – гликоген, который откладывается в печени. Часть гликогена в печени может гидролизоваться в глюкозу, далее поступающую обратно в кровь. Это происходит при понижении содержания глюкозы в крови. Если поджелудочная железа не может вырабатывать инсулин, содержание глюкозы в крови повышается, что приводит к диабету. Именно поэтому людям, болеющим сахарным диабетом, необходимо регулярно вводить в кровь инсулин.
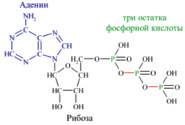
Молекула глюкозы, попадая в клетку организма, окисляется, «сгорает» с образованием воды и диоксида углерода. При этом выделяется энергия, необходимая организму для движения, согревания, осуществления различных физических нагрузок и т.д. Но биологическое окисление глюкозы похоже на обычное горение лишь по своим конечным результатам. Биологическое окисление – процесс медленный, многоступенчатый. Только малая часть высвобождаемой при окислении энергии превращается на каждой стадии данного процесса в тепло. Значительная доля энергии, заключенной в химических связях глюкозы, расходуется на образование других веществ, из которых важнейшее в биоэнергетике – аденозинтрифосфорная кислота C10H16N5O13P3 (АТФ). Это соединение состоит из трех частей – гетероцикла аденина, рибозы (сахара) и трех остатков фосфорной кислоты, образующей с рибозой сложный эфир (рис.2).
Рис. 2. Структура аденозинтрифосфорной кислоты
АТФ в клетках – универсальная энергетическая валюта. Множество ферментов умеют вести химические реакции, осуществляющиеся с затратой энергии, за счет гидролитического отщепления одного или двух остатков фосфорной кислоты от молекулы АТФ (этот процесс сопровождается выделением энергии), или наоборот, умеют использовать энергию, которая высвобождается в реакциях с выделением энергии для того, чтобы АТФ образовалась. Расщепляя АТФ, клетка использует высвобождаемую энергию на биосинтез различных соединений, а окисляя углеводы – синтезирует АТФ.
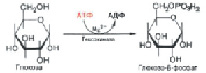
Первая стадия «сгорания» глюкозы в клетке – взаимодействие глюкозы с АТФ (рис. 3). При этом АТФ переходит в АДФ (аденозиндифосфат C10H15N5O10P2), а глюкоза – в 6-фосфат. Этот процесс фосфорилирования происходит под действием фермента гексокиназы за счет перенос остатка фосфорной кислоты (H3PO4) от фосфорилирующего агента – донора к субстрату:
Рис. 3. Взаимодействие глюкозы с АТФ
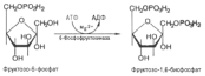
Следующий этап окисления – «рокировка» глюкозофосфата во фруктозофосфат, который происходит под действием фермента изомеразы (рис.4). Рокировка типа глюкоза–фруктоза делает доступным для фосфорилирования еще один гидроксил сахара (т.к. взаимодействовать с АТФ могут только краевые гидроксилы):
Рис. 4. Взаимодействие глюкозо-6-фосфата и фермента изомеразы
После второго фосфорилирования уже под действием другого фермента – фосфорфруктокиназы – получается в итоге фруктозо-1,6-дифосфат (C6H14O12P2 ) (рис.5):
Рис. 5. Взаимодействие фруктозо-6-фосфата и 6-фосфоруктокиназы
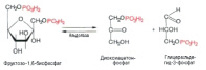
Фруктозо-1,6-дифосфат распадается на две части. Получается дигидроксиацетонфосфат ( C3H7O6P ) и глицеральдегид-3-фосфат ( C3H7O6P) (рис. 6).
Рис. 6. Распад Фруктозо-1,6-дифосфата
Клетке нужен только второй продукт, и она с помощью фермента изомеразы превращает первый фосфат во второй (чтобы не было отходов производства) (рис. 7).
Рис. 7. Превращение диоксиацетон-фосфата в глицеральдегид-3-фосфат
На данной стадии в реакцию вступают два соединения: глутатион – соединение, несущее меркаптогруппу SН и никотинамидаденинуклеотид (НАД). НАД легко присоединяет водород: НАД-Н2.
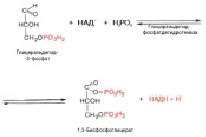
Далее развивается процесс, мало изученный в деталях, но описать его можно пока следующим образом. Под действием НАД и его восстановленной формы, фермента дегидрогеназы и фосфорной кислоты, глицеральдегид-3-фосфат превращается в смешанный ангидрид 3-фосфоглицериновой и фосфорной кислот (рис. 8).
Рис. 8. Превращение глицеральдегид-3-фосфата в смешанный ангидрид 3-фосфоглицериновой и фосфорной кислот
Всё это время энергия только поглощалась, так как АТФ переходил в АДФ. Теперь в реакции будет вступать АДФ, а в продуктах появится АТФ, и энергия будет выделяться. Так, под действием АДФ и фермента фосфоглицераткиназы образуется 3-фосфоглицериновая кислота (рис. 9).
Рис. 9. Образование 3-фосфоглицерата
В ней фермент фосфоглицеромутаза вызывает «рокировку» фосфатной группы в положение 2 (рис. 10).
Рис. 10. Превращение 3-фосфоглицерата в 2-фосфоглицерат
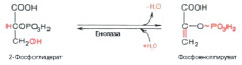
На полученный продукт воздействует фермент енолаза и АДФ – получается пировиноградная кислота (рис. 11, 12).
Рис. 11. Дегидратация 2-фосфоглицерата
Рис. 12. Перенос фосфорильной группы с фосфоенолпирувата на АДФ. Образование пирувата
Процесс превращения глюкозы в пировиноградную кислоту в клетке называется гликолизом [3]. В результате гликолиза клетка получает из одной молекулы глюкозы восемь молекул АТФ и две молекулы пировиноградной кислоты. Превращение глюкозы в пировиноградную кислоту является первой стадией, общей для нескольких процессов. То же самое происходит под действием дрожжей на раствор сахара. Но реакция не закачивается получением пировиноградной кислоты. От этой кислоты отщепляется (под действием фермента декарбоксилазы) молекула диоксида углерода и образуется уксусный альдегид, который, в свою очередь, атакуется ферментом дегидрогеназой и НАД-Н2. В результате при отсутствии кислорода получается этиловый спирт.
На самом деле уравнение этого сложного процесса выглядит довольно просто:
С6Н12О6 à 2С2Н5ОН + 2СО2
Это и есть процесс брожения. В мышцах НАД-Н2 восстанавливает пировиноградную кислоту в молочную. Это происходит при большой нагрузке, когда кровь не успевает подводить кислород в нужном количестве. Поэтому у спортсменов, пробежавших дистанцию, резко увеличивается в крови количество молочной кислоты [4].
Ферменты – это биологические катализаторы, имеющие белковую природу, помогающие ускорить химические реакции как в живых организмах, так и вне их. Ферменты обладают высокой каталитической активностью. К примеру, чтобы расщепить молекулу полиуглевода (крахмал, целлюлозу) или какой – либо белок на составные части, их нужно несколько часов кипятить с крепкими растворами щелочей либо кислот. А ферменты пищеварительных соков (пепсин, протеаза, амилаза) способны гидролизовать эти вещества буквально за несколько секунд при температуре 37 °С. Помимо этого, ферменты обладают избирательностью своего действия в отношении структуры субстрата, условий проведения реакции и её типа (фермент превращает только данный тип субстратов в определенных реакциях и условиях). Ферменты катализируют огромное количество реакций, протекающих в живой клетке при размножении, дыхании, обмене веществ и т.д. [5].
В современном понимании биохимическое расщепление углеводов – это метаболический процесс, при котором регенерируется АТФ, а продукты расщепления органического субстрата могут служить одновременно и донорами, и акцепторами водорода. Огромную роль в биохимических процессах играют микроорганизмы, ферменты и катализаторы. Считается, что анаэробный гликолиз (расщепление углеводов) был первым источником энергии для общих предков всех живых организмов до того, как концентрация кислорода в атмосфере стала достаточно высокой, и поэтому эта форма генерации энергии в клетках – более древняя. За очень редкими исключениями она существует и у всех ныне живущих клеток.
В настоящее время ученые считают, что все реакции биохимического расщепления углеводов на начальной стадии имеют общую схему вплоть до образования пировиноградной кислоты. Затем, в зависимости от условий и качества ферментов, из пировиноградной кислоты образуются конечные продукты реакции: спирты, кислоты (уксусная, лимонная, молочная, яблочная, масляная и т.д.), альдегиды, углекислый газ, водород, вода и пр.
Изучение биохимических реакций расщепления углеводов в организме человека и анализ использованных источников позволили сделать следующие выводы:
1. В общем виде схему механизма расщепления углеводов можно представить следующим образом: сложный углевод (дисахарид, полисахарид) à глюкоза à эфиры фосфорных кислот à глицериновый альдегид à глицериновая кислота à пировиноградная кислота à далее возможны любые упомянутые выше направления.
2. Биохимические реакции углеводов лежат в основе жизнедеятельности клеток живых организмов, в том числе и человека.
3. Биохимические процессы расщепления углеводов, которые изображаются простыми, на первый взгляд, уравнениями начальных и конечных продуктов, на самом деле представляют собой сложные и многоступенчатые процессы.
4. Для осуществления биохимических процессов необходимы ферменты и катализаторы, которые ускоряют реакции расщепления углеводов в тысячи раз.
Изучая сложнейшие процессы, происходящие в живой клетке, ученые задумываются: а нельзя ли, научившись у природы, провести в колбах и ретортах искусственные химические процессы, копирующие биохимические реакции? Начатые по инициативе академика Н.Н. Семенова, такие исследования в области «химической бионики» успешно ведутся в России и во всем мире [6].
Печень и ее функции в организме человека
Название «печень» происходит от слова «печь», т.к. печень обладает самой высокой температурой из всех органов живого тела. С чем это связано? Скорее всего с тем, что в печени на единицу массы происходит самое высокое количество образования энергии. До 20% массы всей клетки печени занимают митохондрии, «силовые станции клетки», которые непрерывно образуют АТФ, распределяющуюся по всему организму.
Вся ткань печени состоит из долек. Долька — это структурная и функциональная единица печени. Пространство между печеночными клетками представляют собой желчные ходы. В центре дольки проходит вена, в междольковой ткани проходят сосуды и нервы.
Кровообращение печени не похоже на кровообращение других внутренних органов. Как все органы, печень снабжается артериальной кровью, насыщенной кислородом из печеночной артерии. Через нее оттекает венозная кровь, бедная кислородом и богатая углекислым газом, и впадает в воротную вену. Однако помимо этого, обычного для всех органов кровообращения, печень получает большое количество крови, оттекающей от всего желудочно-кишечного тракта. Все, что всасывается в желудке, 12-ти перстной кишке, тонком и толстом кишечнике, собирается в большую воротную вену и впадает в печень.
Цель воротной вены не в том, чтобы снабдить печень кислородом и избавить от углекислого газа, а в том, чтобы пропустить через печень все питательные (и не питательные) вещества, которые всосались на протяжении всего желудочно-кишечного тракта. Сначала через воротную вену они проходят через печень, а потом уже в печени, претерпев определенные изменения, всасываются в общий кровоток. На долю воротной вены приходится 80% крови, получаемой печенью. Кровь воротной вены имеет смешанный характер. Она содержит как артериальную, так и венозную кровь, оттекающую от желудочно-кишечного тракта. Таким образом в печени имеются 2 капиллярные системы: обычная, между артериями и венами и капиллярная сеть воротной вены, которую иногда называют «чудесной сетью». Обычная и капиллярная чудесная сеть соединяются между собой.
Симпатическая иннервация
Иннервируется печень из солнечного сплетения и ветвями блуждающего нерва (парасимпатическая импульсация).
Через симпатические волокна стимулируется образование мочевины по парасимпатическим нервам передаются импульсы, усиливающие желчеотделение, способствующие накопление гликогена.
Печень иногда называют самой крупной эндокринной железой организма, но это не совсем верно. Печень выполняет и эндокринные выделительные функции, а также принимает участие в пищеварении.
Продукты расщепления всех питательных веществ образуют в известной степени, общий резервуар обмена веществ, который весь проходит через печень. Из этого резервуара организм по мере необходимости синтезирует необходимые вещества и расщепляет ненужные.
Углеводный обмен
Глюкоза и другие моносахариды, поступающие в печень, превращаются ею в гликоген. Гликоген откладывается в печени как «сахарный резерв». В гликоген помимо моносахаридов превращается и молочная кислота, продукты расщепления белков (аминокислоты), жиров (триглицериды и жирные кислоты). Все эти вещества начинают превращаться в гликоген в том случае, если углеводов в пище не хватает.
Пировиноградная кислота и молочная, жирные кислоты и кетоновые тела — то, что называют токсинами усталости — утилизируются в основном в печени и преобразуются в глюкозу. В организме высоктренированного спортсмена более 50% всей молочной кислоты преобразуется в печени в глюкозу.
Только в печени происходит «цикл трикарбоновых кислот», которые иначе называют «циклом Кребса» по имени английского биохимика Кребса, который, кстати говоря, жив до сих пор. Ему принадлежат классические труды по биохимии, в т.ч. и современный учебник.
Сахарный галлостаз необходим для нормальной деятельности всех систем и органом. В норме количество углеводов в крови составляет 80-120 мг% (т.е. мг на 100 мл крови), и их колебания не должны превышать 20-30 мг%. Значительное понижение содержания углеводов в крови (гипогликемия), а также стойкое повышение их содержания (гипергликемия) могут привести к тяжелым для организма последствиям.
Во время всасывания сахара из кишечника, содержание глюкозы в крови воротной вены может достигать 400 мг%. Содержание сахара в крови печеночной вены и в периферической крови повышается при этом лишь незначительно и редко достигает 200 мг%. Повышение содержания сахара в крови сразу включает «регуляторы», встроенные в печень. Глюкоза превращается, с одной стороны, в гликоген, который ускоряется, с другой стороны, она используется для получения энергии, а если и после этого остается избыток глюкозы, то она превращается в жир.
В последнее время появились данные о способности образования из глюкозы заменителя аминокислот, однако процесс носит в организме органический характер и развивается только в организме высококвалифицированных спортсменов. При понижении уровня глюкозы (длительное голодание, большой объем физических нагрузок) в печени происходит расщепление глюкогена, а если этого недостаточно, то превращаются в сахар аминокислоты и жиры, которые затем превращаются в гликоген.
Глюкозорегулитарная функция печени поддерживается механизмами нейрогуморальной регуляции (регуляция с помощью нервной и эндокринной системы). Содержание сахара в крови повышается адреналином, глюкозеном, тироксином, глюкокортикоидами и диабетогенными факторами гипофиза. При определенных условиях стабилизующим влиянием на сахарный обмен обладают половые гормоны.
Глюкозостатическая функция печени может подвергаться и прямому нервному воздействию. Центральная нервная система может вызвать гипергликемию как гуморальным путем, так и рефлекторно. Некоторые опыты свидетельствуют о том, что в печени существует так же система автономной регуляции уровня сахара в крови.
Белковый обмен
Роль печени в белковом обмене заключается в расщеплении и «перестройке» аминокислот, образовании химически нейтральной мочевины из токсичного для организма аммиака, а также в синтезе белковых молекул. Аминокислоты, которые всасываются в кишечнике и образуются при расщеплении тканевого белка, составляют «резервуар аминокислот» организма, который может служить как источником энергии, так и строительным материалом для синтеза белков. Изотопными методами было установлено, что в организме человека в стуки расщепляется и вновь синтезируется 80-100 г белка. Приблизительно половина этого белка трансформируется в печени. Об интенсивности белковых превращений в печени можно судить по тому, что белки печени обновляются примерно за 7 (!) дней. В других органах этот процесс происходит как минимум за 17 дней. В печени содержится так называемый «резервный белок», который идет на нужды организма в том случае, если не хватает белка с пищей. При двухдневном голодании печень теряет примерно 20% своего белка, в то время, как общая потеря белка всех других органов составляет только около 4%.
Трансформация и синтез недостающих аминокислот могут происходить только в печени; даже если печень удалить на 80%, такой процесс, как дезаминирование, сохраняется. Образование заменимых аминокислот в печени идет через образование глютаминовой и аспарагиновой кислоты, которые служат как бы промежуточным звеном.
Избыточное количество той или иной аминокислоты подвергается снижению сначала до пировиноградной кислоты, а потом в цикле Кребса до воды и углекислого газа с образованием энергии, запасаемой в виде АТФ.
В процессе деземинирования аминокислот — отщепления от них аминогрупп, образуется большое количество токсичного аммиака. Печень преобразует аммиак в нетоксичную мочевину (карбамид), который затем почками выводится из организма. Синтез мочевины происходит только в печени и нигде больше.
Синтез белков плазмы крови — альбуминов и глобулинов происходит в печени. Если произошла кровопотеря, то при здоровой печени содержание белков плазмы крови очень быстро восстанавливается при больной печени такое восстановление значительно замедляется.
Жировой обмен
Печень может депонировать жира намного больше, чем гликогена. Так называемый «структурный липоид» — структурные липиды печени фосфолипиды и холестерин составляют 10-16% сухого вещества печени. Это количество довольно постоянно. Помимо структурных липидов печень имеет включения нейтрального жира, сходного по своему составу с жиром подкожной клетчатки. Содержание нейтрального жира в печени подвержено значительным колебаниям. В целом же, можно сказать, что печень имеет определенный жировой запас, который при дефиците нейтрального жира в организме может расходоваться на энергетические нужды. Жирные кислоты при дефиците энергии могут хорошо окисляться в печени с образованием энергии, запасаемой в виде АТФ. В принципе, жирные кислоты могут окисляться и в любых других внутренних органах, однако процентное соотношение будет таким: 60% печень и 40% все остальные органы.
Желчь, выделяемая печенью в кишечник, эмульгирует жиры, и только лишь в составе такой эмульсии жиры могут впоследствии всасываться в кишечнике.
Половина имеющегося в организме холестерина синтезируется в печени и лишь другая половина имеет пищевое происхождение.
Механизм окисления печенью жирных кислот был выяснен в начале нашего века. Он сводится к так называемому b-окислению. Окисление жирных кислот происходит до 2-го углеродного атома (b-атома). Получается более короткая жирная кислота и уксусная кислота, которая потом превращается в ацетоуксусную. Ацетоуксусная кислота превращается в ацетон, а новая b-окисленная кислота подвергается окислению с большим трудом. И ацетон и b-окисленная кислота объединяют под одним названием «кетоновые тела».
Для расщепления кетоновых тел нужно достаточно большое количество энергии и при дефиците глюкозы в организме (голодание, диабет, длительные аэробные нагрузки) у человека изо рта может появиться запах ацетона. У биохимиков даже есть такое выражение: «жиры сгорают в огне углеводов». Для полного сгорания, полной утилизации жиров до воды и углекислого газа с образованием большого количества АТФ необходимо хотя бы небольшое количество глюкозы. Иначе процесс застопорится на стадии образования кетоновых тел, которые сдвигают рН крови в кислую сторону, вместе с молочной кислотой принимая участие в формировании усталости. Не зря их поэтому и называют «токсинами усталости».
На жировой обмен в печени влияют такие гормоны, как инсулин, АКТГ, диабетогенный фактор гипофиза, глюкокортикоиды. Действие инсулина способствует накоплению жира в печени. Действие АКТГ, диабетогенного фактора, глюкокортикоидов прямо противоположно. Одна из важнейших функций печени в жировом обмене — это образование жира и сахара. Углеводы — непосредственный источник энергии, а жиры — важнейшие запасы энергии в организме. Поэтому при избытке углеводов и, в меньшей степени белков, преобладает синтез жира, а при недостатке углеводов доминирует глюконеогенез (образование глюкозы) из белка и жира.
Холестериновый обмен
Холестериновые молекулы составляют структурный каркас всех без исключения клеточных мембран. Деление клеток без достаточного количества холестерина попросту невозможно. Из холестерина образуются желчные кислоты, т.е. по сути сама желчь. Из холестерина образуются все стероидные гормоны: глюкокортикоиды, минералокортикоиды, все половые гормоны.
Витамины
Все жирорастворимые витамины (А, Д, Е, К и др.) всасываются в стенки кишечника только в присутствии желчных кислот, выделяемых печенью. Некоторые витамины (А, В1, Р, Е, К, РР и др.) депонируются печенью. Многие из них участвуют в химических реакция, происходящих в печени (В1, В2, В5, В12, С, К и др.). Часть витаминов активизируется в печени, подвергаясь в ней фосфорицированию (В1, В2, В6, холин и др.). Без фосфорных остатков эти витамины совершенно неактивны и часто нормальный витаминный баланс в организме больше зависит от нормального состояния печени, чем от достаточного поступления того или иного витамина в организм.
Как видим, в печени могут депонировать как жирорастворимые, так и водорастворимые витамины, только время депонирования жирорастворимых витаминов, конечно, несоизмеримо больше, нежели водорастворимых.
Обмен гормонов
Роль печени на метаболизм стероидных гормонов не ограничивается тем, что она синтезирует холестерины — основу, из которой затем образуются все стероидные гормоны. В печени все стероидные гормоны подвергаются инактивации, хотя образуются они и не в печени.
Распад стероидных гормонов в печени является ферментативным процессом. Большая часть стероидных гормонов инактивируется, соединяясь в печени с глюкуроновой жирной кислотой. При нарушении функции печени в организме в первую очередь повышается содержание гормонов коры надпочечников, которые не подвергаются полному расщеплению. Отсюда возникает очень много различных заболеваний. Больше всего накапливается в организме альдостерона — минералокортикоидного гормона, избыток которого приводит к задержке натрия и воды в организме. В результате возникают отеки, подъем артериального давления и т. д.
В печени в значительной степени происходит инактивация гормонов щитовидной железы, антидиуретического гормона, инсулина, половых гормонов. При некоторых заболеваниях печени мужские половые гормоны не разрушаются, а превращаются в женские. Особенно часто такое расстройство возникает после отравления метиловым спиртом. Сам по себе избыток андрогенов, вызванный введением большого количества их извне, может привести к усилению синтеза женских половых гормонов. Существует, очевидно, некий порог содержания андрогенов в организме, превышение которого приводит к превращению андрогенов в женские половые гормоны. Хотя, в последнее время появились публикации о том, что некоторые лекарственные препараты способны предотвратить превращение в печени андрогенов в эстрогены. Такие препараты называют блокаторами.
Помимо вышеперечисленных гормонов печень инактивирует нейромедиаторы (катехоламины, серотонин, гистамин и многие другие вещества). В некоторых случаях даже развитие психических заболеваний вызвано неспособностью печени инактивировать те или иные нейромедиаторы.
Микроэлементы
Обмен практически всех микроэлементов напрямую зависит от работы печени. Печень, например, оказывает влияние на всасывание железа из кишечника, она депонирует железо и обеспечивает постоянство его концентрации в крови. Печень — депо меди и цинка. Она принимает участие в обмене марганца, молибдена кобальта и других микроэлементов.
Желчеобразование
Желчь, вырабатываемая печенью, как мы уже говорили, принимает активное участие в переваривании жиров. Однако дело не ограничивается всего лишь их эмульгированием. Желчь активизирует жирорасщепляющий фермент липозу панкреатического и кишечного сока. Желчь также ускоряет всасывание в кишечнике жирных кислот, каротина, витаминов Р, Е, К, холестерина, аминокислот, солей кальция. Желчь стимулирует перистальтику кишечника.
За сутки печень вырабатывает не менее 1 л желчи. Желчь представляет собой зеленовато-желтую жидкость слабощелочной реакции. Главные компоненты желчи: соли желчных кислот, желчные пигменты, холестерин, лецитин, жиры, неорганические соли. Печеночная желчь содержит до 98% воды. По своему осмотическому давлению, желчь равна плазме крови. Из печени желчь по внутрипеченочным желчным ходам поступает в печеночный проток, оттуда ее непосредственно выделяется через пузырный проток попадает в желчный пузырь. Здесь происходит концентрация желчи вследствие всасывания воды. Плотность пузырной желчи 1,026-1,095.
Часть веществ, входящих в состав желчи синтезируется непосредственно в печени. Другая часть образуется вне печени и после ряда метаболических изменений выводится с желчью в кишечник. Таким образом, желчь образуется двумя путями. Одни ее компоненты фильтруются из плазмы крови (вода, глюкоза, креатинин, калий, натрий, хлор), другие образуются в печени: желчные кислоты, глюкурониды, парные кислоты и т. д.
Печень человека вырабатывает в сутки 10-20 г желчных кислот. Попадая с желчью в кишечник, желчные кислоты расщепляются с помощью ферментов кишечных бактерий, хотя большая их часть подвергается обратному всасыванию кишечными стенками и вновь оказывается в печени.
С калом выделяется лишь 2-3 г желчных кислот, которые в результате разлагающего действия кишечных бактерий меняют зеленый цвет на коричневый и изменяют запах.
Таким образом, существует как бы печеночно-кишечный кругооборот желчных кислот. Если необходимо увеличить выведение желчных кислот из организма (например, с целью выведения из организма больших количеств холестерина), то принимаются вещества, необратимо связывающие желчные кислоты, которые не позволяют желчным кислотам всасываться в кишечнике и выводят их из организма вместе с калом. Самыми эффективными в этом плане являются специальные ионообменные смолы (например, холестирамин), которые будучи принятыми внутрь, способны связать в кишечнике очень большое количество желчи и, соответственно, желчных кислот. Ранее с этой целью использовали активированный уголь.
Желчные кислоты помимо всего прочего могут образовываться из холестерина. При употреблении мясной пищи, количество желчных кислот увеличивается, при голодании — уменьшается. Благодаря желчным кислотам и их солям, желчь выполняет свои функции в процессе пищеварения и всасывания.
Желчные пигменты (основной из них билирубин) не принимают участие в пищеварении. Их выделение печенью — чисто экскреторный выделительный процесс.
Билирубин образуется из гемоглобина разрушенных эритроцитов в селезенке и особых клетках печени (купферовские клетки). Не зря селезенку называют кладбищем эритроцитов. В отношении билирубина главной задачей печени является его выделение, а не образование, хотя немалая часть его образуется именно в печени. Интересно то, что распад гемоглобина до билирубина осуществляется при участии витамина С. Между гемоглобином и билирубином имеется множество промежуточных продуктов, способных ко взаимному превращению друг в друга. Часть их выделяется с мочой, а часть с калом.
Образование желчи регулируется центральной нервной системой путем разнообразных рефлекторных влияний. Желчеотделение происходит непрерывно, усиливаясь во время еды. Раздражение чревного нерва приводит к уменьшению образования желчи, а раздражение блуждающего нерва и гистамины увеличивают образование желчи.
Желчевыделение, т.е. поступление желчи в кишечник происходит периодически в результате сокращения желчного пузыря в зависимости от приема пищи и ее состава.
Выделительная (экскреторная) функция
Выделительная функция печени очень тесно связана с желчеобразованием, поскольку экскретируемые печенью вещества экскретируются через желчь и хотя бы уже поэтому они автоматически становятся составной частью желчи. К таким веществам относятся уже вышеописанные гормоны щитовидной железы, стероидные соединения, холестерин, медь и другие микроэлементы, витамины, порфириновые соединеиия (пигменты) и т. д.
Вещества, выделяемые практически только с желчью подразделяются на две группы:
Одна из особенностей выделительной функции желчи заключается в том, что она способна вводить из организма такие вещества, которые никаким другим образом из организма выведены быть не могут. В крови мало свободных соединений. Большинство тех же гормонов прочно соединены с транспортными белками крови и будучи прочно соединенными с белками не могут преодолеть почечный фильтр. Такие вещества выделяются из организма вместе с желчью. Другой большой группой веществ, которые не могут быть выведены с мочой являются вещества, нерастворимые в воде.
Роль печени в данном случае сводится к тому, что она соединяет эти вещества с глюкуроновой кислотой и переводит, таким образом, в водорастворимое состояние, после чего они свободно выделяются через почки.
Есть и другие механизмы, которые позволяют печени выделить из организма нерастворимые в воде соединения.
Обезвреживающая функция
Печень выполняет защитную роль не только за счет обезвреживания и выведения токсичных соединений, но, даже за счет попавших в нее микробов, которых она уничтожает. Специальные клетки печени (купферовские клетки) подобно амебам захватывают чужеродные бактерии и переваривают их.
В процессе эволюции печень превратилась в идеальный орган обезвреживания токсических веществ. Если она не может превратить токсичное вещество в полностью нетоксичное, она делает его менее токсичным. Мы уже знаем, что токсичный аммиак превращается в печени в нетоксичную мочевину (карбамид). Чаще всего печень обезвреживает токсичные соединения за счет образования с ними парных соединений с глюкурановой и серной кислотой, глицином, таурином, цистеином и др. так обезвреживаются высокотоксичные фенолы, нейтрализуются стероиды и другие вещества. Большую роль в обезвреживании играют окислительные и восстановительные процессы, ацетилирование, метилирование (поэтому для печени так полезны витамины, содержащие свободные метильные радикалы-СН3), гидролиз и др. Для выполнения печенью своей дезинтоксикационной функции, необходимо достаточное энергетическое обеспечение, а для этого, в свою очередь, необходимо достаточное содержание в ней гликогена и присутствие достаточного количества АТФ.
Свертывание крови
Перераспределение крови в организме
Печень, помимо всех своих прочих функций неплохо выполняет функцию депо крови в организме. В связи с этим она может влиять на кровообращение всего организма. Все внутрипеченочные артерии и вены имеют сфинктеры, которые в очень широких пределах могут изменять кровоток в печени. В среднем кровоток в печени составляют 23 мл/кс/мин. В норме почти 75 мелких сосудов печени выключено сфинктерами из общей циркуляции. При повышении общего кровяного давления происходит расширение сосудов печени и печеночный кровоток в несколько раз возрастает. Наоборот, падение кровяного давления приводит к сужению сосудов в печени и печеночный кровоток уменьшается.
Изменение положения тела также сопровождается изменениями печеночного кровотока. Так, например, в положении стоя кровоток печени на 40% ниже, чем в положении лежа.
Норадреналин и симпатические повышают сопротивление сосудов печени, что уменьшает количество крови, протекающей через печень. Блуждающий нерв, наоборот, уменьшает сопротивление сосудов печени, что увеличивает количество крови, протекающей через печень.
Возрастные изменения
Функциональные возможности печени человека наиболее высоки в раннем детском возрасте и очень медленно умньшаются в возрастом.
Масса печени новорожденного ребенка в среднем составляет 130-135 г. Максимума своего масса печени достигает в возрасте между 30-40 годами, а затем постепенно снижается, особенно между 70-80 годами, причем, у мужчин масса печени падает сильнее, чем у женщин. Регенерационные способности печени к старости несколько снижаются. В молодом возрасте после удаления печени на 70% (ранения, травмы и т. д.), печень восстанавливает через несколько недель утраченную ткань на 113% (с избытком). Такая высокая способность к регенерации не присуща ни одному другому органу и даже используется для лечения тяжелых хронических заболеваний печени. Так, например, некоторым больным циррозом печени, ее частично удаляют и она снова отрастает, но вырастает уже новая, здоровая ткань. С возрастом печень уже не восстанавливается полностью. У старых лиц она отрастает лишь на 91% (что, в принципе, тоже немало).
Синтез альбуминов и глобулинов падает в пожилом возрасте. Преимущественно падает синтез альбуминов. Однако, это не приводит к каким-либо нарушениями в питании тканей и падению онкотичесокого давления крови, т.к. к старости уменьшается интенсивность распада и потребления белков в плазме другими тканями. Таким образом, печень даже в старости обеспечивает потребности организма в синтезе белков плазмы. Способность печени к депонированию гликогена тоже различна в различные возрастные периоды. Гликогенная емкость достигает максимума к трехмесячному возрасту, сохраняется на всю жизнь и лишь слегка снижается к старости. Жировой обмен в печени достигает своего обычного уровня также в очень раннем возрасте и лишь незначительно снижается к старости.
На разных этапах развития организма печень вырабатывает разные количества желчи, но всегда покрывает потребности организма. Состав желчи на протяжении жизни несколько меняется. Так, если у новорожденного ребенка в печеночной желчи содержится желчных кислот около 11 мг-экв/л, то к четырехлетнему возрасту это количество снижается почти в 3 раза, а к 12 годам вновь повышается и достигает приблизительно 8 мг-экв/л.
Скорость опорожнения желчного пузыря, по некоторым данным наименьшая у молодых людей, а у детей и стариков она значительно выше.
Вообще, по всем своим показателям, печень — малостареющий орган. Она исправно служит человеку на протяжении всей его жизни.