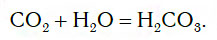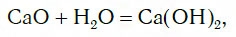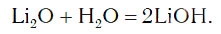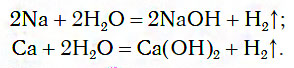что взаимодействует с водой при обычной температуре
Какие металлы реагируют с водой?
Прежде всего следует запомнить, что металлы делят в целом на три группы:
1) Активные металлы: к таким металлам относятся все щелочные металлы, щелочноземельные металлы, а также магний и алюминий.
2) Металлы средней активности: к таковым относят металлы, расположенные между алюминием и водородом в ряду активности.
3) Малоактивные металлы: металлы, расположенные в ряду активности правее водорода.
В первую очередь нужно запомнить, что малоактивные металлы (т.е. те, что расположены после водорода) с водой не реагируют ни при каких условиях.
Щелочные и щелочноземельные металлы реагируют с водой при любых условиях (даже при обычной температуре и на холоде), при этом реакция сопровождается выделением водорода и образованием гидроксида металла. Например:
Магний из-за того, что покрыт защитной оксидной пленкой, реагирует с водой только при кипячении. При нагревании в воде оксидная пленка, состоящая из MgO, разрушается и находящийся под ней магний начинает реагировать с водой. При этом реакция также сопровождается выделением водорода и образованием гидроксида металла, который, однако, в случае магния нерастворим:
Алюминий так же, как и магний, покрыт защитной оксидной пленкой, однако в этом случае кипячением ее разрушить нельзя. Для ее снятия требуются либо механическая чистка (каким-либо абразивом), либо ее химическое разрушение щелочью, растворами солей ртути или солей аммония:
Металлы средней активности реагируют с водой лишь тогда, когда она находится в состоянии перегретого водяного пара. Сам металл при этом должен быть нагрет до температуры красного каления (около 600-800 о С). В отличие от активных металлов, металлы средней активности при реакции с водой вместо гидроксидов образуют оксиды металлов. Продуктом восстановления и в этом случае является водород:
Fe + H2O = FeO + H2 (в зависимости от степени нагрева)
Урок 28. Химические свойства воды
В уроке 28 «Химические свойства воды» из курса «Химия для чайников» узнаем о взаимодействии воды с различными веществами.
При обычных условиях вода является достаточно активным веществом по отношению к другим веществам. Это означает, что со многими из них она вступает в химические реакции.
Взаимодействие с оксидами неметаллов
Если струю газообразного оксида углерода(IV) CO2 (углекислого газа) направить в воду, то часть его растворится в ней (рис. 109).
При этом в растворе протекает химическая реакция соединения, в результате которой образуется новое вещество — угольная кислота H2CO3:
На заметку: Собирая углекислый газ над водой, Дж. Пристли обнаружил, что часть газа растворяется в воде и придает ей приятный терпкий вкус. По сути дела, Пристли впервые получил напиток типа газированной, или содовой, воды.
Реакция соединения происходит также, если к воде прибавить твердый оксид фосфора(V) P2O5. При этом протекает химическая реакция с образованием фосфорной кислоты H3PO4 (рис. 110):
Испытаем растворы, полученные при взаимодействии CO2 и P2O5 с водой, индикатором метиловым оранжевым. Для этого прибавим по 1—2 капли раствора индикатора к полученным растворам. Цвет индикатора изменится с оранжевого на красный, что говорит о присутствии кислот в растворах. Значит, при взаимодействии CO2 и P2O5 с водой действительно образовались кислоты H2CO3 и H3PO4.
Оксиды, подобные CO2 и P2O5, которые при взаимодействии с водой образуют кислоты, относят к кислотным оксидам.
Кислотные оксиды — это оксиды, которым соответствуют кислоты.
Некоторые из кислотных оксидов и соответствующих им кислот приведены в таблице 11. Обратите внимание, что это оксиды элементов неметаллов. Как правило, оксиды неметаллов являются кислотными оксидами.
Взаимодействие с оксидами металлов
С оксидами металлов вода реагирует иначе, чем с оксидами неметаллов.
Исследуем взаимодействие оксида кальция CaO с водой. Для этого поместим в стакан с водой небольшое количество CaO и тщательно перемешаем. При этом протекает химическая реакция:
в результате которой образуется новое вещество Ca(OH)2, относящееся к классу оснований. Таким же образом реагируют с водой оксиды лития, натрия. При этом также образуются основания, например:
Подробнее с основаниями вы познакомитесь в следующем уроке. Оксиды металлов, которым соответствуют основания, называют основными оксидами.
Основные оксиды — это оксиды, которым соответствуют основания.
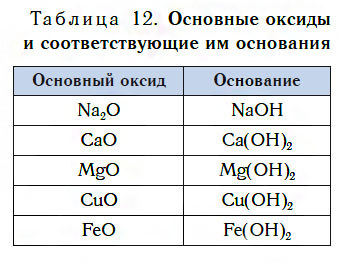
В таблице 12 приведены формулы некоторых основных оксидов и соответствующих им оснований. Заметьте, что, в отличие от кислотных оксидов, в состав основных оксидов входят атомы металлов. Большинство оксидов металлов — это основные оксиды.
Несмотря на то что каждому основному оксиду соответствует основание, не все основные оксиды взаимодействуют с водой, подобно CaO, образуя основания.
Взаимодействие с металлами
При обычных условиях активные металлы (K, Na, Ca, Ba и др.) бурно реагируют с водой:
В этих реакциях выделяется водород и образуются растворимые в воде основания.
Как химически активное вещество вода вступает в реакции со многими другими веществами, но об этом вы узнаете при дальнейшем изучении химии.
Краткие выводы урока:
Надеюсь урок 28 «Химические свойства воды» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Какие металлы взаимодействуют с водой при обычной температуре
ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ
Щелочно-земельные металлы – это II группа, А – главная подгруппа (Be, Mg не относятся) – Ca, Sr, Ba, Ra
Основания – это сложные вещества с общей формулой Ме(ОН)n
ОН – гидроксильная группа, с валентностью (I)
Щёлочи – это растворимые в воде основания (см. ТАБЛИЦУ РАСТВОРИМОСТИ)
Кислоты – это сложные вещества с общей формулой Нn (КО)
(КО) – кислотный остаток
Кислотный оксид – неМех Оу и Мех Оу
Основные оксиды – Мех Оу
I. Взаимодействие воды с металлами.
В зависимости от активности металла, реакция протекает при различных условиях и образуются разные продукты.
1). Взаимодействие с самыми активными металлами, стоящими в периодической системе в I А и I I А группах (щелочные и щелочно-земельные металлы) и алюминий. В ряду активности эти металлы расположены до алюминия (включительно)
Реакция протекает при обычных условиях, при этом образуется щелочь и водород.
2Li + 2 H2O = 2 Li OH + H2 (протекает реакция замещения)
Ba + 2 H2O = Ba (OH)2 + H2
2 Al + 6 H2O = 2 Al (OH)3 + 3 H2
ОН – гидроксогруппа, она всегда одновалентна
2) Взаимодействие с менее активными металлами, которые расположены в ряду активности от алюминия до водорода.
Реакция протекает только с парообразной водой, т.е. при нагревании.
При этом образуются: оксид этого металла и водород.
Fe + H2O = FeO + H2 (протекает реакция замещения)
(Валентность металла можно легко определить по ряду активности металлов, над их символом стоит значение, например +2, это означает, что валентность этого металла равна 2).
Me + Н2О = Мех Оу + Н2 (р. замещения)
3) Металлы, стоящие в ряду активности после водорода, не реагируют с водой.
Cu + H2O = нет реакции
I I. Взаимодействие с оксидами (основными и кислотными)
С водой взаимодействуют только такие оксиды, которые при взаимодействии с водой дают растворимый в воде продукт (кислоту или щелочь).
1). Взаимодействие с основными оксидами.
С водой взаимодействуют только основные оксиды активных металлов, которые расположены в в I А и I I А группах, кроме Ве и Mg (оксид алюминия не реагирует, т.к. он амфотерный). Реакция протекает при обычных условиях, при этом образуется только щелочь.
Na2O + H2O = 2 NaOH BaO + H2O = Ba (OH)2 (протекает реакция соединения)
Al2O3 + H2O = нет реакции
BeO + H2O = нет реакции
MgO + H2O = нет реакции
2) Взаимодействие кислотных оксидов с водой.
Кислотные оксиды реагируют с водой все. Исключение составляет только SiO2.
При этом образуются кислоты. Во всех кислотах на первом месте расположен водород, поэтому уравнение реакции записывают так:
SO3 + H2O = H2SO4 P2O5 + H2O = 2 HPO3
P2O5 + 3 H2O = 2 H3 PO4
Обратите внимание, что в зависимости от температуры воды при взаимодействии с Р2 О5 образуются разные продукты.
H2O + КИСЛОТНЫЙ ОКСИД = Hn A (р. соединения)
Внимание! SiO2 + H2O = нет реакции
IV Взаимодействие воды c неметаллами
Примеры: Cl2 + H2O = HCl + HClO
IIA группа содержит только металлы – Be (бериллий), Mg (магний), Ca (кальций), Sr (стронций), Ba (барий) и Ra (радий). Химические свойства первого представителя этой группы — бериллия — наиболее сильно отличаются от химических свойств остальных элементов данной группы. Его химические свойства во многом даже более схожи с алюминием, чем с остальными металлами IIA группы (так называемое «диагональное сходство»). Магний же по химическим свойствами тоже заметно отличается от Ca, Sr, Ba и Ra, но все же имеет с ними намного больше сходных химических свойств, чем с бериллием. В связи со значительным сходством химических свойств кальция, стронция, бария и радия их объединяют в одно семейство, называемое щелочноземельными металлами.
Вследствие особенностей электронного строения металлов IIA группы, данные элементы, помимо нуля, способны иметь только одну единственную степень окисления, равную +2. Простые вещества, образованные элементами IIA группы, при участии в любых химических реакциях способны только окисляться, т.е. отдавать электроны:
Ме0 – 2e— → Ме+2
Кальций, стронций, барий и радий обладают крайне высокой химической активностью. Простые вещества, образованные ими, являются очень сильными восстановителями. Также сильным восстановителем является магний. Восстановительная активность металлов подчиняется общим закономерностям периодического закона Д.И. Менделеева и увеличивается вниз по подгруппе.
Взаимодействие с простыми веществами
с кислородом
Без нагревания бериллий и магний не реагируют ни с кислородом воздуха, ни с чистым кислородом ввиду того, что покрыты тонкими защитными пленками, состоящими соответственно из оксидов BeO и MgO. Их хранение не требует каких-либо особых способов защиты от воздуха и влаги, в отличие от щелочноземельных металлов, которые хранят под слоем инертной по отношению к ним жидкости, чаще всего керосина.
Be, Mg, Ca, Sr при горении в кислороде образуют оксиды состава MeO, а Ba – смесь оксида бария (BaO) и пероксида бария (BaO2):
Следует отметить, что при горении щелочноземельных металлов и магния на воздухе побочно протекает также реакция этих металлов с азотом воздуха, в результате которой, помимо соединений металлов с кислородом, образуются также нитриды c общей формулой Me3N2.
с галогенами
Бериллий реагирует с галогенами только при высоких температурах, а остальные металлы IIA группы — уже при комнатной температуре:
Мg + I2 = MgI2 – иодид магния
Са + Br2 = СаBr2 – бромид кальция
Ва + Cl2 = ВаCl2 – хлорид бария
с неметаллами IV–VI групп
Все металлы IIA группы реагируют при нагревании со всеми неметаллами IV–VI групп, но в зависимости от положения металла в группе, а также активности неметаллов требуется различная степень нагрева. Поскольку бериллий является среди всех металлов IIA группы наиболее химически инертным, при проведении его реакций с неметаллами требуется существенно большая температура.
Остальные металлы II А группы образуют с углеродом ацетилениды:
С кремнием металлы IIA группы образуют силициды — соединения вида Me2Si, с азотом – нитриды (Me3N2), фосфором – фосфиды (Me3P2):
с водородом
Все щелочноземельные металлы реагируют при нагревании с водородом. Для того чтобы магний прореагировал с водородом, одного нагрева, как в случае со щелочноземельными металлами, недостаточно, требуется, помимо высокой температуры, также и повышенное давление водорода. Бериллий не реагирует с водородом ни при каких условиях.
Взаимодействие со сложными веществами
с водой
Все щелочноземельные металлы активно реагируют с водой с образованием щелочей (растворимых гидроксидов металлов) и водорода. Магний реагирует с водой лишь при кипячении вследствие того, что при нагревании в воде растворяется защитная оксидная пленка MgO. В случае бериллия защитная оксидная пленка очень стойкая: с ним вода не реагирует ни при кипячении, ни даже при температуре красного каления:
c кислотами-неокислителями
Все металлы главной подгруппы II группы реагируют с кислотами-неокислителями, поскольку находятся в ряду активности левее водорода. При этом образуются соль соответствующей кислоты и водород. Примеры реакций:
Ве + Н2SO4(разб.) = BeSO4 + H2↑
Mg + 2HBr = MgBr2 + H2↑
Ca + 2CH3COOH = (CH3COO)2Ca + H2↑
c кислотами-окислителями
− разбавленной азотной кислотой
С разбавленной азотной кислотой реагируют все металлы IIA группы. При этом продуктами восстановления вместо водорода (как в случае кислот-неокислителей) являются оксиды азота, преимущественно оксид азота (I) (N2O), а в случае сильно разбавленной азотной кислоты – нитрат аммония (NH4NO3):
4Mg + 10HNO3(сильно разб.) = 4Mg(NO3)2 + NН4NO3 + 3H2O
− концентрированной азотной кислотой
Концентрированная азотная кислота при обычной (или низкой) температуре пассивирует бериллий, т.е. в реакцию с ним не вступает. При кипячении реакция возможна и протекает преимущественно в соответствии с уравнением:
Магний и щелочноземельные металлы реагируют с концентрированной азотной кислотой с образованием большого спектра различных продуктов восстановления азота.
− концентрированной серной кислотой
Бериллий пассивируется концентрированной серной кислотой, т.е. не реагирует с ней в обычных условиях, однако реакция протекает при кипячении и приводит к образованию сульфата бериллия, диоксида серы и воды:
Be + 2H2SO4 → BeSO4 + SO2↑+ 2H2O
Барий также пассивируется концентрированной серной кислотой вследствие образования нерастворимого сульфата бария, но реагирует с ней при нагревании, сульфат бария растворяется при нагревании в концентрированной серной кислоте благодаря его превращению в гидросульфат бария.
Остальные металлы главной IIA группы реагируют с концентрированной серной кислотой при любых условиях, в том числе на холоду. Восстановление серы происходит преимущественно до сероводорода:
4Mg + 5H2SO4(конц.) = 4MgSO4 + H2S↑ + 4H2O
с щелочами
Магний и щелочноземельные металлы со щелочами не взаимодействуют, а бериллий легко реагирует как растворами щелочей, так и с безводными щелочами при сплавлении. При этом при осуществлении реакции в водном растворе в реакции участвует также и вода, а продуктами являются тетрагидроксобериллаты щелочных или щелочноземельных металлов и газообразный водород:
Be + 2KOH + 2H2O = H2↑ + K2[Be(OH)4] — тетрагидроксобериллат калия
При осуществлении реакции с твердой щелочью при сплавлении образуются бериллаты щелочных или щелочноземельных металлов и водород
Be + 2KOH = H2↑+ K2BeO2 — бериллат калия
с оксидами
Щелочноземельные металлы, а также магний могут восстанавливать менее активные металлы и некоторые неметаллы из их оксидов при нагревании, например:
Метод восстановления металлов из их оксидов магнием называют магниетермией.
Среди металлов традиционно выделяют несколько групп. Входящие в их состав представители характеризуются отличной от других металлов химической активностью. Такими группами являются:
Простые вещества, обладающие металлическими свойствами, в химических реакциях всегда являются восстановителями. Положение металла в ряду активности характеризует то, насколько активно данный металл способен вступать в химические реакции (т. е. то, насколько сильно у него проявляются свойства восстановителя).
Ряд активности металлов
Какие металлы реагируют с водой?
В первую очередь нужно запомнить, что малоактивные металлы (т. е. те, что расположены после водорода) с водой не реагируют ни при каких условиях.
Щелочные и щелочноземельные металлы реагируют с водой при любых условиях (даже при обычной температуре и на холоде), при этом реакция сопровождается выделением водорода и образованием гидроксида металла. Например:
2Na + 2H2O = 2NaOH + H2↑
Ca + 2H2O = Ca(OH)2 + H2↑
Магний из-за того, что покрыт защитной оксидной пленкой, реагирует с водой только при кипячении. При нагревании в воде оксидная пленка, состоящая из MgO, разрушается и находящийся под ней магний начинает реагировать с водой. При этом реакция также сопровождается выделением водорода и образованием гидроксида металла, который, однако, в случае магния нерастворим:
Mg + 2H2O = Mg(OH)2↓ + H2↑
Алюминий так же, как и магний, покрыт защитной оксидной пленкой, однако в этом случае кипячением ее разрушить нельзя. Для ее снятия требуются либо механическая чистка (каким-либо абразивом), либо ее химическое разрушение щелочью, растворами солей ртути или солей аммония:
2Al + 6H2O = 2Al(OH)3 + 3H2↑
Металлы средней активности реагируют с водой лишь тогда, когда она находится в состоянии перегретого водяного пара. Сам металл при этом должен быть нагрет до температуры красного каления (около 600-800 оС). В отличие от активных металлов, металлы средней активности при реакции с водой вместо гидроксидов образуют оксиды металлов. Продуктом восстановления и в этом случае является водород:
Zn + 2H2O = Zn(OH)2 + H2↑
3Fe + 4H2O = Fe3O4 + 4H2 или
Fe + H2O = FeO + H2 (в зависимости от степени нагрева)
Вода в нашей жизни
Продолжение. Начало см. в № 3, 4/2009
§ 2. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ

Форма занятия. Лекция с элементами беседы, демонстрационный эксперимент исследовательского характера, лабораторная работа, тест.
Оборудование и реактивы. Химические стаканы, пробирки, индикаторы; растворы хлорида и карбоната натрия, хлорида цинка, сульфата магния, оксиды кальция и фосфора(V).
В курсе химии за 8-й класс (учебно-методический комплект О.С.Габриеляна) представлены некоторые химические свойства этого соединения при изучении темы «Типы химических реакций на примере свойств воды». На данном уроке предстоит не только повторить, но и расширить представления учащихся о химических свойствах воды.
Учитель. В молекуле воды и водород, и кислород находятся в устойчивых степенях окисления, соответственно +1 и –2. Поэтому вода не обладает ярко выраженными окислительно-восстановительными свойствами. Они проявляются при взаимодействии воды только с очень активными восстановителями или окислителями.
В роли окислителя вода выступает с такими сильными восстановителями, как щелочные и щелочно-земельные металлы. Взаимодействие протекает при обычной температуре:
Учащиеся комментируют записанные схемы, указывая изменение степеней окисления, определяют окислители и восстановители, процессы окисления и восстановления.
Ученик. Реакция с натрием протекает бурно, поэтому не случайно во всех инструкциях по технике безопасности особо указывается, что при возникновении пожара на складе с натрием нельзя применять воду.
Ученики поясняют, что выделяющийся водород при определенных условиях загорается и реагирует с кислородом воздуха, что может привести к взрыву.
При нагревании протекает взаимодействие водяного пара и с менее активными металлами:
Последняя реакция (в присутствии атмосферного кислорода) является причиной коррозии металла, перед которой не устоять трубопроводам, мостам и другим металлическим конструкциям. Химики-технологи разработали достаточно эффективные способы замедления коррозии, но до полной победы над ней еще далеко. Вездесущая влага рано или поздно проникает через защитные покрытия и разрушает сплавы железа, принося многомиллионные убытки.
Кроме того, вода взаимодействует с гидридами щелочных и щелочно-земельных металлов, являющимися очень сильными восстановителями:
Данной реакцией очень удобно пользоваться в полевых условиях, если возникает необходимость в получении водорода, например при заправке гидрометеорологических шаров-зондов.
Вода выступает в роли восстановителя с сильными окислителями, например со фтором:
Эта реакция, проведенная в изолированных условиях, из-за ядовитости галогена, очень удивила ученых. В атмосфере фтора вода сгорала голубоватым пламенем.
Ничего нет вечного и в химии – при температуре выше 1000 °С водяной пар разлагается на водород и кислород, т.е. происходит внутримолекулярный окислительно-восстановительный процесс:
В природных условиях разложение воды по данной схеме ничтожно мало, столь высокие температуры создаются только при грозовых разрядах.
Многие научные коллективы пытаются найти практическое применение данной реакции и решить ряд энергетических и экологических проблем. Если в будущем появится удачное техническое решение, то автомобилисты вместо бензина начнут заливать в бак простую воду, она будет разлагаться на составляющие компоненты и соединяться вновь. Как известно, взаимодействие водорода и кислорода сопровождается выделением энергии, ее с лихвой хватит на движение автомобиля. В крупных городах население наконец-то получит возможность дышать свежим воздухом, ведь из выхлопной трубы будет выделяться только водяной пар. В нашем ХХI в. это уже не фантастика, опытные образцы подобных двигателей созданы, но они достаточно громоздки и пока намного дороже автомобилей с бензиновым двигателем.
Учитель. В самих названиях «кислота» и «основание» уже заложен намек на агрессивность соединений.
Не зря гласит пословица: «в тихом омуте черти водятся». Ей можно дать и химическое толкование – в обычной воде присутствуют одновременно и кислота, и основание. Это происходит в ходе своеобразной борьбы молекул воды друг с другом. Одна из шустрых молекул «умудряется» вырвать у соседки протон и присвоить его себе. При этом «хулиганка» превращается в ион гидроксония, т.е. кислоту, а «пострадавшая» молекула становится гидроксид-ионом, т.е. основанием. Такому явлению присвоено особое название – самоионизация. Данный процесс связан с тепловым движением частиц и взаимным притяжением диполей. Происходит ослабление и разрыв связей О–Н, в итоге протон присоединяется к атому кислорода соседней молекулы по донорно-акцепторному механизму:
В сущности, ион гидроксония является гидратированным ионом водорода Н + •Н2О. Упрощенно процесс ионизации воды обычно выражают следующим уравнением:
Таким образом, при ионизации одновременно образуются катионы водорода и гидроксид-
анионы, т.е. вода является слабым амфотерным электролитом. Легко заметить, что ионы образуются в равном соотношении и при диссоциации воды реакция среды нейтральна.
Степень ионизации воды незначительна. При комнатной температуре лишь одна из 10 8 молекул воды находится в диссоциированной форме, что подтверждается весьма низкой электропроводностью чистой воды. Вода – не просто слабый, а очень слабый электролит. Концентрации ионов Н + и ОН – в воде равны 10 –7 моль/л. Вода не проявляет явно выраженных кислотных или основных свойств. Однако этот «нейтралитет» достаточно условен. Если химическим методом связывать один из ионов, т.е. смещать равновесие реакции самоионизации, можно создавать в водных растворах кислую или шелочную среду. Далее мы узнаем, что такие процессы имеют немаловажное значение.
Вода оказывает сильное ионизирующее действие на растворяемые в ней электролиты. Под действием диполей воды полярные ковалентные связи в молекулах растворенных веществ превращаются в ионные. В частности, на этих свойствах воды основана работа многих аккумуляторов.
Учитель. Полярность и малые размеры молекулы воды определяют ее сильные гидратирующие свойства.
Гидратация – это присоединение воды к веществу.
Учащиеся записывают схемы реакций кислотных оксидов с водой:
CО2 + H2O 
Демонстрационный эксперимент «Взаимодействие оксидов с водой»
Учитель предлагает ученикам помочь лаборанту различить содержимое склянок, на которых испорчены этикетки. Предположительно, в них содержались оксиды кальция и фосфора.
Двое учащихся выполняют демонстрационный эксперимент, добавляя в стаканчики с небольшой порцией белых порошков (0,5 г) воду. Остается только проверить кислотность среды и записать на доске соответствующие уравнения:
Учитель. Многие виды гидратации имеют практическое значение. С их помощью в промышленности получают азотную, серную кислоты. В строительном деле, например, не обойтись без оксида кальция (негашеной извести). При добавлении воды образуется соответствующий гидроксид – гашеная известь, которая применяется в смесях для побелки, строительных растворах для кладки кирпичных стен.
Оксид фосфора(V) очень активно связывает воду и часто необходим для полной осушки некоторых органических растворителей. Данному процессу присвоен особый термин – абсолютирование. Для некоторых синтезов ученые используют абсолютно сухие вещества, нередко химики проводят реакции при полном отсутствии влаги в реакционной среде и даже вынуждены осушать воздух или какой-либо инертный газ оксидом фосфора(V) или концентрированной серной кислотой.
Учитель. Гидролизом называется процесс разложения веществ в результате обменного взаимодействия между молекулами вещества и молекулами воды.
По своей сути гидролиз – это «насильственное» связывание одного из ионов, образующихся при диссоциации воды, которое приводит к изменению кислотности растворов.
Различают несколько типов гидролиза.
1) Гидролиз по аниону характерен для соли, образованной сильным основанием и слабой кислотой:
Без этой полезной реакции сложно представить стирку белья в жесткой воде. Сходно гидролизуется и питьевая сода – гидрокарбонат натрия. Именно за счет щелочной среды «работают» содовые лечебные растворы. Они используются для полоскания полости рта в случае воспалительных процессов. В экстренных случаях раствор питьевой соды применяется при изжоге, вызванной повышенной кислотностью желудочного сока.
Труднорастворимые соли тоже подвергаются гидролизу, но он идет очень медленно. Так, при внесении в кислые почвы извести – карбоната кальция, постепенно идет гидролиз, выделяющиеся гидроксид-ионы участвуют в устранении кислотности почвы. В конечном счете, плодородие почвы восстанавливается. Это имеет большое значение для растениеводства, т.к. многие сельскохозяйственные культуры плохо развиваются на кислых почвах.
Нерациональное вмешательство в природу нередко приводит к трагическим последствиям. Так, в районах, прилегающих к озеру Баскунчак, очень велика кислотность почв. Вспашка таких целинных земель нередко сопровождается пыльными бурями, которые рассеивают по окрестностям много солей, подвергающихся гидролизу.
2) Гидролиз по катиону протекает с солями, образованными слабым основанием и сильной кислотой:
3) Гидролиз по катиону и аниону характерен для солей, образованных слабым основанием и слабой кислотой:
Карбонаты и ацетаты аммония используются в производстве кондитерских изделий как разрыхлители, их добавляют в тесто для придания воздушности выпечке. Под действием высокой температуры гидролиз усиливается, газообразные продукты (углекислый газ и аммиак) улетучиваются и придают дополнительную рыхлость кондитерскому изделию. Любителям домашней выпечки полезно читать информацию на пакетиках с разрыхлителями. Так, обозначение Е-503 свидетельствует о содержании в них карбоната аммония.
4) Необратимый (полный) гидролиз:
Al2S3 + 6HOН = 2Al(OH)3 

В этом случае ионы водорода связываются в летучую кислоту, а гидроксид-анионы – в малодиссоциирующее соединение, т.е. сульфид алюминия в растворах практически не существует. В таблице растворимости такие соли отмечены знаком «минус».
Для закрепления материала проводится эксперимент.
Лабораторная работа «Распознавание солей»
Учитель предлагает распознать вещества. В пробирки налиты растворы хлорида и карбоната натрия, хлорида цинка, сульфата магния. Последние растворы выдают себя характерной окраской при добавлении индикатора.
Учитель предлагает пояснить причину использования соды при стирке белья и записать в тетрадях схемы гидролиза карбоната натрия, сульфата магния, хлорида цинка.
Учитель. Реакции гидролиза сложных соединений лежат и в основе обмена веществ в организме человека и животных. Например, гидролиз белков представляет собой сложный многостадийный процесс, конечным продуктом которого являются аминокислоты – строительный материал всех тканей организма. Гидролиз сахарозы, которую мы добавляем в чай или кофе, проходит до глюкозы – ценного питательного и энергетического вещества. Аналогично, до глюкозы, протекает и многоступенчатый гидролиз крахмала, входящего в состав многих продуктов питания (изделий из муки, риса, картофеля). Реакции гидролиза в организме протекают под действием биологических катализаторов – ферментов. Без воды невозможно представить обменные процессы в живом организме. Не случайно в медицинских вузах очень большое внимание уделяется изучению химии – органической и биологической.
После завершения лекции ученикам предлагается домашняя работа по выполнению тестов, позволяющих проверить знания по химическим свойствам воды.
Вопросы для собеседованияпо теме «Химические свойства воды»
1. Напишите уравнения химических реакций, отражающие окислительные свойства воды.
2. Приведите примеры химических реакций, в которых вода проявляет восстановительные свойства.
3. Допишите уравнения химических реакций:
4. Почему вода является амфотерным соединением?
5. Приведите уравнения химических реакций гидролиза в молекулярной и ионной формах для солей, которые гидролизуются по: а) катиону; б) аниону; в) катиону и аниону.
6. Для каких веществ гидролиз протекает необратимо? Приведите примеры такого гидролиза для солей и других бинарных соединений.
7. Известные пословицы гласят: «Вода и камень точит», «Вода разбивает камень не силой, а частым падением». Можно ли пояснить их с позиций физических и химических процессов?
8. Какое из удобрений следует применить агроному для нейтрализации кислотности почв: а) кальциевую селитру – Са(NО3)2; б) известь – СаСО3; в) калийную селитру – KNО3? Ответ поясните.
Тест «Химические свойства воды»
1. При комнатной температуре с водой реагируют оба металла, указанные в паре:
а) барий и медь; б) кальций и литий;
в) алюминий и ртуть; г) серебро и натрий.
2. К реакции замещения относится взаимодействие воды:
а) с гидридом калия;
б) с оксидом серы(VI);
в) с натрием металлическим;
г) с оксидом кальция.
3. Обменное взаимодействие веществ с водой, приводящее к их разложению, называют:
а) гидрированием; б) гидрогенизацией;
в) гидролизом; г) гидратацией.
4. Вода не образуется в результате химической реакции между:
а) соляной кислотой и гидроксидом калия;
б) оксидом кальция и азотной кислотой;
в) гидроксидом натрия и оксидом углерода(IV);
г) нитратом серебра и соляной кислотой.
5. Какие два оксида при взаимодействии с водой образуют соответствующие им кислоты?
6. Укажите оксид, образующий при растворении в воде две кислоты:
7. При обычной температуре в химическую реакцию с водой не вступает:
а) оксид серы(IV); б) хлорид аммония;
в) оксид кальция; г) хлорид натрия.
8. Вода – это не только оксид водорода, но и оксид:
а) основный; б) амфотерный;
в) несолеобразующий; г) кислотный.
9. Масса воды (в г), которая образуется при нейтрализации 2 моль гидроксида натрия соляной кислотой, равна:
а) 18; б) 54; в) 9; г) 36.
10. С какой парой веществ взаимодействует вода: