что вреднее ибупрофен или диклофенак
Что безопаснее ибупрофен или диклофенак?
Часто при выборе препарата от боли или для устранения воспаления люди отдают предпочтения группе нестероидных противовоспалительных средств (НПВС), а также задаются распространенным характерным вопросом: что безопаснее ибупрофен или диклофенак?
И ибупрофен, и диклофенак относятся к одной и той же группе, а их механизм действия связан с уменьшением выработки простагландинов, которые участвуют в болевых и воспалительных реакциях. Но образование данных гормоноподобных веществ происходит благодаря группе ферментов циклооксигеназы (ЦОГ), которые синтезируют простагландины из арахидоновой кислоты путем биохимической реакции. Циклооксигеназа содержится в различных тканях и имеется два ее вида: ЦОГ-1 и ЦОГ-2. Оба препарата неселективно (неизбирательно) ингибируют два вида изоферментов ЦОГ.
Так почему же все врачи и провизоры как один твердят о том, что ибупрофен безопаснее, нежели диклофенак?
Все потому, что связано это с несколькими факторами, такими как различная фармакокинетика (отличаются процессы, связанные с лекарством при его попадании внутрь организма), с производным происхождением, так как диклофенак — производное фенилуксусной кислоты, а ибупрофен — производное пропионовой кислоты, что также оказывает разную силу и интенсивность воздействия на организм.
Диклофенак является более сильным препаратом по сравнению с ибупрофеном, его чаще применяют при ревматических болезнях. Чем сильнее средство, тем выше вероятность возникновения побочных эффектов. Его не следует применять детям до 18 лет.
Ибупрофен широко используются в педиатрической практике в детских лекарственных формах в виде сиропа и свечей Нурофена для устранения лихорадки.
Исходя из вышеуказанной информации о сравнении двух лекарственных средств, следует сделать вывод, что для снятия незначительной боли и снижения температуры хорошо подойдет ибупрофен, а для различных сильных болей (суставной, зубной, менструальной и т.д.), эффективнее диклофенак.
Источники
Опишите симптомы или нужный препарат — мы поможем подобрать его дозировку или аналог, оформим заказ с доставкой домой или просто проконсультируем. Мы — это 28 провизоров и 0 ботов.
Напишите нам «Морковка» и мы начислим вам 50 грн бонусов. Так мы всегда будем с вами на связи и сможем пообщаться в любой момент.
Опишите симптомы или нужный препарат — мы поможем подобрать его дозировку или аналог, оформим заказ с доставкой домой или просто проконсультируем. Мы — это 28 провизоров и 0 ботов.
Напишите нам «Морковка» и мы начислим вам 50 грн бонусов. Так мы всегда будем с вами на связи и сможем пообщаться в любой момент.
Сравнительная эффективность нестероидных противовоспалительных препаратов при болях в спине
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В настоящее время боли в спине (БС) широко распространены, а в развитых странах, по данным экспертов ВОЗ, сравнимы с неинфекционной эпидемией, что в большинстве случаев связано с возрастающими нагрузками на человека [4]. Высокая инвалидизация лиц трудоспособного возраста вследствие поражений опорно-двигательного аппарата возводит проблему лечения БС в ранг актуальной. Популяционные исследования выявили ассоциацию болей в нижней части спины (БНС) с такими факторами, как пол и возраст, осанка, мышечная сила, подвижность позвоночника. В недавно проведенном в Швеции популяционном исследовании спинальных болей среди лиц в возрасте 35-45 лет установлено, что частота возникновения болей за последний год составила 66,3%, причем данный показатель среди женщин был незначительно выше, чем среди мужчин. У 25% респондентов возникли существенные проблемы с трудоспособностью, степенью нарушения функционального статуса. В Великобритании вследствие болей в спине в 1992 г. было потеряно 90 миллионов рабочих дней, что уступало только заболеваниям органов дыхания и кровообращения. При этом 75% больных составили пациенты от 30 до 59 лет, то есть в период максимальной трудоспособности.
Все случаи болей в спине делятся на первичные и вторичные.
Вторичный синдром БС может быть связан с врожденными аномалиями, травматическими поражениями позвоночника, опухолевыми и инфекционными процессами, остеопорозом, заболеваниями внутренних органов.
БС чаще всего развивается в возрасте от 20 до 50 лет (пик заболеваемости в возрасте от 35 до 45 лет). Именно в этой возрастной группе обычно диагностируют первичный (механический) синдром БС, тогда как у больных моложе 20 лет и старше 50 лет преобладает вторичный синдром БС (табл. 1).
Диагностика БС требует участия врачей разных специальностей: терапевта, ревматолога, невропатолога, ортопеда и хирурга, задачей которых, в частности, является исключение вторичного характера болей в нижней части спины.
Провоцирующими факторами острого течения БС могут быть травма, подъем непосильного груза, неподготовленные движения, длительное пребывание в нефизиологической позе, переохлаждения. Хроническая боль может возникать как после регресса острой боли, так и независимо от нее.
Лечение проводится с учетом формы заболевания и варианта его течения с использованием консервативного и хирургического подходов.
В настоящее время показания к хирургическому лечению сужены, поскольку накопились факты о том, что даже при очень хорошей методике хирургической декомпрессии и стабилизации заболевание склонно рецидивировать.
При обострении клинических проявлений БС ранее рекомендовался отдых в течение нескольких недель. Однако во всех исследованиях последних лет подчеркивается, что не постельный режим, а ранняя активизация больных должна быть главным компонентом программы лечения, что способствует улучшению питания межпозвонкового диска, в связи с чем постельный режим при остром течении ограничивается несколькими днями.
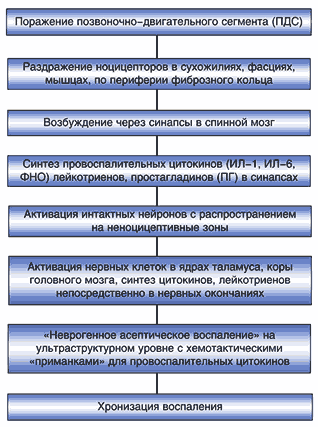
Дегенеративный процесс в межпозвонковом диске активирует ноцицепторы по периферии фиброзного кольца, в сухожилиях, фасциях, мышцах с последующей передачей импульсов в спинной мозг. При этом запускаются иммунные и биохимические реакции, завершающиеся формированием асептического нейрогенного воспаления. В связи с этим целесообразность назначения НПВП обоснована (схема 1) [3].
Схема 1. Механизмы асептического неврогенного воспаления при спондилоартрозе (Borenstein D., 2000).
В настоящее время появилась возможность применения такого НПВП, как кетопрофен (Кетонал) при остеоартрозе, а также при лечении болей в спине. Кетопрофен является производным пропионовой кислоты. Особенностью его противовоспалительного действия является не только ингибирование синтеза простагландинов на уровне циклооксигеназы; он также ингибирует липооксигеназу, обладает антибрадикининовой активностью, стабилизирует лизосомальные мембраны. При приеме внутрь препарат быстро и максимально полно абсорбируется из желудочно-кишечного тракта. Максимальная концентрация в крови достигается через 1-2 часа. Кетонал хорошо проникает в синовиальную жидкость и соединительную ткань. Значимые уровни концентраций достигаются уже через 15 минут после однократного внутримышечного введения 100 мг кетопрофена. Важным преимуществом препарата является то, что он представлен различными лекарственными формами: капсулами, таблетками форте и ретард, раствором для внутримышечных инъекций, кремом и суппозиториями.
Кетонал обладает «сбалансированной» активностью в отношении ингибиции ЦОГ-1 и ЦОГ-2, что позволяет оптимально сочетать высокую эффективность с хорошей переносимостью, сравнимой, по данным ряда авторов, с переносимостью селективных НПВП [3,5]. Исследователи связывают мощный болеутоляющий эффект Кетонала с его доказанным центральным воздействием, которое реализуется на уровне задних рогов спинного мозга, а также за счет непосредственного влияния на таламические центры болевой чувствительности, что, по-видимому, связано с угнетением синтеза простагландинов в ЦНС [4,5].
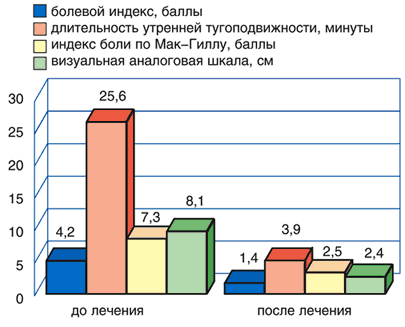
Рис. 1. Динамика клинических показателей у пациентов с болями в спине до и после лечения Кетоналом форте
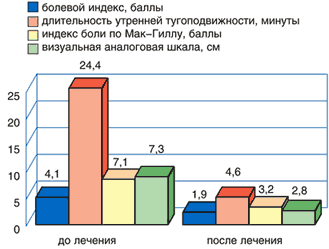
Рис. 2. Динамика клинических показателей у пациентов с болями в спине до и после лечения диклофенаком
Оценки эффективности лечения больным и врачом практически не отличались друг от друга и свидетельствовали о выраженной клинической эффективности препаратов. Высокая эффективность отмечена у 93,3% пациентов, принимавших Кетонал форте, у 73,3% пациентов, принимавших диклофенак.
Переносимость препарата «хорошая» или «очень хорошая» была отмечена у 80% больных, принимавших Кетонал, и у 64% принимавших диклофенак. Основными побочными эффектами при приеме как диклофенака, так и Кетонала были изжога, дискомфорт в эпигастральной области. Прекращение лечения потребовалось лишь в 1 случае, когда у пациента развилась крапивница на фоне приема диклофенака, которая была расценена, как побочный эффект средней степени тяжести.
Таким образом, в настоящее время лечение болей в спине оптимизировано использованием препаратов группы НПВП, в частности, Кетонала, в силу его высокой эффективности, проявляющейся отчетливо выраженной положительной динамикой с регрессом болевых проявлений у пациентов с БС.
1. Клинические рекомендации для практических врачей, основанные на доказательной медицине. Изд. дом «ГЭОТАР-МЕД», 2001, с. 606-611.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (перспективы применения в медицине). М., 2000, 262.
3. Насонов Е.Л., Чичасова Н.В., Шмидт Е.И. Перспективы применения неселективных нестероидных противовоспалительных препаратов (на примере кетопрофена) и селективных ингибиторов ЦОГ-2 в клинической практике. Русский медицинский журнал, том 10, №22, 2002, с 1014-1017.
4. Ветшев П.С., Ветшева М.С. Принципы аналгезии в раннем послеоперационном периоде. Хирургия, 2002, №12, с. 49-52.
5. Чичасова Н.В., Насонов Е.Л., Имаметдинова Г.Р. Применение кетопрофена (кетонал) в медицинской практике. Фарматека, 2003, №5, с. 30-32.
6. Borenstein D. «Эпидемиология, этиология, диагностическая оценка и лечение поясничной боли». Междун. Медиц. Журнал, 2000, №35, с. 36-42.
7. WHO. Department of noncomunicable disease menagement. Low back pain iniciative. Geneve.1999.
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
Клиническая оценка нестероидных противовоспалительных препаратов в конце ХХ века
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Институт ревматологии РАМН, Москва
П рименение народных средств, обладающих жаропонижающим и обезболивающим эффектом, насчитывает не одно тысячелетие. Примером тому может служить отвар коры ивы, о котором писал еще великий Гиппократ. Отвар, как было установлено много веков спустя, содержал салициловую кислоту. Сам по себе этот факт показывает устойчивую необходимость для человека находить такие средства лечения, которые позволяют достаточно быстро смягчить или полностью устранить симптомы, существенно ухудшающие, как теперь принято говорить, качество жизни.
Со времени синтеза ацетилсалициловой кислоты прошло более 100 лет, и если в первую половину этого периода ее использовали, как жаропонижающее и обезболивающее средство, применяемое в больших дозах, то во вторую – уже в низких дозах для профилактики сосудистых заболеваний (инфаркта миокарда и инсульта) в связи с ее уникальной способностью ингибирования избыточного образования тромбоксана, определяющего склонность к развитию тромбозов.
Ацетилсалициловая кислота, синтезированная в 1899 году, была, в сущности, первым лекарственным средством, которое обладало не только жаропонижающим и обезболивающим, но и противовоспалительным действием. Однако настоящим прорывом в эффективной противовоспалительной терапии стала вторая половина ХХ века, когда были получены данные исключительной важности для понимания самих механизмов развития воспаления, включая иммуноопосредованное хроническое воспаление при многих ревматических заболеваниях, и открыты активные противовоспалительные препараты, в первую очередь, кортикостероиды и близкие по активности различные классы слабых кислот, названные нестероидными противовоспалительными (НПВП).
Вслед за фенилбутазоном и индометацином, введенными в клиническую практику 50–60-е годы, последовало лавинообразное открытие различных химических групп НПВП – производных арилпропионовой (ибупрофен, 1969), арилуксусной (диклофенак натрия, 1971) и эноликовой (пироксикам, 1980) кислот – не только обладавших столь же высокой эффективностью, но и лучшей переносимостью. Модификации в перечисленных классах кислот привели к синтезу и других, достаточно эффективных лекарств, в частности, напроксена, флурбипрофина, кетопрофена – в пропионовой группе, мелоксикама, лорноксикама – среди препаратов эноликовой кислоты.
Механизмы действия НПВП
До 70-х годов основные механизмы противовоспалительного действия НПВП связывались с такими известными к тому времени провоспалительными факторами, как снижение проницаемости сосудистой стенки, стабилизация лизосомных мембран клеток, участвующих в воспалении, подавление активности простагландинов, кининов, других биологически активных компонентов.
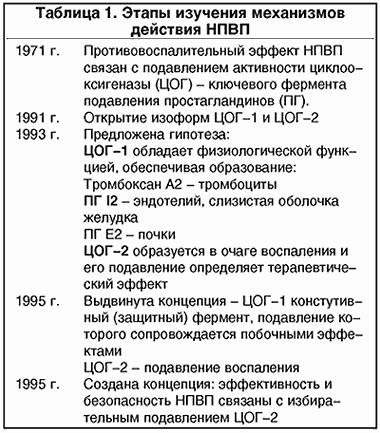
Лишь в начале 70-х J.Vane (1971) показал, что принципиальный механизм противовоспалительного действия ацетилсалициловой кислоты и индометацина обусловлен подавлением активности циклооксигеназы (ЦОГ) – ключевого фермента синтеза простагландинов. В последующем доказано существование двух изоформ – ЦОГ-1 и ЦОГ-2, обладающих соответственно физиологическим цитопротективным действием и индуцируемым провоспалительным. Изофермент ЦОГ-1 постоянно присутствует во многих тканях, синтезирующих простагландины, регулирует нормальную активность тех или иных клеток, обеспечивая тем самым цитопротекцию слизистой желудочно-кишечного тракта (ЖКТ), сосудистый гемостаз и функционирование почек. Тогда как изофермент ЦОГ-2 экспрессируется только в очаге воспаления, определяя избыточное образование простагландинов провоспалительной активности. Эти данные позволили создать концепцию: эффективность и безопасность НПВП связаны с избирательным подавлением ЦОГ-2 (табл. 1). Следовательно, НПВП, сильнее подавляющие активность ЦОГ-1 (ацетилсалициловая кислота, например), чаще вызывают поражение ЖКТ, чем препараты, более подавляющие ЦОГ-2 или обладающие действием эквипотентным в отношении обоих ЦОГ (диклофенак натрия), либо время-зависимым эффектом в отношении ЦОГ-1 (ибупрофен).
Особенно важно, что изучение механизмов действия НПВП послужило мощным толчком к созданию новых препаратов, в значительной мере лишенных побочных эффектов. Среди них пока наиболее изучены преимущественно селективные ингибиторы ЦОГ-2 (мелоксикам, нимесулид), накапливаются данные и о специфических ингибиторах ЦОГ-2 (целекоксиб и рофекоксиб).
Клиническая значимость предложенной концепции позволила пересмотреть подход к выбору НПВП. Если еще в 80-е годы считалось, что наличие десяти НПВП препаратов дает врачу возможность индивидуально подобрать наиболее эффективный и хорошо переносимый препарат, то новые знания механизма действия помогают сегодня более обосновано оценивать все “за” и “против” в отношении того или иного противовоспалительного средства. Безусловно, этому будет способствовать получающая все большее распространение патогенетическая классификация НПВП (табл.2), основанная на селективности или специфичности действия в отношении ЦОГ-1 и ЦОГ-2, либо, что характерно для большинства традиционных НПВП, на подавлении в той или иной степени обоих изоферментов ЦОГ.
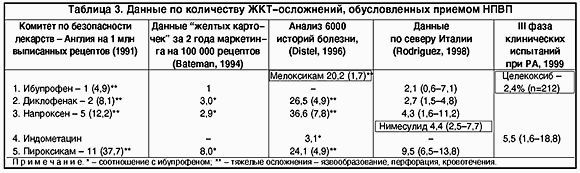
Анализируя приведенную классификацию, необходимо подчеркнуть особо высокую селективность ацетилсалициловой кислоты в отношении ЦОГ-1, проявляющуюся стойким подавлением активности последней даже при приеме 50 мг препарата, на чем и основано его профилактическое дезагрегантное действие. Что касается второй группы, к которой относится большинство ныне применяемых НПВП, то следует отметить следующее. Во-первых, с этими лекарствами связаны многие годы клинического применения и объективных оценок эффективности и переносимости, позволяющих избирательно их назначать. Несмотря на высокую ЖКТ-токсичность, индометацин по-прежнему сохраняет свое значение при лечении анкилозирующего спондилоартрита и дегенеративных заболеваний позвоночника при условии тщательного исключения факторов риска развития этого осложнения (язвенный анамнез у больного или членов семьи, полипрогмазия, курение, злоупотребление алкоголем, кофе, несоблюдение диеты и др.). Напроксен обладает высокой анальгетической активностью в средних дозах и может быть препаратом выбора при ревматических заболеваниях, а также у девушек и молодых женщин с синдромом дисменорреи, для которой характерны высокая активность ЦОГ-2 в репродуктивных органах и системное проявление гиперпродукции простагландинов. Кетопрофен обладает очень высокой анальгетической активностью, сравниваемой с опиоидной, а потому, как и прежде, находит оправданное применение в хирургической практике при подготовке к операции, в послеоперационном периоде, а также в случаях острейших болей в опорно-двигательном аппарате. Что касается ибупрофена и диклофенака натрия, то следует подчеркнуть, что по последним данным (1996, 1998 гг.) они являются эталоном безопасности (табл. 3). При этом сравнительные данные авторов в разные годы показывают близкие показатели по отношению к ибупрофену и диклофенаку, как и к пироксикаму. Однако наибольшее внимание должны привлечь к себе статистические материалы по тяжелым жизнеугрожающим ЖКТ-осложнениям, таким как язвообразование, перфорация или кровотечения. Сравнительные материалы показывают преимущество мелоксикама по сравнению с диклофенаком.
По данным Mc Kenna (2000 г.), гастропатия особенно коварна, так как 50% язвенных поражений бессимптомны и нет корреляций между эндоскопическими находками (эрозиями, например) и диспепсическими явлениями. Поэтому не удивительно, что ослабленным и пожилым людям более всего угрожает развитие тяжелых ЖКТ-осложнений. Популяционные данные по Англии показывают, что 1-2% регулярно принимающих НПВП поступают ежегодно в стационары с ЖКТ-кровотечениями и перфорациями и 10% из них умирают (ежегодно регистрируется до 3 тыс. смертей). Мировой опыт свидетельствует, что развитие вызванных НПВП желудочных кровотечений представляет наибольшую угрозу для больных ревматоидными артритами (РА), так как они принимают большие дозы НПВП, нередко в сочетании с глюкокортикостероидами. Но главное по причине системного характера болей в суставах развившееся осложнение крайне сложно диагностировать.
С другой стороны, нередко в клинической практике неправильно переоценивается местное раздражающее действие НПВП на слизистую оболочку желудка и двенадцатиперстной кишки (как слабых кислот). Больному рекомендуют изменить способ введения препарата – в виде свечи или инъекции, что, к сожалению, не снимает угрозы тяжелого ЖКТ-осложнения, поскольку все эти препараты оказывают системное подавление ЦОГ-1, а не местное – в слизистой оболочке желудка и других отделов.
Эффективность практически всех НПВП доказана на большом клиническом материале, при этом именно диклофенак натрия признан “золотым стандартом” эффективности, с которым сравниваются и новые лекарственные средства, такие как мелоксикам и целекоксиб.
Диклофенак натрия в дозе 100–150 мг в 2–3 приема, безусловно, обладает высокой анальгетической и противовоспалительной активностью при РА, спондилоартритах (анкилозирующем прондилоартрите и реактивных нарушениях), дегенеративных заболеваниях суставов и позвоночника, поражениях внесуставных мягких тканей, спортивных травмах и др. Безусловное преимущество диклофенака натрия – многообразие фармакологических форм быстрого действия и ретардных таблеток, инъекций, мазей, гелей. В последнее время все чаще при острых болях используется рапидная форма в виде калиевой соли диклофенака. Как и 30 лет назад, диклофенак остается одним из наиболее востребованных НПВП и не только в ревматологии.
Многоцентровые международные исследования эффективности мелоксикама (15 и 22,5 мг/ в день ) в сравнении с пироксикамом (20 мг/день) у больных анкилозирующим спондилоартритом выявили более высокую эффективность мелоксикама. И хотя лечение прекратили 19 и 18% больных, соответственно, тяжелые ЖКТ-осложнения развивались редко – у 4 больных в группе пироксикама и у 1 – мелоксикама. Таким образом, многоцентровое годичное сравнительное исследование при анкилозирующем спондилоартрите показало, что мелоксикам в дозе 15 мг – эффективное терапевтическое средство при этой болезни.
Получены достаточно обнадеживающие результаты эффективности и переносимости целекоксиба. Так, длительное (6–12 мес) двойное слепое плацебо-контролируемое и сравнительно с другими НПВП исследование более чем у 11 тыс. больных с ОА и РА показало, что целекоксиб в дозе 400 мг был сходен по эффективности с напроксеном (500 мг 2 раза в сутки) и диклофенаком (75 мг 2 раза в сутки). Что касается побочных эффектов ЖКТ, то они встречались с такой же частотой, как в группах плацебо. Обращает на себя внимание то, что сравнительное исследование целекоксиба с плацебо и неселективными НПВП у больных старше 65 лет выявило лучшую переносимость целекоксиба – боли в животе отмечены у 4% больных, против 9,2% принимавших НПВП. Чрезвычайно важно подчеркнуть, что лечение целекоксибом не приводило к обострению аспириновой бронхиальной астмы и скрытой сердечной недостаточности. Однако при наличии факторов риска сосудистых нарушений целесообразно назначать больным дополнительно небольшие дозы ацетилсалициловой кислоты.
Особенности применения у пожилых
Клиническое обсуждение особенностей лечения НПВП невозможно без пристального внимания к назначению этих лекарственных средств при ОА у лиц пожилого и старческого возраста. Это связано с достаточно большой прослойкой в популяции людей старших возрастных групп, сложностью лечения этой категории больных из-за наличия у них и других хронических заболеваний, требующих приема различных препаратов. К сожалению, до сих пор не решен вопрос, с чего нужно начинать лечение ОА – с простых анальгетиков или сразу с НПВП? Выше уже указывалось, что в пользу раннего назначения НПВП при манифестном ОА свидетельствует нередкое развитие синовита и/или воспалительного процесса в самом хряще, а также возможность выбора эффективного, хорошо переносимого и совместимого с другими лекарствами НПВП, включая современные селективные и специфические ингибиторы ЦОГ-2 (табл. 4). Но главный аргумент, пожалуй, состоит в том, что прием НПВП позволяет отодвинуть на многие годы операцию эндопротезирования.
В заключение необходимо подчеркнуть, что к концу ХХ века медицинская наука и клиническая практика добились ошеломляющих результатов в познании механизмов развития воспаления и подавления его активности, в понимании фармакологически обоснованных побочных эффектов со стороны ЖКТ и необходимости постоянного мониторинга (в том числе проведения повторных эндоскопий) для своевременного распознавания жизнеугрожающих осложнений. В то же время клинический опыт показал необходимость сотрудничества с больным, повышения ответственности больного во время лечения и устранения тех факторов риска, которые способствуют более частому развитию побочных эффектов. С этой точки зрения особенно важно обоюдное осознание ответственности врача и больного при приеме высокоэффективных, но небезопасных лекарств, каковыми являются НПВП.
В заключение необходимо подчеркнуть, что к концу ХХ века медицинская наука и клиническая практика добились ошеломляющих результатов в познании механизмов развития воспаления и подавления его активности, в понимании фармакологически обоснованных побочных эффектов со стороны ЖКТ и необходимости постоянного мониторинга (в том числе проведения повторных эндоскопий) для своевременного распознавания жизнеугрожающих осложнений. В то же время клинический опыт показал необходимость сотрудничества с больным, повышения ответственности больного во время лечения и устранения тех факторов риска, которые способствуют более частому развитию побочных эффектов. С этой точки зрения особенно важно обоюдное осознание ответственности врача и больного при приеме высокоэффективных, но небезопасных лекарств, каковыми являются НПВП.