что включает в себя понятие сплав
Сплав
Сплав — макроскопически однородный металлический материал, состоящий из смеси двух или большего числа химических элементов с преобладанием металлических компонентов.
Сплавы состоят из основы (одного или нескольких металлов), малых добавок специально вводимых в сплав легирующих и модифицирующих элементов, а также из не удаленных примесей (природных, технологических и случайных).
Сплавы являются одним из основных конструкционных материалов. Среди них наибольшее значение имеют сплавы на основе железа и алюминия. В технике применяется более 5 тыс. сплавов.
Содержание
Виды сплавов
По способу изготовления сплавов различают литые и порошковые сплавы. Литые сплавы получают кристаллизацией расплава смешанных компонентов. Порошковые — прессованием смеси порошков с последующим спеканием при высокой температуре. Компонентами порошкового сплава могут быть не только порошки простых веществ, но и порошки химических соединений. Например, основными компонентами твёрдых сплавов являются карбиды вольфрама или титана.
По способу получения заготовки (изделия) различают литейные (например, чугуны, силумины), деформируемые (например, стали) и порошковые сплавы.
В твердом агрегатном состоянии сплав может быть гомогенным (однородным, однофазным — состоит из кристаллитов одного типа) и гетерогенным (неоднородным, многофазным).Твёрдый раствор является основой сплава (матричная фаза). Фазовый состав гетерогенного сплава зависит от его химического состава. В сплаве могут присутствовать: твердые растворы внедрения, твердые растворы замещения, химических соединений(в том числе карбиды, нитриды, интерметаллиды …) и кристаллиты простых веществ.
Свойства сплавов
Свойства металлов и сплавов полностью определяются их структурой (кристаллической структурой фаз и микроструктурой). Макроскопические свойства сплавов определяются микроструктурой и всегда отличаются от свойств их фаз, которые зависят только от кристаллической структуры. Макроскопическая однородность многофазных (гетерогенных) сплавов достигается за счёт равномерного распределения фаз в металлической матрице. Сплавы проявляют металлические свойства, например: электропроводность и теплопроводность, отражательную способность (металлический блеск) и пластичность. Важнейшей характеристикой сплавов является свариваемость.
Сплавы, используемые в промышленности
Сплавы различают по назначению: конструкционные, инструментальные и специальные.
Конструкционные со специальными свойствами (например, искробезопасность, антифрикционные свойства):
Для заливки подшипников:
Для измерительной и электронагревательной аппаратуры:
Для изготовления режущих инструментов:
См. также
Литература
Ссылки
Полезное
Смотреть что такое «Сплав» в других словарях:
сплав — сплав, а … Русский орфографический словарь
сплав — СПЛАВ, а, муж. Однородная смесь, образовавшаяся вследствие затвердения расплава двух или нескольких отдельных веществ. Металлические сплавы (из двух или нескольких металлов или из металла и неметалла). Неметаллические сплавы (гранит, базальт,… … Толковый словарь Ожегова
сплав — см. соединение Словарь синонимов русского языка. Практический справочник. М.: Русский язык. З. Е. Александрова. 2011. сплав сущ. • лесосплав … Словарь синонимов
сплав — 1. СПЛАВ, а; м. 1. Вещество, полученное при плавлении из двух или нескольких плавких твёрдых тел (преимущественно металлов). Лёгкие сплавы. Сверхтвёрдый с. Мельхиор с. меди с никелем. 2. Соединение различных элементов, частей и т.п. чего л. Его… … Энциклопедический словарь
СПЛАВ — 1. СПЛАВ1, сплава, муж. Смесь из двух или нескольких плавких твердых тел, преим. металлов. 2. СПЛАВ2, сплава, мн. нет, муж. Действие по гл. сплавить2 в 1 знач. сплавлять2. Сплав леса по реке. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СПЛАВ — 1. СПЛАВ1, сплава, муж. Смесь из двух или нескольких плавких твердых тел, преим. металлов. 2. СПЛАВ2, сплава, мн. нет, муж. Действие по гл. сплавить2 в 1 знач. сплавлять2. Сплав леса по реке. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
СПЛАВ 1 — СПЛАВ 1, а, м. Однородная смесь, образовавшаяся вследствие затвердения расплава двух или нескольких отдельных веществ. Металлические сплавы (из двух или нескольких металлов или из металла и неметалла). Неметаллические сплавы (гранит, базальт,… … Толковый словарь Ожегова
СПЛАВ 2 — см. сплавить 2. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
сплав — 1 іменник чоловічого роду складна речовина сплав 2 іменник чоловічого роду сплавлення лісу … Орфографічний словник української мови
Сплав — I м. 1. Соединение двух или нескольких плавких тел. 2. перен. Соединение различных элементов, частей и т.п. чего либо. II м. действие по гл. сплавлять II, сплавить II Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
Сплав — I м. 1. Соединение двух или нескольких плавких тел. 2. перен. Соединение различных элементов, частей и т.п. чего либо. II м. действие по гл. сплавлять II, сплавить II Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
Понятие о сплавах
Сплав – это вещество, полученное сплавлением, спеканием, электролизом, возгонкой двух или более элементов. Сплав, приготовленный из металлов или имеющий металлическую основу и обладающий металлическими свойствами называется металлическим сплавом (МС). МС более сложное вещество, чем чистый металл, МС обладают более высокими прочностными и другими механическими свойствами по сравнению с чистыми металлами. Им часто придаются специфические свойства. Поэтому они получили более широкое применение.
Характер взаимодействия компонентов в сплавах зависит от их положения в таблице Менделеева, особенностей строения атомов, их электронных оболочек, типов и параметров решёток, соотношения температур плавления, их атомных диаметров, растворимости друг в друге и других факторов. МС может быть: а) механической смесью, б) химическим соединением, в) раствором элементов друг в друге с неограниченной или ограниченной растворимостью, а также их промежуточными смесями.
Механическая смесь двух и более компонентов возможна тогда, когда металлы (вещества, элементы) не растворимы в твёрдом состоянии и не вступают в химическую реакцию с образованием соединений. Рентгенограмма показывает наличие двух решёток компонентов А и Б, что соответствует чистым металлам. Механические свойства соответствуют и зависят от количества компонентов А и Б.
Химическое соединение (ХС). При образовании ХС достигается следующее:
— соотношение атомов элементов соответствует стехиометрической пропорции Аm × Вn ;
— образуется новая отличная от элементов кристаллическая решётка с упорядоченным расположением атомов;
— ХС характеризуется определёнными физическими свойствами (температура плавления, удельный вес, электро- и теплопроводность, мехсвойства, запах, вкус, ковкость, пластичность и т.д.).
Если ХС образуется металлами, то в углах решётки располагаются атомы (ионы), между ними электронный газ. К таким элементам относятся Cu2MnSn, CuAl2, CuAu, CuAg и т.п. Связи жёсткие, химические соединения образуются без учёта валентности.
При образовании химсоединения металла с неметаллом возникает ионная связь. Элементы удерживаются электронным притяжением (NaCl, KMnO4 и т.д.)
В жидком состоянии большинство металлических сплавов представляют однородные жидкие растворы. При переходе в твёрдое состояние однородность сохраняется, сохраняется и растворимость. Рентгеновский анализ обнаруживает только один тип решётки. В отличие от механических смесей твёрдый раствор является однофазным. В отличие от химического соединения твёрдый раствор существует не при строго определённом соотношении компонентов, а в интервале концентрации. Различают твёрдые растворы замещения и внедрения. Замещают металлы друг друга, заменяя в узлах решётки. Внедряются в металл обычно элементы с малым диаметром атома (C, H, N и др.). С образованием твёрдых растворов внедрения периоды решётки увеличиваются.
Замечено, что неограниченная растворимость наблюдается у элементов относительно близко расположенных друг от друга в периодической системе. Если элементы расположены друг от друга далеко и имеют различную физическую природу, то они чаще всего склонны к образованию химических соединений, а не твёрдых растворов.
Химические соединения могут также образовывать растворы замещения, растворять другие атомы. Например, борид железа (Fe4B2) способен растворять хром, углерод.
Электронные соединения могут образовывать металлы следующих групп: Cu, Ag, Au, Fe, Co, Ni, Pt, Pd, Be, Zn, Cd, Al, Sn, Si
Электронные соединения встречаются в важнейших сплавах: Cu-Zn; Cu-Sn; Fe-Al; Cu-Si; Al-Si; Cu-Al и т.д. Обычно в системе наблюдаются три фазы (β, γ, ε). Электронные соединения промежуточные между хим. соединениями и твёрдым раствором.
Диаграммы состояния представляют собой графическое изображение фаз и структур в зависимости от температуры, давления и концентрации элементов.
Фаза – это однородная часть системы, отделённая от других частей системы (фаз) поверхностью раздела, при переходе через которую изменяется состав, часто решётка, структура скачкообразно.
Компоненты – вещества, образующие систему.
Состояние одного компонента – прямая линия; диаграмма состояния 2-х компонентов системы – плоская фигура (на оси ординат откладывается t 0 С, на оси абсцисс – концентрация элементов); 3-х компонентная система – пространственная фигура с основанием в виде треугольника и т.д.
Линия начала кристаллизации называется точкой ликвидуса, конец кристаллизации – точка солидуса.
Имеются следующие диаграммы:
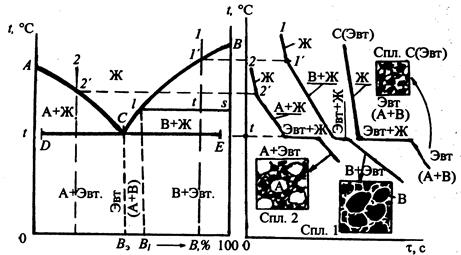
В доэвтектических сплавах содержится компонент А совместно с эвтектикой (АВ), в заэвтектических содержится компонент В с эвтектикой (АВ).
а – диаграмма состояния; б – схемы получающихся структур
Рисунок 22 – Диаграмма состояния I рода и схемы получающихся структур
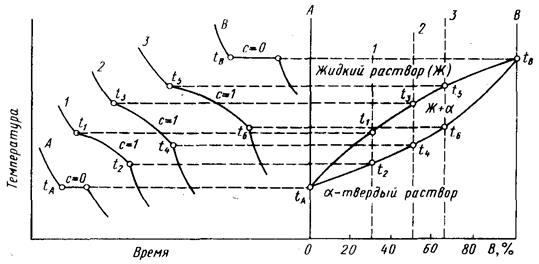
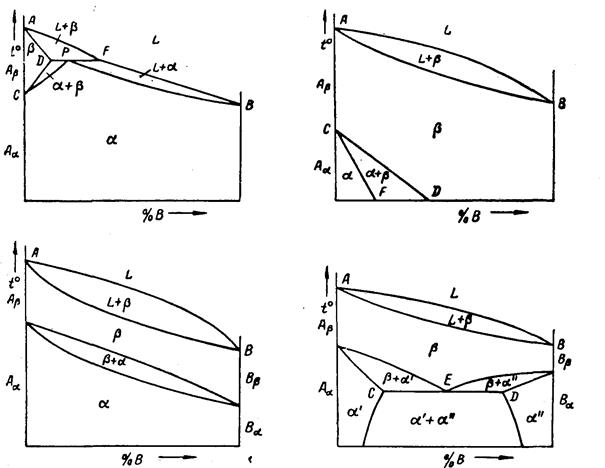
а – кривые охлаждения; б – диаграмма состояния
Рисунок 23 – Диаграмма состояния для случая неограниченной растворимости компонентов А и В в твёрдом и жидком состоянии
в) диаграмма состояния 3-го рода описывает сплавы с ограниченной растворимостью в твёрдом состоянии, не образующих химическое соединение. На рисунке 24 изображена диаграмма с эвтектикой, на рисунке 25 – с перитектикой. Перитектическая реакция ж+ 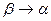
а – кривые охлаждения; б – диаграмма состояния
Рисунок 24– Кривые охлаждения и диаграмма состояния сплавов, образующих ограниченные твердые растворы и эвтектику
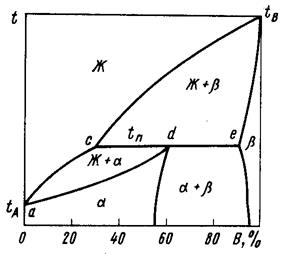
Рисунок 25 – Диаграмма состояния сплавов, образующих ограниченные твердые растворы и испытывающих перитектическое превращение
Ограниченная растворимость наиболее часто встречается в металлических сплавах. Линия а-с-в ликвидус, линия a-d-c-e-в – солидус. Выше “acв” расположена жидкость, между “асв” и “adceв” – жидкость и кристаллы 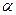

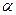

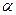
20 0 С) начинает распадаться с выделением дисперсных частиц избыточной фазы 
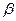
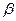
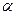
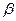
Сплавы, расположенные левее точки d однофазные и лучше обрабатываются давлением, хуже льются.
При кристаллизации часто наблюдается разность химсостава по сечению литой заготовки. Этот процесс называется ликвацией.
Разберём коротко диаграмму с перетектикой (рис.25). Точка d характеризует максимальную растворимость компонента B в A, а точка “e”- предельную растворимость A в B. Линия “CDE” – линия перетектического превращения. При эвтектическом превращении кристаллизуется сразу 2 фазы, при перетектическом превращении кристаллизуется одна фаза из ранее выпавшей твёрдой фазы и жидкости. Из жидкого раствора правее точки d из жидкой фазы в начале выделяется 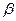
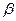
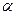
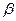
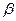
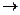
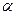
Неизрасходованная часть жидкости и кристаллы 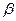
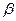
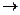
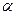
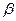
Кристаллизация сплавов по “c-d” происходит по формуле жс+ 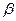
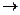
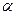
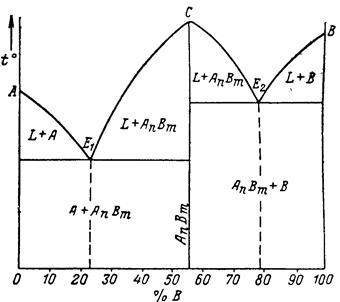
г) диаграмма состояния сплава, образующего устойчивое химическое соединение (рис. 26) Аm × Вn. Устойчивых соединений может быть 1,2,3…
Рисунок 26 – Диаграмма состояния IV рода
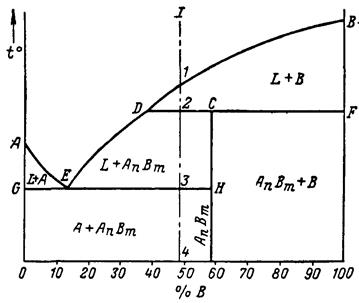
д) диаграмма состояния с неустойчивым химическим соединением представлена на рисунке 27. На линии d-c-t в равновесии находится три фазы: Жд+кристаллы компонента В и кристаллы химсоединения An Bm. Выше линии DCF происходит An Bm 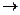
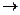
Рисунок 27 – Диаграмма состояния с неустойчивым химическим соединением
Рисунок 28 – Диаграммы состояния с полиморфными превращениями
Перечисленные выше диаграммы равновесные, т.е. выполнены при малых скоростях охлаждения. Изучив теоретическую кристаллизацию, можно рассматривать неравновесные условия, когда могут не происходить диффузионные процессы при различных переохлаждениях.
В реальных условиях первые кристаллы имеют большую концентрацию тугоплавкого компонента. Последующие кристаллы самые легкоплавкие. Это явление называется ликвацией. Она может быть уменьшена длительным диффузным отжигом или обработкой давлением.
Неравновесная кристаллизация происходит при большом переохлаждении. Чем больше переохлаждение, тем мельче будут вторичные кристаллы, тем напряжённей и неустойчивее система. Получается пересыщенный раствор одного компонента в другом – мартенсит, который прочен, твёрд. Этот процесс называется закалкой. Нагревая сплав после закалки, мы приводим систему в более устойчивое состояние, снижая прочность. Этот процесс называется отпуском или старением. С помощью термообработки можно изменять механические свойства сплавов.
2.2 Диаграмма железо – углерод
Железоуглеродистые сплавы (стали, чугуны) важнейшие, так как их производят 90-95% от общего производства всех металлов. Начало изучению диаграммы положено Д.К.Черновым, П.П.Амосовым. Было указано о существовании критических точек в стали, дано первое представление о диаграмме Fe-С. Зарубежные учёные Осмонд, Ле – Шателье, Аустенит, русские – Байков, Гудцов, Гуляев развивали науку о диаграмме Fe-С.
При 768 0 С и выше железо становится немагнитным. Железо со многими элементами образует сплавы (растворы):
а) с металлами – растворы замещения, с Fe3C также раствор замещения;
б) с лёгкими элементами – растворы внедрения (C, B, N, и др.).
Растворимость углерода в железе зависит от его кристаллической решётки. В Fea растворится от 0,005% (20 0 С) до 0,02% (723 0 С), в Feg растворится максимально 2,14% углерода.
Рисунок 29 – Микроструктура технического железа. Феррит
Рисунок 30 –Структура аустенита углеродистой стали, выявленная травлением при высоких температурах
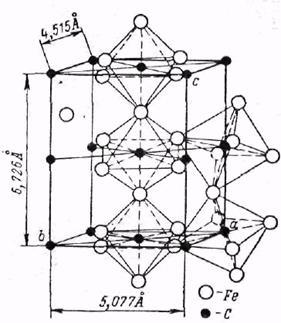
Цементит (Ц, Fe3C) – это химическое соединение углерода с железом (карбид железа), имеющий свою решётку, физико-химические свойства (рис 31). Температура плавления
1500 0 С, не полиморфен, слабо магнитен. Он имеет высокую твёрдость (80 HRС), низкую пластичность. Цементит с железом и другими металлами образует твёрдые растворы замещения. Углерод может замещаться азотом, кислородом, бором и др., атомы железа металлами: Mn, Cr, W, Ni, Co, Cu и т.д. Такой твёрдый раствор на базе решётки цементита и железа называется легированным.
Рисунок 31 – Кристаллическая структура цементита
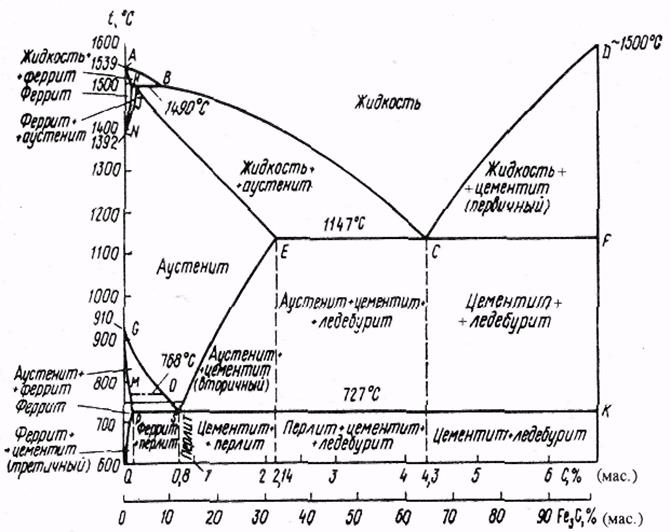
Диаграмма Fe – C изображена на рисунке 32.
Рисунок 32 – Диаграмма фазового состояния Fe-Fe3C
Линия ABCД – ликвидус, AHJECF – солидус. В системе существуют следующие фазы:
— жидкий сплав (раствор) углерода в железе обозначается Ж или Z;
— цементит (Fe3C) линия ДFKL (Ц);
— феррит (Fea, Ф, a) расположен в областях GPQ и AHN;
— аустенит (Feg, А, g) занимает область NJESG.
На диаграмме имеется три горизонтальные линии HJB, ECF, PSK указывающие на протекание трёх реакций. При 1499 0 С ЖB+ФН ®АJ; реакция протекает у сплавов, содержащих углерод от 0,1 до 0,5 %. Реакция – перитектическая. При 1147 0 С протекает эвтектическая реакция ЖС ®AE +ЦF в результате образуется механическая смесь аустенита и цементита – эвтектика – ледебурит. Реакция протекает у всех сплавов, содержащих углерод более 2,14%. При температуре меньше 727 0 С ледебурит состоит из перлита и цементита.
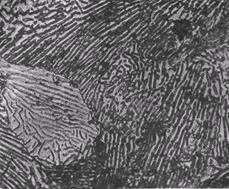
При 727 0 С протекает эвтектоидная реакция AS ®ФР +ЦК. Продуктом её является механическая смесь феррита и цементита вторичного – перлит (рис. 33). Перлитное превращение происходит у всех сплавов, содержащих углерод более 0,02%.
Рисунок 33 – Структура перлита
Диаграмма Fe – Fe3C – метастабильная. Концентрация углерода для характерных точек следующая: B – 0,51 %C, H – 0,1 %C, J – 0,16 %C, E – 2,14 %C, C – 4,3 %C, S – 0,8 %C, P – 0,02 %C.
В системе Fe – Fe3C имеются сплавы: сталь и чугун. Стали содержат углерод до 2,14 %, чугуны от 2,14 до 6,67 %, сталь, содержащая 0,8 % углерода называется эвтектоидной, чисто перлитной. Стали доэвтектоидные (конструкционные) содержат до 0,8 % углерода; стали, содержащие углерод от более 0,8 до 2,14 называются заэвтектоидными (инструментальными). На рисунке 34 показана доэвтектоидная (Ф+П), эвтектоидная (П) и заэвтектоидная (П+Ц2) стали. Перлит имеет кристаллы феррита вперемешку с кристаллами цементита.
а – доэвтектоидная сталь;
б – эвтектоидная сталь;
в – заэвтектоидная сталь
Рисунок 34 – Микроструктура сталей
Понятие сплав. Компоненты сплава. Фазы и структурные составляющие



Сплав – вещество, полученное сплавлением нескольких элементов. Другими словами, сплав – это твердое вещество, обладающее всеми признаками металлов и состоящее из 2-х и более химических элементов. Состоят из основы (одного или нескольких металлов), малых добавок специально вводимых в сплавлегирующих и модифицирующих элементов, а также из неудалённых примесей (природных, технологических и случайных).
Компонент – элемент или химическое соединение, входящее в состав сплава (элементы или химические соединения, образующие сплав). Компонент, преобладающий в сплаве количественно, называется основным. Компоненты, вводимые в сплав для придания ему нужных свойств, называются легирующими.
Фазовая составляющая (фаза) – однородная часть сплава, характеризующаяся определенным составом, свойствами, типом кристаллической решетки и отделенная от других частей сплава поверхностью раздела (при переходе через которую химический состав, структура, а, следовательно, свойства меняются скачкообразно).
Сплавы могут быть и однофазными и многофазными. Однофазные сплавы всегда состоят из кристаллов твердого раствора одного вида (состава).
В многофазных сплавах может одновременно присутствовать несколько структурных составляющих: 1) кристаллы твердого раствора (одного или нескольких составов), 2) кристаллы химических соединений, 3) кристаллы компонент сплава, 4) эвтектики и 5) эвтектоиды.
Основными структурами, составляющими железоуглеродистые сплавы, являются следующие.
Феррит – твердый раствор углерода в α-Fe. При температуре 723° С предельное содержание углерода 0,02 %. При отсутствии примесей не корродирует.
Цементит – карбид железа Fe3C – химическое соединение, содержащее 6,67 % углерода. Является составной частью эвтектической смеси, а также самостоятельной структурной составляющей. Способен образовывать твердые растворы путем замещения атомами других металлов, неустойчив, распадается при термической обработке. Цементит очень тверд (НВ 800) и хрупок.
Аустенит – твердый раствор углерода в γ–Fe. Атомы углерода внедряются в кристаллическую решетку, причем насыщение может быть различным в зависимости от температуры и примесей. Устойчив только при высокой температуре, а с примесями Mn, Сг – при обычных, даже низких температурах. Твердость аустенита НВ 170. 220.
Перлит – эвтектоидная смесь феррита и цементита, образуется при распаде аустенита при температуре 723° С и содержании углерода 0,83 %. Примеси Si и Мn способствуют образованию перлита и при меньшем содержании углерода. Твердость перлита НВ 160. 260. Структура перлита может быть пластинчатой и глобулярной (зернистой).
Ледебурит – эвтектическая смесь аустенита и цементита, образующаяся при 1130° С и содержании углерода 4,3 % Структура неустойчивая: при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит. Ледебурит очень тверд (НВ 700) и хрупок.
Графит – мягкая и хрупкая составляющая чугуна, состоящая из разновидностей углерода. Встречается в серых и ковких чугунах.
1. В жидком состоянии компоненты сплава обычно неограниченно растворяются друг в друге, образуя жидкие растворы.