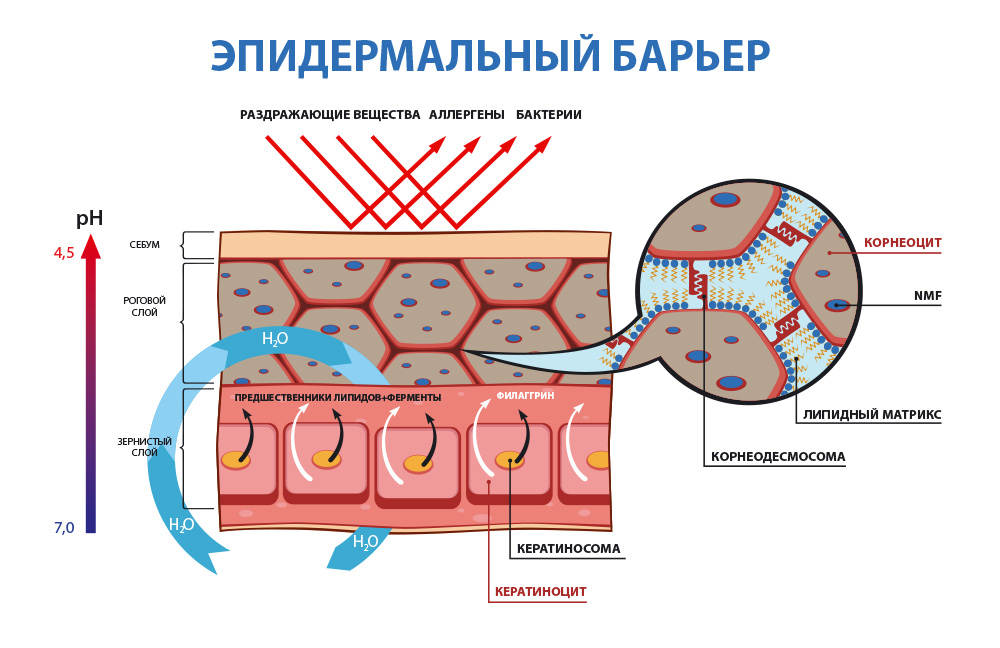
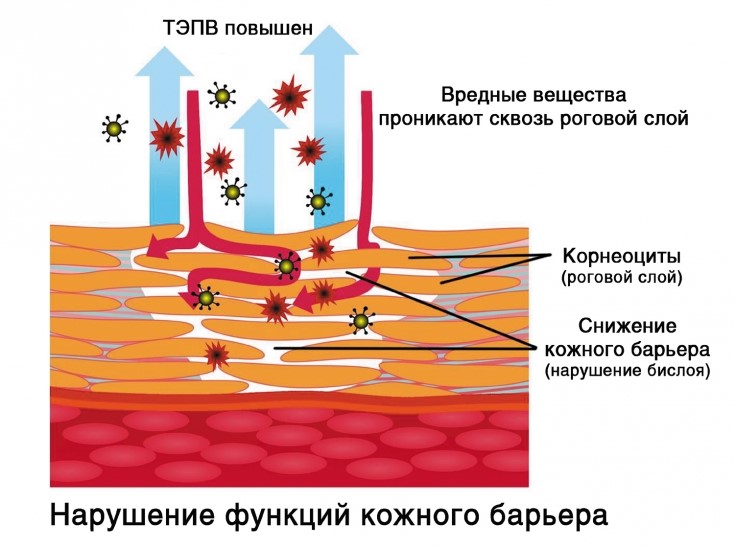
что в коже осуществляет барьерную функцию
Гидролипидная мантия кожи. Кожа и два ее барьера
Гидролипидная мантия кожи – одна из составляющих эпидермального барьера кожи.
Здоровье кожи в широком смысле этого слова – её качество, цвет, тонус, увлажненность и т.п. – напрямую зависит от состояния эпидермального барьера. Многие дерматологические проблемы возникают именно из-за «брешей» в его работе.
Нарушения функции и дефекты в этом барьере неизбежно провоцируют проникновение чужеродных микробов и аллергенов в кожу, активируют дегидратацию эпидермиса и вызывают сухость кожи, повышают её чувствительность к различным воздействиям окружающей среды.
Что же такое эпидермальный барьер
Кожа – самый большой орган человеческого тела. Она составляет почти 18% общего веса человека.
В составе кожи три основных слоя:
Эпидермальный барьер состоит из:
1. Гидролипидная или водно-жировая мантия
— это, некая, невидимая глазу пленка на поверхности кожи, которая образуется из смеси отслоившихся роговых чешуек, пота, кожного сала, а также органических кислот и микрофлоры.
Благодаря наличию кислой среды, в которой перестают размножаться и погибают вредоносные бактериии, гидролипидная мантия является самым первым звеном защиты кожи от большинства чужеродных микроорганизмов и агентов.
Кислотность гидролипидной мантии может нарушаться в ту или иную сторону по разным причинам (будет описано ниже). Например, при грибковых заболеваниях рН возрастает до 6, при экземе до 6,5; при угревой болезни защелачивается до 7.
Повреждённая гидро-липидная мантия кожи восстанавливается самостоятельно при правильном очищении, грамотном уходе и защите.
2. Липидо-эпидермальный барьер
– основной защитный барьер кожи. Находясь непосредственно в эпидермисе, он защищает организм и кожу от обезвоживания путем механизма транс-эпидермальной потери влаги (ТЭПВ), а также является вторым звеном защиты после гидролипидной мантии от проникновения в кожу патологических бактерий и аллергенов, различных химических соединений.
Основу липидо-эпидермального барьера составляют три вида липидов — церамиды, свободные жирные кислоты и холестерин.
Механизм ТЭПВ. По большому счету кожа увлажняется изнутри – то есть из глубоких слоёв гиподермы и дермы вода поступает к эпидермису, липиды удерживают воду в эпидермисе, обеспечивая его увлажненность. Повреждённый липидо-эпидермальный барьер является главной причиной неадекватной трансэпидермальной потери влаги и в результате сухости кожи. Поэтому, чтобы обеспечить хорошую увлажненность кожи, необходимо в первую очередь восстановить липидный барьер.
Кроме того, бреши в липидо-эпидермальном барьере приводят не только к обезвоженности кожи, но и к её повышенной чувствительности, аллергическим реакциям, раздражениям и кожным заболеваниям.
Незначительные повреждения липидо-эпидермального барьера клетки кожи восстанавливают сами. В случае выраженных нарушений – им необходимо помочь. В первую очередь это процедуры регулярного увлажнения, правильного ухода за поверхностью кожи и дермы, здоровый образ жизни и сбалансированное питание.
Внешние проявления, связанные с повреждением гидролипидной мантии
Наличие вышеперечисленных проблем – повод обратиться к дерматологу.
Факторы, повреждающие кожные барьеры
Применение при очищении кожи мыла, умывалок и др., содержащих ПАВы и щелочи; частое использование обезжиривающих и спиртовых тоников.
Щелочи и ПАВы, присутствующие в большинстве очищающих средств нарушают кислый pН гидролипидной мантии. В результате водно-жировая мантия разрушается. Открываются входные ворота для чужеродных бактерий. Повреждается липидный барьер, вода активно начинает испаряться с поверхности кожи, вызывая её сухость.
Здоровый эпидермальный барьер — залог красивого вида любого типа кожи — жирной, проблемной, сухой, чувствительной и даже увядающей.
Сохранение и восстановление эпидермального барьера один их самых ключевых принципов в профессиональных программах по уходу за любым типом кожи и омолаживающих врачебных процедурах, а также домашнего хода за кожей.
Методы восстановления и сохранения барьеров кожи
Адекватное очищение кожи.
Домашний уход. Важно правильно определить с профессиональным дерматологом свой тип кожи и использовать ежедневно очищающие средства, которые соответствуют вашему типу кожи, не нарушая при этом эпидермальный барьер.
Профессиональный уход. В условиях клиники – проведение грамотно подобранных процедур очищения и эксфолиации кожи и соблюдения режима их выполнения: химического пилинга, и лазерного пилинга,ручной чистки лица с учётом вашего типа кожи и решаемых проблем.
Регулярное увлажнение.
Домашний уход. Ежедневно наносите на кожу увлажняющие кремы и периодически маски, содержащие компоненты, удерживающие влагу: аминокислоты, гиалуроновую кислоту, коллаген, эластин, алое вера и др. Плюс, как это ни банально, пейте адекватное количество чистой воды.
Профессиональный уход в условиях клиники. Регулярно (курсами 2 раза в год) проводите процедуры биоревитализации, биорепарации, мезотерапии
Профессиональный уход в условиях клиники. При повреждении кожи и развитии патологической флоры, например при угревой болезни – применение различных медикаментозных препаратов, назначенных врачом, а также лечение акне на лазерной установке Fotona с целью инактивации патологической флоры, уменьшения воспалительного процесса и улучшения трофики тканей.
Сбалансированное питание и уход.
Домашний уход. Ежедневно используйте питательные крема, соответствующие вашему типу кожи, возрасту и времени сезона года, чередуйте их с увлажняющими средствами. Отдавайте предпочтение средствам, содержащим церамиды, липосомы и жирные кислоты – они защищают и восстанавливают повреждённый липидный слой.
Употребляйте в пищу продукты, богатые омега 3 и омега 6 жирными кислотами. Не исключайте из рациона масла и жиры.
Постоянная защита.
Подводим итоги
Здоровье кожи напрямую зависит от целостности и нормального функционирования эпидермального барьера, основу которого составляет гидро-липидная мантия и липидо-эпидермальный барьер.
Сверху эпидермальный барьер «окутан» в гидролипидную мантию. Важно бережно относиться к ней и не повреждать её. Она первая «встречает» патогенные микробы и агенты, препятствуя их проникновению вглубь кожи.
Повреждение липидо-эпидермального барьера и гидролипидной мантии является серьёзной проблемой для кожи. Как правило, это приводит к обезвоживанию эпидермиса, появлению сухости, повышенной чувствительности, раздражениям, может спровоцировать и поддерживать кожные заболевания и др.
Нарушенный эпидермальный барьер можно восстановить, если правильно подобрать домашний уход, а также проводить профессиональные процедуры у косметолога. Сбалансированный уход за кожей и правильный образ жизни обеспечат защиту, увлажнение и восстановление кожи.
Эпидермальный барьер: от нормы к патологии
В представленной статье обобщены современные данные о строении и функции эпидермального барьера, рассмотрены вопросы его роли в развитии атопического дерматита.
This article summarizes current data on the structure and function of the epidermal barrier, we also considered its role in development of atopic dermatitis.
С тех пор как наземная жизнь стала угрожать млекопитающим обезвоживанием, все более становятся актуальными исследования структурных, клеточных, биохимических и регуляторных механизмов организма, участвующих в поддержании гомеостаза проницаемости эпидермального барьера [1].
Кожа обеспечивает жизненно важную функцию, защищая позвоночных от повседневных и экстремальных влияний факторов внешней среды, таких как воздействие антигенов, ультрафиолетового света, моющих средств, микроорганизмов, токсинов, наночастиц и иных повреждений [2]. Таким образом, эпидермальный барьер, являясь физическим барьером [3], обеспечивает защиту организма на границе двух сред, ограничивая как потерю воды из организма, так и попадание патогенных микроорганизмов в организм [4].
Важнейшая составная часть эпидермального барьера, от которой зависит проникновение раздражителей и аллергенов, находится в нижней части рогового слоя [5]. Несмотря на минимальные размеры (толщина около 7–35 мкм), он играет определяющую роль в формировании защитного барьера и способствует предотвращению чрезкожного проникновения патогенов. Кроме роли физического барьера, роговой слой участвует в терморегуляции, газообмене, гидратации, обеспечении врожденного иммунитета, а создавая определенную pH поверхности кожи (слегка кислую), обеспечивает дополнительную защиту от болезнетворных микроорганизмов [6].
Во время терминальной дифференцировки кератиноциты зернистого слоя «заменяют» свою клеточную мембрану на нерастворимый белковый слой — роговую оболочку [7]. Она придает прочность корнеоцитам и является «платформой» для прикрепления липидов. Роговая оболочка в основном сформирована структурными белками, такими как лорикрин, инволюкрин, филаггрин (ФЛГ) и малыми пролин-богатыми белками. Особенно важен филаггрин, объединяющий кератиновые волокна клеток, «скручивая» кератиноциты в уплощенные диски с большой площадью поверхности [8].
Вокруг корнеоцитов расположены холестерин, фосфолипиды и церамиды, создавая многослойную мембрану из липидных пластинок [3, 9]. Последние играют важную роль в регуляции водного гомеостаза кожи, помогают сохранять воду в организме, а также предотвращают проникновение патогенных микроорганизмов и аллергенов [10].
На границе между роговым и зернистым слоями происходит секреция ламеллярных телец, содержащих предшественники липидов, а также необходимые ферменты для переработки этих прекурсоров в зрелые составляющие липидной матрицы [11]. Перед секрецией происходит сборка ламеллярных телец в пластинчатом комплексе, посредством дифференцированной их упаковки с различным содержимым [12]. Кроме вышеупомянутых метаболитов липидов, липидные тельца доставляют в межклеточное пространство рогового слоя протеолитически активные ферменты, такие как сериновые протеазы семейства калликреина, а также их ингибиторов, в том числе и лимфоэпителиальный ингибитор сериновых протеаз типа Kazal-5 (LEKTI) [13].
Единство между корнеоцитами рогового слоя зависит прежде всего от корнеодесмосом. Подобно десмосомам, они поддерживают целостность тканей посредством молекул межклеточной адгезии с помощью кальций-зависимых взаимодействий между двумя представителями семейства кадгерина, внеклеточных трансмембранных гликопротеинов — десмоглеина и десмоколлина. Внутри корнеоцитов десмоглеин и десмоколлин соединяют кератиновые филламенты корнеодесмосом посредством «соединительной бляшки», состоящей из плакоглобина, десмоплакина и плакофиллина. Десмоглеин и десмоколлин перемещаются от оболочки корнеоцитов в липидную пластину между корнеоцитами и связывают воедино белки соседних клеток. Кроме того, в процессе кератинизации эпителия экспрессируется специфический белок с молекулярной массой 52 кДа — корнеодесмосин [8, 14]. После секреции в экстрацеллюлярное пространство корнеодесмосин перемещается в область между зернистым и роговым слоями и проникает в десмосому. Появление корнеодесмосина знаменует переход от десмосом к корнеодесмосомам [3, 12].
Во время «нормальной» десквамации рогового слоя самые поверхностные корнеоциты «уходят» с поверхности кожи, замещаясь кератиноцитами, подвергшимися терминальной дифференцировке [14, 15]. Таким образом, существует «тонкий» баланс между базальной клеточной пролиферацией и десквамацией рогового слоя. Это обеспечивает постоянное обновление клеток эпидермиса, а также способствует поддержанию одинаковой толщины эпителия [14, 16]. Caubet и соавт. [15] описали несколько деградационных протеаз, которые разрушают внеклеточные корнеодесмосомальные адгезивные белки, связывающие корнеоциты вместе.
В роговом слое среди протеаз, вовлеченных в процесс десквамации, присутствуют хемотрипсиновые (SCCE) и трипсиновые ферменты (SCTE), которые экспрессируются кератиноцитами зернистого слоя и находятся во внеклеточном пространстве рогового слоя [14]. Данные протеазы гидролизуют корнеодесмосин и десмоколлин [15]. Их активность контролируется семейством специфических ингибиторов, в которое входит LEKTI [17]. При этом скорость десквамации коррелирует с количеством ингибиторов протеаз, поступивших из ламеллярных телец [3].
На барьерную функцию эпидермиса влияют структура, дифференцировка, функциональная активность кератиноцитов, качественный и количественный состав липидов рогового слоя эпидермиса, наличие веществ, относящихся к естественному увлажняющему фактору, а также рН поверхности кожи [18]. При изменении каких-либо из перечисленных показателей барьерная функция эпидермиса нарушается, что приводит к усиленному испарению воды через роговой слой. У человека эпидермальный барьер восстанавливается на 60% через 12 часов, а полное восстановление занимает 72 часа [19]. Полагают, что быстрое восстановление эпидермального барьера происходит за счет массового выброса из клеток готовых ламеллярных телец. В медленную фазу восстановления усиливается синтез жирных кислот, холестерина, церамидов, а также образование новых ламеллярных гранул. Нарушение восстановления кожного барьера приводит к обезвоживанию эпидермиса и развитию выраженной сухости кожи, что и наблюдается при развитии атопического дерматита (АД) [20].
Повреждение эпидермального барьера способствует проникновению через кожу микробов, аллергенов и различных поллютантов (токсины, раздражающие и загрязняющие вещества). Проникновение агентов с антигенными свойствами увеличивает риск сенсибилизации, поскольку взаимодействие аллергенов и аллерген-представляющих клеток кожи инициирует воспаление [14]. Степень дисфункции барьера коррелирует со степенью воспаления и тяжестью АД [11]. Впервые Y. Werner и M. Lindberg (1985 г.) привели доказательства нарушений барьерной функции кожи, измерив трансэпидермальную потерю воды (ТЭПВ) у лиц с АД. Авторам удалось показать, что у больных АД нарушения эпидермального барьера отмечаются не только в очагах активного воспаления, но и на клинически неизмененной коже [10, 21].
Изменения в свойствах эпидермального барьера, которые наблюдаются при АД, включают увеличение ТЭПВ, изменения рН поверхности кожи, повышение ее проницаемости, увеличение бактериальной колонизации, изменение в экспрессии антимикробных пептидов, а также нарушение его целостности. При аномалии эпидермального барьера аллергены, раздражающие и другие вещества могут проникать через кожу, способствуя обострению АД [6].
В настоящее время нарушение функции кожного барьера является одним из ведущих этиопатогенетических факторов АД. По данным разных авторов у 30–66% больных АД протекает без изменения уровня общего IgE в сыворотке крови и специфичных IgE к аллергенам. Полагают, что именно у этих пациентов нарушение функции кожного барьера играет ведущую роль в развитии и прогрессировании заболевания [22].
В последние годы определен ряд генетических мутаций, приводящих к изменениям в роговом слое эпидермиса. Так, у больных АД определяются мутации гена профилаггрина [23], способствующие нарушению синтеза белка ФЛГ — одного из компонентов цитокератинового скелета, обеспечивающего ороговение кератиноцитов. В результате изменения терминальной дифференцировки кератиноцитов развивается их функциональная несостоятельность [24]. Кроме того, снижение экспрессии гена ФЛГ уменьшает уровень «натурального увлажняющего фактора» [25]. Дефицит ФЛГ и/или продуктов его деградации способствует сухости кожи, что коррелирует с клинической картиной нарушения эпидермального барьера при АД [26]. Более того, при уменьшении ФЛГ усиливается «раздражающий» эффект аллергенов на дендритные клетки, понижая при этом порог их чувствительности к воспалению, что демонстрирует важность этого белка в предотвращении пенетрации аллергенов [27].
Кроме того, у больных АД выявлены полиморфные варианты гена SPINK5, приводящие к дизрегуляции синтеза ингибитора сериновой протеазы LEKTI, который в норме блокирует избыточную продукцию SCCE [28]. Активность деградационных протеаз также значимо связана с дефектом кожного барьера при АД [23]. Разбалансировка функционирования этих ферментов ведет к усиленному отшелушиванию клеток и истончению рогового слоя, увеличивая проницаемость эпидермального барьера [14]. Установлено, что у больных АД изменена липидная мантия рогового слоя, предупреждающая ТЭПВ. Отмечается низкий уровень церамидов первого и третьего типов в сочетании с повышением уровня свободного холестерола [29]. Повышение уровня рН на поверхности кожи приводит к снижению синтеза липидов и активизации ферментов (в частности, SCCE), повреждающих корнеодесмосомы. Уменьшение количества веществ, относящихся к «натуральному увлажняющему фактору», также способствует нарушению функционирования эпидермального барьера [30].
Таким образом, у больных АД отмечается комплекс нарушений, приводящих к дисфункции кожного барьера, усилению ТЭПВ и обезвоживанию кожных покровов [14]. Из вышеуказанного следует, что пациенты с АД могут иметь дефект кожного барьера, в основе которого лежат как генетические, так и приобретенные механизмы. Этот дефект способны спровоцировать внешние факторы, такие как царапины, использование моющих средств, микробная колонизация, а также воздействие протеаз различных аллергенов (в частности, протеаз клещей домашней пыли) [10]. Распознание конкретных механизмов, участвующих в патогенезе воспалительных заболеваний кожи, в частности, АД, безусловно, будет способствовать поиску и разработке новых, более эффективных методов воздействия на патологический процесс с минимальным количеством системных эффектов [8].
Литература
ГБОУ ВПО БГМУ МЗ РФ, Уфа
Что в коже осуществляет барьерную функцию
А. Б. КОТЕЛЬНИКОВА, О. И. ФРОЛОВА, Т. В. РАЕВА, Н.П. И ШУТИНА
Включение Гептрала (адеметионина) в комплексную программу лечения данной категории больных способствует достоверному уменьшению степени тяжести патологического процесса (индекса PASI) и выраженности нарушений качества жизни.
| «КАРТАЛИН» — ПРЕПАРАТ ВЫБОРА В НАРУЖНОЙ ТЕРАПИИ ХРОНИЧЕСКИХ ДЕРМАТОЗОВ Псориаз и атопический дерматит — дерматозы, к которым большой интерес проявляют многие научные исследователи, но до сих пор вопрос патогенеза остается до конца не изученным. Учитывая высокий процент болеющих людей среди населения с данной патологией кожи, ведется активный поиск и внедрение средств системного действия и наружно применяемых лекарственных форм, прежде всего восстанавливающих процессы дифференцировки и пролиферации кератиноцитов, а следовательно, нормализующих структуру и функциональные возможности эпидермиса. |
| К СТЕРОИДНОЙ ТЕРАПИИ ТЯЖЕЛЫХ ДЕРМАТОЗОВ Н.Г. КОЧЕРГИН, Л.М. СМИРНОВА, Н.П. ТЕПЛЮК Последние полтора десятка лет среди отечественных дерматологов популярностью пользуется термин «стероидчувствительные дерматозы» (СЧД), включающий обширную группу различных кожных заболеваний, при которых глюкокортикостероидные препараты дают различной степени выраженности клинический эффект, нередко являясь единственным решением терапевтической проблемы в конкретном случае. Чаще кортикостероиды при СЧД применяются в виде наружных средств, однако при ряде тяжело протекающих дерматозов необходимой становится системная глюкокортикостероидная терапия, будучи подчас единственной эффективной и даже жизненно необходимой альтернативой. |
| ДИФФЕРЕНЦИРОВАННАЯ ТОПИЧЕСКАЯ ТЕРАПИЯ БОЛЬНЫХ ПСОРИАЗОМ МЕДИЦИНСКАЯ ТЕХНОЛОГИЯ № ФС-2007/086-У ОТ 3 МАЯ 2007 ГОДА Проблема эффективной терапии больных псориазом остается одной из наиболее актуальных в современной дерматологии в связи с хроническим, рецидивирующим течением заболевания, сложностью патогенетических механизмов развития дерматоза, и несмотря на значительное число исследовательских работ, и появлением новых лекарственных средств. |
| ВЛИЯНИЕ ОЗОНОТЕРАПИИ НА ИММУННЫЕ НАРУШЕНИЯ У БОЛЬНЫХ ПСОРИАЗОМ P.M. ЗАГРТДИНОВА, М.А. ИВАНОВА, Д.Е. КОЛОДКИН, А.Я. СНЕГИРЕВ Актуальность псориаза обусловлена незавершенностью концепций патогенеза, увеличением удельного веса тяжело текущих, торпидных к лечению форм. В последние годы складывается мнение о том, что ведущая роль в патогенезе псориаза принадлежит иммунным нарушениям. Коррекция иммунных нарушений весьма затруднительна в связи с их неоднородностью. |
| РОЛЬ ВРОЖДЕННОГО И АДАПТИВНОГО ИММУНИТЕТА В ПАТОГЕНЕЗЕ ПСОРИАЗА О.Р. КАТУНИНА |
| УЛЬТРАЗВУКОВОЕ СКАНИРОВАНИЕ, КАК НЕИНВАЗИВНЫИ МЕТОД ДИАГНОСТИКИ БАЗАЛЬНО-КЛЕТОЧНОГО РАКА КОЖИ Е.В. ПРЯДКИНА, О. Р. КАТУНИНА |
| Базально-клеточный рак кожи: диагностика, лечение В.Н. Волгин, Т.В. Соколовская, М.С. Колбина, А.А. Соколовская Проблема совершенствования методов диагностики и выбора оптимальных способов лечения базально-клеточного рака кожи (БКРК) является очень актуальной в современной дерматологии и онкологии. Это обусловлено, во-первых, неуклонным ростом заболеваемости БКРК, во-вторых, частым рецидивированием опухолевого процесса после различных методов лечения. |
| БАРЬЕРНЫЕ СВОЙСТВА КОЖИ И БАЗОВЫЙ УХОД: ИННОВАЦИИ В ТЕОРИИ И ПРАКТИКЕ Е.Р. АРАВИЙСКАЯ, Е.В. СОКОЛОВСКИЙ В последние годы в дерматологии и косметологии большое значение придается барьерным свойствам кожи, а также базовому уходу как за пораженной. так и за здоровой кожей. Это связано, с одной стороны, со стремительным развитием науки. С другой стороны, повышенный интерес к данной проблематике обусловлен постоянным появлением на рынке новых очищающих и увлажняющих средств. В настоящем обзоре освещаются представления о барьерных свойствах кожи, основанные на последних научных данных, сведения об их нарушении и принципах коррекции при различных состояниях. |
| Некоторые аспекты патогенеза псориаза и особенности комплексного лечения больных И.Б. ТРОФИМОВА, Л.М. БАРДЕНШТЕЙН, Я.Ю. ВОРОНИНА, B.C. СУСКОВА Псориаз — одно из наиболее распространенных дерматозов. Доля больных псориазом среди всех больных с кожными болезнями, по данным разных авторов, составляет 2—10%, а среди стационарных больных в кожных отделениях — 6,5—22%. Все чаще встречаются тяжелые и резистентные к терапии клинические формы дерматоза. |
| Сравнительная оценка эффективности лечения больных обыкновенными бородавками деструктивными методами Ю.Ю. Штиршнайдер, В.А. Волнухин Обыкновенные бородавки (син. вульгарные, простые бородавки) — доброкачественные эпителиальные опухоли, вызываемые вирусом папилломы человека (HPV), как правило, типов 1—4, 7, 26—29, 38, 41, 49, 57, 63, 65, 75—77, встречаются у 7—10% популяции. В литературе описано более 30 различных методов лечения бородавок, что свидетельствует об отсутствии на сегодняшний день универсального средства лечения. |
| Функциональные особенности макрофагов в очаге витилиго В.В. Жульмина, Е.Н. Кологривова, П.Н. Пестерев, Н.П. Лабзовская Витилиго — мультифакторное приобретенное полигенное заболевание кожи из группы дисхромий, характеризующееся хроническим течением, появлением на коже депигментированных пятен белого цвета, склонных к периферическому росту, слиянию вследствие отсутствия либо снижения содержания меланина в коже. По данным ВОЗ, в мире страдают витилиго от 0,2 до 1% всего населения (около 30 млн человек). |
| Базально-клеточный рак кожи: эпидемиология, этиология, патогенез, клиническая картина. Часть 1. В.И. Волгин, Т.В. Соколова, М.С. Колбина, А.А. Соколовская |