что в фармакологии обозначают понятием рецепторам
Что в фармакологии обозначают понятием рецепторам
Рецепторы — макромолекулы, функция которых заключается в связывании веществ-посредников и в преобразовании этой связи в действие, т, е. изменение клеточной функции. Рецепторы отличаются по своей структуре и способу преобразования контакта с лигандом в клеточный ответ (преобразование сигнала).
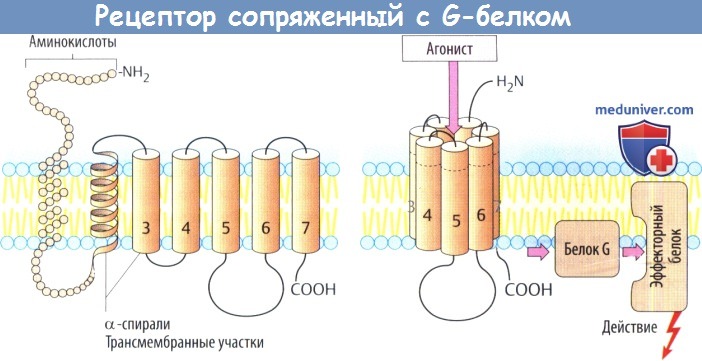
а) Рецепторы, сопряженные с белком G, состоят из цепи аминокислот, которая направлена в сторону мембраны и от нее в виде серпантина. С вне-мембранными петлевыми участками молекулы связаны углеводные остатки через различные точки N-гликозилирования.
Семь а-спиральных, охватывающих мембрану участков образуют окружность возле центральной ниши, которая несет участки для связывания медиаторных веществ. Связывание молекулы медиатора или структурно связанной молекулы агониста вызывает изменение конформации белка, в результате чего он вступает во взаимодействие с белком G (белок, связывающий нуклеотид гуанил).
Белки G располагаются в нижнем слое плазмолеммы и состоят из трех субъединиц, обозначаемых а, β и γ. Существует несколько белков G, которые отличаются в основном своей a-единицей. Контакте рецептором активирует белок G, что, в свою очередь, приводит к активации другого белка (фермента, ионного канала). Многие медиаторы действуют через рецепторы, сопряженные с белком G.
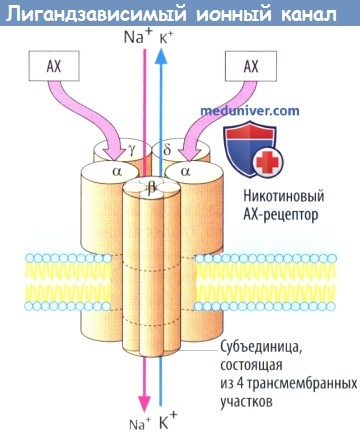
б) Примером лигандзависимого ионного канала является никотиновый холинорецептор на концевой пластинке двигательного нерва. Рецепторный комплекс образован пятью субъединицами, каждая из которых содержит четыре трансмембранных участка.
Одновременное связывание двух молекул АХ двумя а-субъединицами приводит к открытию ионного канала со входом Na + (и выходом некоторого количества К + ), деполяризации мембраны и активации потенциала действия. Нейронные N-холинорецепторы, очевидно, состоят лишь изо- и β-субъединиц.
Ряд рецепторов медиатора γ-аминомасляной кислоты (ГАМК) принадлежат к данной группе: подтип ГАМКA связан с хлорными каналами (и с участком связывания бензодиазепинов). Глутамат и глицин оба действуют через лигандзависимые ионные каналы.
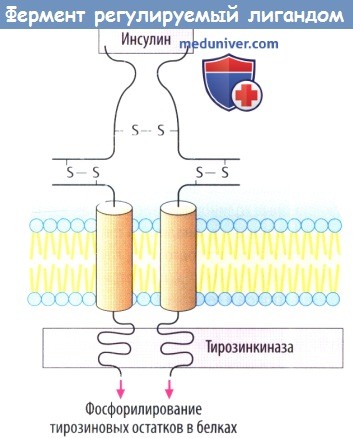
в) Белок инсулинового рецептора представляет собой управляемый лигандом фермент, каталитический рецептор. При связывании инсулина с внеклеточным участком «отключается» активность тирозинкиназы внутри клетки. Фосфорилирование белка приводит к изменению клеточной функции в результате образования других сигнальных белков. Рецепторы гормонов роста тоже принадлежат к классу каталитических рецепторов.
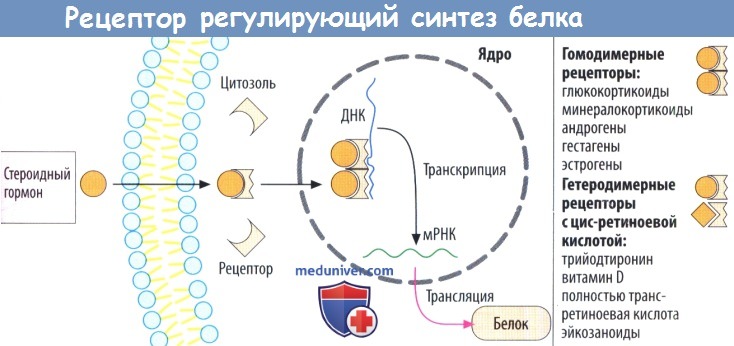
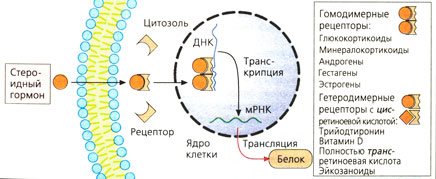
г) Рецепторы, регулирующие синтез белка, стероидов и гормонов щитовидной железы, находятся в цитозоле и в клеточном ядре соответственно. Белки рецепторов также расположены внутриклеточно, в зависимости от гормона — в цитозоле (глюкокортикоиды, минералокортикоиды, андрогены и гестагены) или в клеточном ядре (эстрогены, гормоны щитовидной железы).
При связывании гормона открывается скрытый в норме участок белка рецептора, что дает возможность последнему связаться с особой последовательностью нуклеотидов ДНК в гене и регулировать его транскрипцию. Из этого следует, что комплексы лиганд-рецептор работают как факторы, регулирующие транскрипцию. Обычно происходит активация или усиление и, редко, блокада транскрипции.
Комплексы гормон-рецептор взаимодействуют парно с ДНК. Эти пары (димеры) могут состоять из двух идентичных комплексов гормон-рецептор (гомодимерная форма, например, с гормонами надпочечников или половыми гормонами). Комплекс тиреоидный гормон-рецептор встречается в гетеродимерной форме и сочетается с комплексом цис-ретиноевая кислота-рецептор.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Виды рецепторов фармакологических препаратов
Содержание
Типы рецепторов [ править | править код ]
Рецепторы — это макромолекулы, которые способны присоединять биологически активные вещества-переносчики, в результате чего происходит изменение клеточной функции. Рецепторы различаются по строению и типу передачи сигнала (трансдукция сигнала).
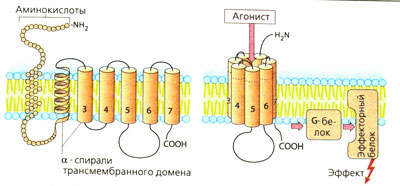
Рецепторы, связанные с G-белком (А), состоят из аминокислотной цепи, которая многократно пронизывает мембрану в форме а-спиралей. Вне мембраны рецепторы связаны с остатками сахара (гликозилированы). Предполагают, что семь трансмембранных доменов расположены по кругу, а в центре находится углубление со специальными участками связывания переносчика. Присоединение переносчика или схожего агониста приводит к изменению конформации рецепторных белков, благодаря чему открывается доступ к G-белку (гуанин-нуклеотид-связывающий белок). G-Белок расположен на внутренней стороне мембраны и состоит из трех субъединиц: а, β и у. Разные G-белки отличаются строением а-субъединиц. Контакт с рецептором приводит к активации G-белка, что в свою очередь влияет на другие белки (ферменты, ионные каналы). Очень многие вещества-переносчики действуют через рецепторы, связанные с G-белком.
Примером лиганд-зависимого ионного канала (Б) является никотиновый холинорецептор мотонейрона. Рецепторный комплекс состоит из пяти субъединиц; каждая содержит по четыре трансмембранных домена. Одновременное присоединение двух молекул ацетилхолина (ACh) к обеим а-субъединицам приводит к открытию ионных каналов для входа Na+ (и выхода К+), деполяризации мембраны и возникновению потенциала действия. N-Xoлинорецепторы ганглиев состоят только из а- и β-субъединиц (а2рз). Часть ГАМ К-рецепторов (лигандом для которых является у-аминомасляная кислота) также относится к этому типу рецепторов: ГАМКд-рецептор содержит один хлорный канал (и, кроме того, участок связывания бензодиазепина).
К лиганд-зависимым ферментам (В) относится инсулиновый рецептор, который представляет собой каталитический рецептор. Если инсулин присоединяется к внеклеточному центру связывания, то во внутриклеточной части «включается» тирозинки-назная активность. Фосфорилирование белков приводит к изменениям функции клетки. Рецепторы гормонов роста тоже относятся к каталитическому типу.
Рецепторы, регулирующие синтез белка (Г), характерны для стероидных гормонов и гормонов щитовидной железы. Рецепторные белки расположены в цитозоле клетки (например, глюкокортикоиды, минералокортикоиды, андрогены, гестагены) или в ядре (например, экстрогены, гормоны щитовидной железы). После присоединения переносчика высвобождается скрытый домен рецепторного белка и становится возможным присоединение нуклеотидов к цепи ДНК и транскрипция определенных генов. Комплекс лиганд-рецептор является регулятором транскрипции, которая чаще всего активируется, реже блокируется.
Гормонорецепторный комплекс в виде димеров взаимодействует с ДНК. Димеры могут состоять из двух идентичных гормонорецепторных комплексов (гомодимеры, например у гормонов надпочечников или половых гормонов). Комплекс гормона щитовидной железы с рецептором образует гетеродимер с комплексом цис-ретиноевой кислоты и рецептора.

Рецепторы фармакологических препаратов [ править | править код ]
Рецепторная теория действия лекарств начала развитие с конца XIX в., когда П. Эрилих выдвинул концепцию о лекарстве как «волшебной пуле», направленной на «поражаемый рецептор». Многие годы рецепторы характеризовали по эффектам различных эндо- и экзогенных соединений, названия которых определяли номенклатуру рецепторов.
Прямая идентификация рецепторов лекарств, гормонов, нейромедиаторов стала возможной в 60-х годах XX в. благодаря разработке методов радиолигандного анализа. Более глубокое понимание структуры и функции рецепторов в последние два десятилетия достигнуто на основе молекулярно-генетических исследований. Большинство рецепторов выделено, определена их аминокислотная последовательность, клонированы сотни кодирующих рецепторы генов.
Большинство современных исследователей отличают рецепторное связывание от неспецифического, прежде всего, поскольку последнее не ведет к специфическому эффекту.
Не все лекарства влияют на рецепторы, имеющие эндогенные лиганды: фармакологическое действие может опосредоваться ферментами, небелковыми элементами — липидами, изменением содержания ионов и состава воды, другими процессами.
Взаимодействие лекарственных средств со специфическими рецепторами обеспечивается различными типами химических связей. Иногда имеет место ковалентное связывание, однако для фармакологических препаратов характерно обратимое связывание за счет комбинации электростатического взаимодействия, водородных связей, ван-дер-ваальсовых связей при высокой комплементарности лиганда к рецептору. Рецептор также должен быть стереоселективен в отношении оптических изомеров лекарств.
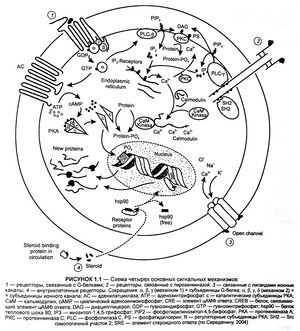
Сигнальные механизмы. На сегодняшний день выделяют четыре основных механизма, по которым экстраклеточный лиганд регулирует внутриклеточные процессы. Молекулярные основы сигнальных систем трансдукции значительно различаются.
Первой, наиболее сложной, является рецепторная система, связанная с G-белками. Она состоит из трансмембранного рецептора, к которому лиганд присоединяется на поверхности клетки, этот рецептор сопрягается с расположенным на внутренней поверхности мембраны гуаниннуклеотидсвязывающим белком (G-белком). Этот белок в свою очередь регулирует эффекторный фермент, генерирующий внутриклеточный вторичный мессенджер.
Второй тип рецепторной системы — рецепторы, связанные с тирозинкиназой и гуанилилциклазой. Они состоят из трансмембранных рецепторов, в которых внутриклеточная часть обладает ферментативной активностью, аллостерически регулируемой лигандным связыванием на внешнем по отношению к мембране участке рецептора.
Третий тип — более простая система рецептора, это регулируемый лигандом трансмембранный ионный канал. Его открытое состояние определяется прямым связыванием лиганда с экстраклеточным участком каналообразующих белков.
Четвертый тип — характерен для жирорастворимых лигандов. В этом случае проникший через мембрану лиганд связывается с внутриклеточным рецептором, далее этот комплекс присоединяется к специфическому участку ДНК в ядре и регулирует транскрипцию.
Для понимания фармакогенетического значения лиганд-рецепторного взаимодействия механизмы трансдукции следует рассмотреть более подробно.
Рецепторы, связанные с ферментами [ править | править код ]
Гуанилатциклазные рецепторы. Известен только один класс таких рецепторов для семейства пептидных гормонов, называемых предсердными натрийуретическими пептидами (atrial natriuretic peptides, ANP). Они секретируются мышечными клетками в ответ на повышение артериального давления и связываются с рецепторами в почках, где индуцируют увеличение экскреции натрия и воды, и в гладких мышцах сосудов, вызывая их релаксацию. ANP-рецептор является одиночным полипептидом, содержащим экстрацеллюлярный ANP-связывающий домен, одиночный трансмембранный домен и внутриклеточный каталитический домен с гуанилатциклазой. Активация рецептора ведет к увеличению продукции цГМФ, который в свою очередь активирует серин-треонинкиназы, цГМФ-зависимую протеинкиназу (протеинкиназу G). Белки-мишени для протеинкиназы G и сигнальные каскады, ведущие к ответу на AN Р, недостаточно изучены.
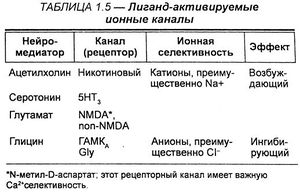
Ионные каналы, контролируемые лигандным связыванием. Синаптические нейромедиаторы связываются с группой рецепторов на постсинаптических мембранах, известных как лиганд-контролируемые ионные каналы. Среди них ацетилхолин, γ-аминомасляная кислота, глицин, глутамат. Лигандконтролируемые ионные каналы — важнейшая мишень для действия лекарственных средств, особенно психотропных. Различные ионные каналы сходны по структуре, они состоят из нескольких субъединиц, формирующих в мембране ионный канал. Каждая субъединица канала — полипептид, содержащий четыре перекрывающих мембрану домена. В то же время для них характерна специфичность связывания нейромедиаторов и селективность транспорта ионов.
В данном классе наиболее полно охарактеризован Н-ацетилхолиновый рецептор. Этот ионный канал состоит из 5 субъединиц (2а, 5, Цу), которые совместно формируют пору, проходящую через плазматическую мембрану. Закрытая позиция двух а-субъединиц внутри мембраны формирует «ворота», препятствующие прохождению ионов через канал. Ацетилхолин, присоединяясь к экстрацеллюлярным участкам двух а-субъединиц, вызывает в них конформационные изменения, ведущие к открытию канала для ионов, особенно для Na+, которые соответственно химическому градиенту идут внутрь клетки.
Взаимодействия лекарственного вещества с рецептором
, PhD, PharmD, Columbia Southern University, Orange Beach, AL
Рецепторы – это макромолекулы, участвующие в передаче химических сигналов как между клетками, так и внутри одной клетки; они могут находится на поверхности клеточной мембраны или в цитоплазме (см. таблицу Некоторые типы физиологических рецепторов и рецепторов лекарственных препаратов Влияние возраста на особенности клинических эффектов некоторых лекарственных препаратов Фармакодинамика определяет заданную эффективность лекарственного препарата в организме и реакцию организма на воздействие лекарственного препарата; эти эффекты обусловлены рецепторными связями. Прочитайте дополнительные сведения ). Активированные рецепторы прямо или косвенно регулируют клеточные биохимические процессы (например, проводимость ионных каналов, фосфорилирование белков, транскрипцию ДНК, ферментативную активность).
Молекулы (к примеру, лекарственные препараты, гормоны, нейротрансмиттеры), которые связываются с рецептором, называются лигандами. Связывание может быть специфическим и обратимым. Связывание с лигандом может приводить к активации либо инактивации рецептора; активация может стимулировать либо ингибировать ту или иную клеточную функцию. Каждый лиганд способен взаимодействовать с различными подтипами рецепторов. Почти не существует препаратов, абсолютно специфичных к одному рецептору или его подтипу, но большинство из них имеет относительную селективность. Селективность – это степень, с которой лекарственное средство действует на определенный участок относительно других участков; селективность относится в основном к физико-химическому связыванию препарата с клеточными рецепторами.
Способность лекарственного препарата воздействовать на конкретный тип рецептора зависит от его аффинности (вероятности того, что ЛС займет рецептор в определенный момент времени) и внутренней активности (степени активации рецептора после связывания с лигандом и развития клеточной реакции). Аффинность и внутренняя активность лекарственного вещества в свою очередь определяются его химической структурой.
Фармакологический эффект определяется также длительностью сохранения комплекса «препарат-рецептор» (время удержания). На продолжительность существования комплекса «препарат-рецептор» влияют динамические процессы (изменения конформации), которые контролируют скорость ассоциации и диссоциации лекарственных веществ от своей мишени. Большее время удержания служит объяснением продолжительному фармакологическому действию. К препаратам с длительным временем удержания относятся финастерид и дарунавир. Длительное время удержания может быть потенциальным недостатком, если за этот счет продлевается и токсический эффект препарата. Для некоторых рецепторов транзиторное связывание производит нужный фармакологический эффект, в то время как длительное связывание провоцирует токсичность.
Физиологические функции (такие как сокращение, секреция), как правило, регулируются множественными рецептор-опосредованными механизмами и включают несколько этапов (связывание с рецептором, активация внутриклеточных вторичных мессенджеров и т. д.) между первоначальным взаимодействием лекарственного вещества с рецептором и конечным ответом ткани или органа. По этой причине один и тот же желаемый фармакологический эффект может быть достигнут применением ЛС с разной химической структурой.
Лиганды связываются с определенными участками на макромолекуле рецептора, называемыми сайтами узнавания. Места связывания лекарственного вещества и эндогенного агониста (гормона или нейротрансмиттера) могут быть идентичными либо различаться. Агонисты, связывающиеся со смежным или другим сайтом, иногда называются аллостерическими агонистами. Также происходит неспецифическое связывание препаратов, т.е. с молекулярными участками, не являющимися рецепторами (например, белками плазмы крови). Связывание лекарственного вещества с подобными неспецифическими участками, например, связывание с белками сыворотки крови, препятствует его связыванию с рецептором, тем самым делая препарат неактивным. Несвязанные препараты способны взаимодействовать с рецепторами и, следовательно, вызывать эффект.
Агонисты и антагонисты
Антагонисты препятствуют активации рецептора. Предотвращение активации оказывает множество эффектов. Антагонисты усиливают клеточную функцию в том случае, если они блокируют действие вещества, обычно подавляющего данную функцию. Справедлива и обратная закомерность: антагонисты снижают клеточную функцию, если блокируют действие вещества, усиливающего ее.
Антагонисты рецепторов могут быть классифицированы на обратимые и необратимые. Обратимые антагонисты легко диссоциируют от соответствующих рецепторов, необратимые – образуют стабильную, постоянную или почти постоянную химическую связь со своим рецептором (например, при алкилировании). Псевдообратимые антагонисты медленно разрывают связь со своим рецептором.
При конкурентном антагонизме связывание антагониста с рецептором препятствует связыванию с ним агониста.
При неконкурентном антагонизме агонист и антагонист могут связываться одновременно, но связывание антагониста снижает эффект агониста либо препятствует его развитию.
Такие лекарственные вещества называются частичными агонистами или агонистами-антагонистами. Структурные аналоги молекул агониста часто обладают одновременно свойствами агониста и антагониста. Например, пентазоцин активирует опиоидные рецепторы, но блокирует их активацию другими опиоидами. Таким образом, пентазоцин обеспечивает опиоидное действие, но ослабляет эффект другого опиоида, если последний вводится в период сохранения связи пентазоцина с рецептором. Лекарственное средство, действующее как частичный агонист в одной ткани, может действовать как полный агонист в другой.
Виды фармакологического действия ЛС (часть 2)
Избирательное (селективное) действие лекарственных веществ обусловлено их сродством (аффинитетом) к отдельным подтипам рецепторов или селективным изменением транспорта ионов (Na+, K+, Ca2+, Cl-) в определенном органе, что зависит от химической структуры биологически активного вещества, наличием в его структуре определенных функциональных групп.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Например, сердечные гликозиды избирательно влияют на сердечную мышцу; Окситоцин – на гладкую мускулатуру матки; Сальбутамол (Вентолин) избирательно стимулирует b2-адренорецепторы бронхов и матки; Метопролол (Беталок ЗОК) селективно блокирует b1-адренорецепторы сердца. Антидиарейное средство Лоперамид (Имодиум) – селективный агонист опиоидных рецепторов кишечника. Он на длительный период замедляет перистальтику ЖКТ, устраняет понос и нормализует нормальный стул пациента. Препарат не оказывает влияния на подтипы опиоидных рецепторов ЦНС, поэтому при повторном применении не вызывает привыкания и лекарственной зависимости.
Неизбирательным (неселективным) действием обладают ЛС, воздействующие на многие рецепторы одновременно. Например, такое действие оказывает гормон мозгового слоя надпочечников – адреналин, как ЛС является адреномиметиком, связывается с α, β-адренергическими рецепторами. Антихолинергические средства (атропин, платифиллин) блокируют неизбирательно все мускариночувствительные М1, М2, М3-холинорецепторы.
Преимущественное действие – когда один и тот же препарат, действуя на различные рецепторы, обладает более выраженным фармакологическим эффектом на один из рецепторов. Например, орципреналина сульфат (Алупент, Астмопент), воздействуя на β1β2 адренорецепторы, вызывает более выраженный эффект на β2-адренорецепторы бронхов, поэтому в клинической практике его используют как бронхорасширяющее средство.
Иногда трудно определить, на какой конкретно орган действует то или иное лекарственное средство, тогда говорят об общем действии на организм или о неспецифическом действии. Такие препараты вызывают широкий спектр фармакологических эффектов и влияют на различные биохимические процессы в организме. При воздействии ЛС на конкретные отделы головного, спинного мозга, обеспечивающим адекватную ответную реакцию организма, говорят о центральном действии. Влияние ЛС на функции внутренних органов рассматривают как периферическое действие.
Общее действие развивается при применении лекарств, оказывающих фармакологический эффект одновременно на весь организм (в целом). Общим действием обладают общетонизирующие ЛС, адаптогены, такие как женьшень, элеутерококк, заманиха. Действующие вещества этих растений приспосабливают организм к изменившейся внешней или внутренней среде. При применении этих препаратов в осенне-весенний период повышается общий тонус, работоспособность, снимается умственная и физическая усталость, переутомление, общая слабость организма. Таким же общим действием обладают поливитаминные препараты, содержащие комплекс витаминов, макро- и микроэлементов. Наркозные средства или общие анестетики – Ксенон, Кетамин – обладают общим обратимым угнетающим действием на большинство клеток в ЦНС и этот эффект распространяется и на периферические органы.
Центральное действие оказывают лекарственные средства, действие которых направлено на различные отделы центральной нервной системы (ЦНС). Действие на ЦНС развивается только после прохождения лекарств через гематоэнцефалический барьер. Это сложный липидный барьер между кровью, нейроглиальными клетками, эндотелиальными клетками капилляров сосудов мозга, оболочками базальной мембраны, интерстициальной жидкостью мозга. К ЛС, воздействующим на ЦНС, относятся следующие группы – «Противопаркинсонические ЛС», «Противосудорожные (противоэпилептические) ЛС», «Наркотические анальгетики», «Снотворные средства». Центральным действием обладают психотропные средства, оказывающие влияние на психическую деятельность человека, – «Антипсихотические», «Анксиолитические», «Психостимуляторы», «Антидепрессанты» и др.
Периферическое действие развивается при действии лекарств непосредственно на периферические органы и ткани: печень, почки, сердце, сосуды, органы дыхания или при влиянии на эфферентные нервные окончания, иннервирующие внутренние органы и скелетную мускулатуру. Периферическим действием обладают диуретики, маточные, кардиотонические, гепатопротекторы, холинергические, адренергические средства и др.
Местное нежелательное действие проявляется при прямом контакте ЛС с кожей, подкожной жировой клетчаткой, слизистыми оболочками. Такое действие могут оказать препараты, обладающие раздражающим действием. Так, многие противогистаминные средства (например, Диазолин) оказывают раздражающее действие при введении внутрь, для устранения которого их выпускают в драже или таблетках, покрытых оболочкой.
Ульцерогенное действие проявляется раздражением и эрозивными поражениями слизистой оболочки, уменьшением выработки защитного слоя (муцина, слизи), защитных факторов (бикарбонатов, ПГЕ1) и повышением проницаемости эпителиальных клеток для Н+-ионов. Эрозивно-язвенные поражения ЖКТ и кровотечения возникают при приеме лекарств из групп «Глюкокортикостероиды» (ГКС) и «Нестероидные противовоспалительные средства» (НПВС). Например, при длительном применении больших доз ацетилсалициловой кислоты, основным проявлением побочного действия является ульцерогенное, включающее раздражение, изъязвление ЖКТ, возможно с кровотечением, – это отрицательный нежелательный эффект. Другие виды его фармакологического действия – анальгезирующий, жаропонижающий – являются побочными положительными, проявляющимися на фоне его основного противовоспалительного эффекта действия.
Рефлекторное нежелательное действие является следствием выраженного местного эффекта (раздражающего влияния) и сводится к торможению функций органа или системы органов, на которые оказывается основное действие. Например, рефлекторная остановка сердца и дыхания возможна при вдыхании больших концентраций эфира для наркоза.
Дисбактериоз – нарушение подвижного равновесия состава естественной микрофлоры, в норме заселяющей слизистые оболочки ЖКТ или влагалища. Это клинико-лабораторный синдром, сопутствующий острым и хроническим заболеваниям органов пищеварения, возникающий на фоне длительной антибактериальной терапии, хронического употребления алкоголя, нарушения питания, проживания в неблагоприятных условиях. Наблюдаются качественные и количественные изменения состава микробных ассоциаций, нарушается антагонистическая активность микрофлоры, начинают активно развиваться условно-патогенные и патогенные микроорганизмы.