чем обрабатывать высыпания при опоясывающем герпесе
Что такое опоясывающий герпес (опоясывающий лишай)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
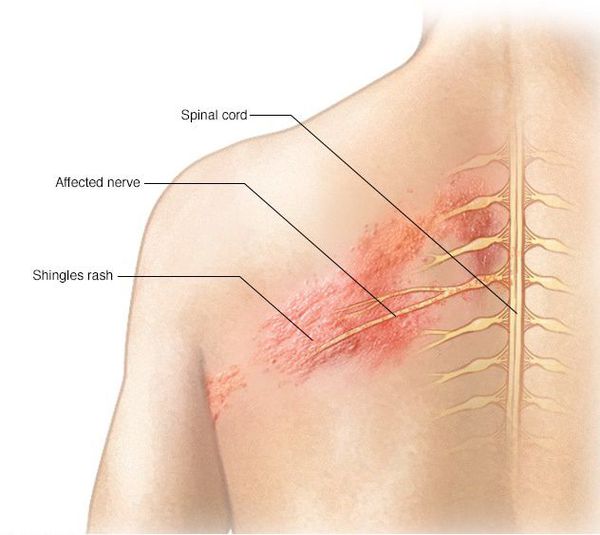
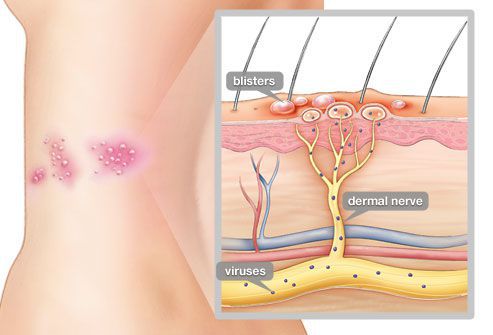
Опоясывающий герпес (опоясывающий лишай) — это инфекционное заболевание, которое возникает у людей, переболевших ветряной оспой. Его вызывает вирус Varicella zoster (вирус ветряной оспы), который активизируется из латентного состояния и поражает задние корешки спинного мозга, межпозвоночные нервные узлы (ганглии) и кожу.
Клинически характеризуется умеренно выраженным синдромом общей инфекционной интоксикации, везикулёзной сыпью по ходу чувствительных нервов, вовлечённых в процесс, и выраженными болями.
Этиология
Семейство — Herpesviridae (от греч. herpes — ползучий)
Вид — вирус герпеса 3 типа — Varicella zoster (VZV, HHV-3).
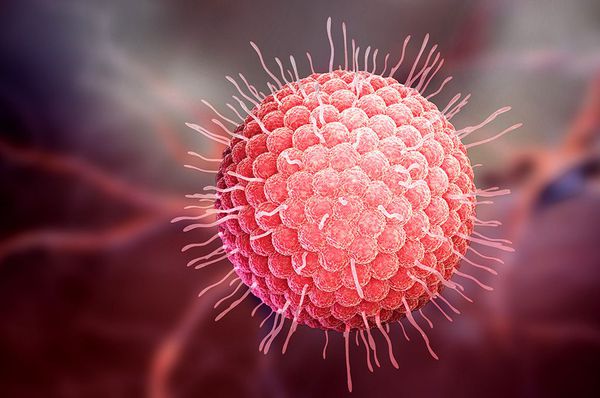
Varicella zoster — ДНК-содержащий клеточно-ассоциированный вирус овальной формы. В диаметре он достигает 120-179 нм. Покрыт липидной оболочкой с гликопротеиновыми шипиками. Имеет антигены как снаружи, так и внутри (сердцевинные антигены). Их количество и качество непостоянно. Других вариантов патогена не найдено.
После того, как человек перенёс ветряную оспу, вирус ретроградным обратным путём перемещается по отросткам нервных клеток (аксонам) к ганглиям. Там он пожизненно сохраняется в латентном состоянии. Антигены вируса на поверхности инфицированных нейронов отсутствуют. Это не позволяет иммунной системе распознать данные клетки.
Эпидемиология
Заболеванию подвержены люди, которые перенесли ветряную оспу (как правило, давно) при снижении иммунореактивности организма. К ним относятся пожилые, беременные, ВИЧ-инфицированные, люди после стресса или трансплантации органов — получающие иммуносупрессивную терапию (подавление нежелательных реакций иммунной системы) и другие иммунодепрессированные контингенты.
Так как заболевание развивается из-за реактивации вируса, уже находящегося в организме, опоясывающий герпес называют эндогенной болезнью.
Заболевание не носит массовый характер. У него нет чёткой сезонности. Чуть чаще болеют женщины и представители белой расы.
Люди с опоясывающим герпесом являются источником распространения вируса и могут быть опасны в плане заражения ветряной оспой у ранее не болевших людей, особенно детей.
В среднем заболеваемость находится на уровне 10-12 случаев на 1000 человек старше 60 лет. В последнее десятилетие наблюдается рост заболеваемости в более младших возрастных группах.
Симптомы опоясывающего герпеса
Инкубационный период в привычном понимании отсутствует, так как опоясывающий герпес — это не первичная инфекция. Может пройти вся жизнь, а манифестация так и наступит, хотя вирус в организме присутствует.
Предугадать развитие болезни сложно. Её начало и проявления широко различаются и зависят от степени тяжести. Заболеванию может предшествовать стресс, травма или ОРЗ.
Выделяют симптоматику отдельных форм опоясывающего лишая.
Ганглиокожная форма
Эта форма начинается с продромы — лёгкое недомогание, нарушения чувствительности, умеренные болевые ощущения в местах будущих высыпаний. Этот период длится до семи дней. Затем боли становятся выраженными, появляется лихорадка, умеренно выраженный синдром общей инфекционной интоксикации. Иногда боли усиливаются даже при дуновении ветра (т.н. аллодинические боли — от неболевых раздражителей).
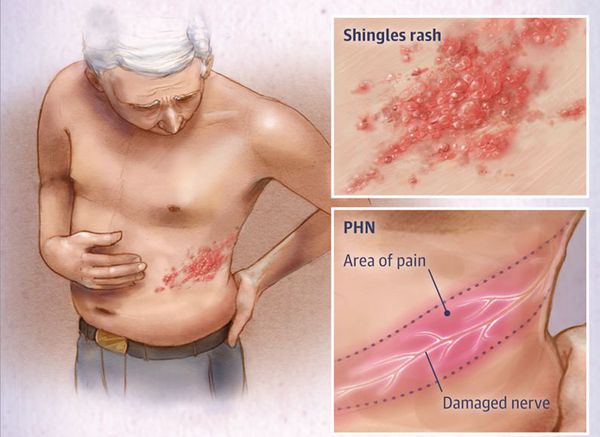
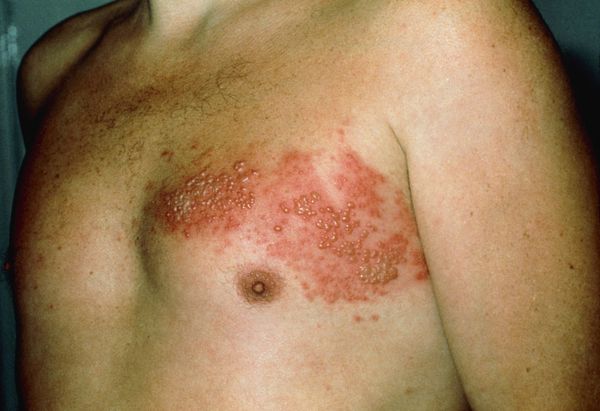
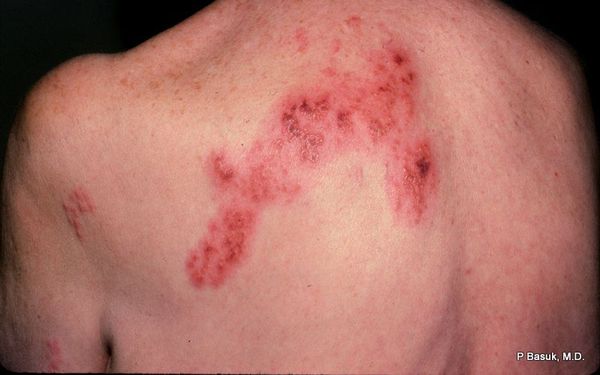
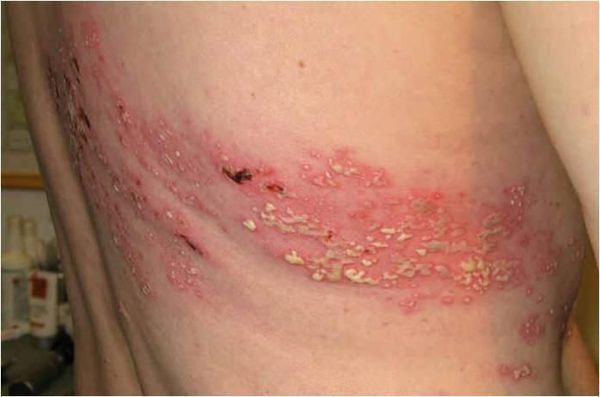
Через 3-10 дней в этих местах на фоне покраснения появляется везикулёзная сыпь. При этом интенсивность боли обычно снижается. Сыпь возникает с одной стороны, ограниченная областью иннервации одного сенсорного ганглия. Везикулы имеют тенденцию к группировке.
В дальнейшем содержимое везикул мутнеет, иногда вскрывается. Через 4-5 дней от появления сыпи появляются корочки. Они исчезают на 2-4 неделе болезни.
Разрешаются в ысыпания бесследно, но только при отсутствии расчёсов и глубоких воспалительных повреждений. А вот болевые феномены могут сохраняться длительно, иногда до года. Это требует своевременной противовирусной терапии и купирования боли.
В целом боли при опоясывающем герпесе достаточно выраженные, усиливаются при движении, прикосновении (даже незначительном). Их можно расценить как острые (с продромы и до одного месяца), подострые (1-4 месяца) и хронические (более 4 месяцев – постгерпетическая невралгия – типичная нейропатическая боль). Характер болей может быть различным – постоянным и спонтанным, чаще жгучим, давящим. Иногда боли сравнивают с ударом тока. Они могут причинять значительные физические страдания больным, нарушать сон, изматывать пациента.
Локализация болей и сыпи соответствует проекции поражённых нервов.
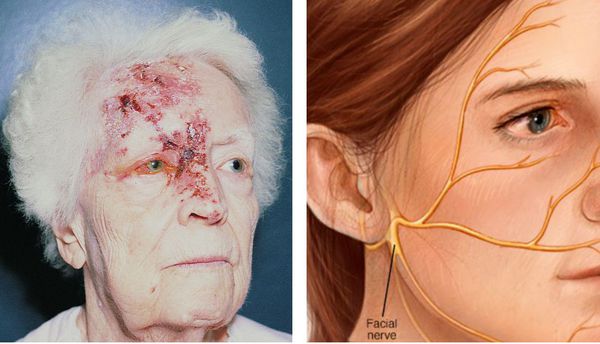
Глазная форма
Высыпания появляются на лице, носе и глазах. Это связано с поражением тройничного нерва и гассерова узла. Сыпь распространяется от уровня глаза до теменной области, резко прерывается по срединной линии лба. Иногда процесс затрагивает глаз.
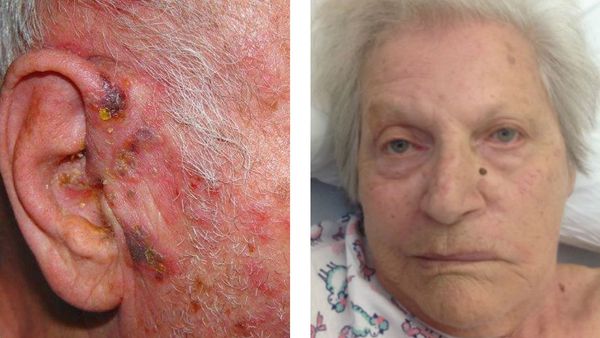
Ушная форма
Поражается коленчатый узел. При этом захватывается ушная раковина, наружный слуховой проход. Может возникнуть паралич лицевого нерва и лицевой мускулатуры — т.н. синдром Ханта. Теряется вкусовая чувствительность.
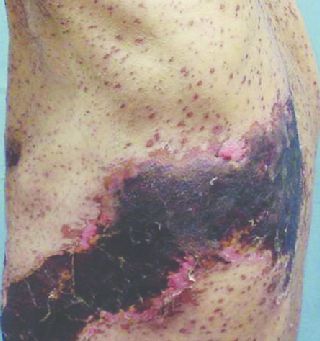
Гангренозная (некротическая) форма
Возникает глубокое поражение кожи. Формируются грубые рубцы, иногда с геморрагическим пропитыванием содержимого — геморрагическая форма. Чаще всего развивается у пожилых людей с отягощённым соматическим анамнезом — сахарным диабетом, язвенной болезнью и т. д.
Менингоэнцефалитическая форма
Чаще наблюдается при расположении сыпи на голове. Повышается температура, возникают головные боли, тошнота и рвота, не приносящая облегчения, менингеальный синдром, нарушения сознания, кома. Летальность при этом состоянии — свыше 60 %.
Диссеминированная форма
Возникает при СПИДе. Высыпания распространяются по всему кожному покрову. Часто при этом поражаются внутренние органы — лёгкие, мозг, печень, почки. Прогноз неблагоприятный.
Ганглионевралгическая форма
Характерные высыпания отсутствуют, но есть явный болевой синдром. Диагностика крайне затруднительна. Из-за очень позднего диагноза лечение сводиться лишь к купированию боли. Применение противовирусных препаратов в отсроченный период явно не влияет на процесс.
Опоясывающий герпес при беременности
Патогенез опоясывающего герпеса
Даже спустя много лет после перенесённой ветряной оспы вирус сохраняется в межпозвоночных нервных узлах и задних корешках спинного мозга. Под воздействием провоцирующего фактора (ВИЧ, стресса, приёма иммунодепрессантов, онкологии, радиации, пересадки органов и других) он активизируется и выходит из нервных клеток. Продвигаясь по аксонам чувствительных нервных стволов (чаще межрёберных, тройничного нерва) до кожного покрова, вызывает характерное поражение кожи — болезненную везикулёзную сыпь.
Такой процесс происходит у людей с наличием специфических антител класса G в низких концентрациях и сниженным уровнем клеточного иммунитета.
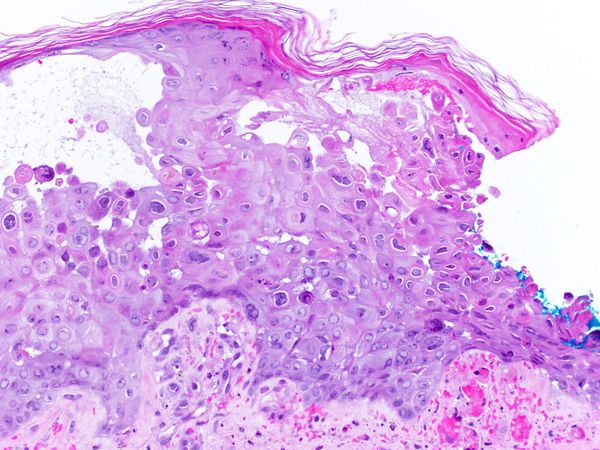
Патоморфологические изменения кожи напоминают изменения при простом герпесе:
Классификация и стадии развития опоясывающего герпеса
МКБ-10 (Международная классификация болезней) выделяет семь вариантов опоясывающего герпеса (B02):
По клинической картине выделяют две основные формы заболевания:
По степени тяжести заболевание может быть:
Осложнения опоясывающего герпеса
Диагностика опоясывающего герпеса
Лабораторная диагностика:
Дифференциальная диагностика:
Лечение опоясывающего герпеса
Пациентов с тяжёлыми формами опоясывающего герпеса необходимо госпитализировать в инфекционный стационар. Остальные больные при отсутствии серьёзных сопутствующих состояний могут лечиться на дому.
В первую очередь показан приём препаратов прямого противогерпетического действия (на основе ацикловира) в высоких дозировках. Он снижает выраженность и длительность инфекционного и постинфекционного (болевой синдром) процесса.
Начать такое лечение нужно как можно раньше — не позднее семи дней от начала болезни и трёх дней от появления сыпи.
При применении препаратов в более поздние сроки их эффективность резко снижается, так как вирус уже достиг пика своего развития и вызвал каскад иммунонейропатологических реакций.
Использование местных средств против герпеса — мазей и кремов — оказывает слабый терапевтический эффект.
Для подсушивающего, местного антисептического действия используют любой местный антисептик подобного рода — цинковые болтушки, растворы бриллиантового зелёного.
При обширных поражениях, сопровождающихся выраженной воспалительной реакцией, используются противовоспалительные средства, глюкокортикостероиды и противоаллергические препараты.
Прогноз. Профилактика
При неосложнённых и локализованных формах болезни прогноз благоприятный. При развитии ганглионевритических болей может существенно снизиться качество жизни на достаточно длительный срок (до года), а при менингоэнцефалитической и диссеминированной формах — на ещё более серьёзный срок, нередки летальные исходы.
Профилактика болезни в очаге заражения не проводится. Если опоясывающим герпесом болел ВИЧ-инфицированный пациент, то достаточно проветрить помещение.
В целях неспецифической профилактики опоясывающего герпеса нужно постараться вести здоровый образ жизни, сбалансировано и полноценно питаться, избегать стрессовых ситуаций.
В качестве специфической профилактики используются вакцины против ветряной оспы — «Варилрикс» и «Окавакс». Их можно делать как до болезни ветряной оспы (детям и неболевшим взрослым), так и после (пожилым людям с риском реактивации вируса).
Содержание
Дерматология в России
Зарегистрируйтесь!
Если Вы врач, то после регистрации на сайте Вы получите доступ к специальной информации.
Если Вы уже зарегистрированы, введите имя и пароль (форма в верхнем правом углу или здесь).
Эпидемиология, лечение и профилактика опоясывающего герпеса: комплексный обзор
Эпидемиология, лечение и профилактика опоясывающего герпеса: комплексный обзор
Вирус ветряной оспы является одним из восьми вирусов герпеса, которые являются патогенными только для человека. Он вызывает первичную инфекцию, называемую ветряной оспой, чаще всего у детей, которая очень заразна. Чаще всего он передается воздушным путем от человека к человеку или при непосредственном контакте с поражением. Во время первичной инфекции вирус распространяется через кровоток к коже, слизистой оболочке полости рта и лимфатическим узлам, вызывая генерализованную сыпь ветряной оспы. После первичной инфекции или вакцинации вирус ветряной оспы остается бездействующим в клетках ганглиев сенсорных корешков спинного мозга. Разрешение первичной инфекции вызывает индукцию Т-клеток памяти, специфичных для вируса ветряной оспы. Иммунитет Т-клеток памяти со временем снижается. Снижение ниже теоретического «порога опоясывающего лишая» коррелирует с повышенным риском инфекции опоясывающего герпеса. Иммунитет памяти к вирусу ветряной оспы может быть повышен путем экзогенного усиления (путем воздействия ветряной оспы) или эндогенного усиления (субклиническая реактивация из-за латентности). Средний период иммунитета против ветряной оспы после инфекции составляет 20 лет. Возраст, стресс, состояние с ослабленным иммунитетом и иммунодепрессанты являются известными факторами реактивации вируса. Утех, у кого развивается опоясывающий лишай рекомендуется определить ВИЧ-статус. Как только вирус реактивируется, он путешествует по пораженному чувствительному нерву, вызывает повреждение нейронов, достигает соответствующих дерматомов и образует везикулярную сыпь опоясывающего лишая. Опоясывающий герпес обычно характеризуется односторонней болезненной везикулярной сыпью, которая ограничивается одним дерматомом. Исследования показали, что более 95% взрослых инфицированы вирусом ветряной оспы и поэтому подвержены риску развития опоясывающего герпеса. После заражения опоясывающим герпесом высока вероятность повреждения периферической и центральной нервной системы, что приводит к постгерпетической невралгии. Двумя основными факторами, которые играют роль в развитии постгерпетической невралгии, являются сенсибилизация и деафференцировка. Частота вовлечения локализаций по убыванию ее следующая: грудная, поясничная и шейная, крестцовая. Повышенное распространение вируса опоясывающего герпеса за пределы изолированного дерматома ганглиозного нерва наблюдается у пациентов с дефицитом Т-лимфоцитов и макрофагальной иммунной защиты. Вовлечение легких, центральной нервной системы (ЦНС), слизистых оболочек, печени, сердечно-сосудистой системы (ССС), мочевого пузыря, скелетной системы, кровеносных сосудов и желудочно-кишечного тракта можно наблюдать среди пациентов с диссеминированными заболеваниями. Вовлечение легких, печени и ЦНС может привести к летальному исходу. Опоясывающий лишай не возникает после воздействия вируса ветряной оспы. Однако люди, пораженные опоясывающим герпесом, могут передавать вирус ветряной оспы серонегативным контактам, у которых развивается ветряная оспа, а не опоясывающий лишай. Лица, подвергшиеся воздействию опоясывающего герпеса, подвержены более низкому риску (16%) развития инфекции ветряной оспы, по сравнению с лицами, подвергшимися воздействию вируса ветряной оспы (61-100%). Передача вируса ветряной оспы от случаев опоясывающего лишая встречается чаще всего при прямом контакте с поражениями, чем воздушным путем. Было показано, что вакцинация против вируса ветряной оспы среди детей приводит к долгосрочному снижению риска у вакцинированных людей при развитии опоясывающего герпеса. Однако исследование Brisson et al. показало, что массовая детская иммунизация против вируса ветряной оспы вызвала увеличение заболеваемости опоясывающим герпесом в течение первых 30-50 лет жизни. Патогенез реактивации вируса ветряной оспы неизвестен. Но любой фактор, влияющий на клеточный иммунитет, может играть роль в реактивации вируса ветряной оспы.
Распределение по возрасту
Заболеваемость опоясывающим герпесом увеличивается с возрастом, что было подтверждено популяционным исследованием, проведенным в Корее, в котором сообщалось, что заболеваемость варьировала от 2,0 / 1000 человек в год в детской группе до 21,8 / 1000 человек в год в возрасте 70–79 лет. Пик заболеваемости опоясывающим герпесом задокументирован в возрастной группе 60–69 лет, а в возрасте старше 80 лет отмечен низкий уровень заболеваемости. Легами и др. сообщили о повышении частоты госпитализации по поводу опоясывающего герпеса среди пациентов в возрасте> 72 лет (0,46 / 1000 человек в год) по сравнению с пациентами в возрасте 15–44 лет (0,03 / 1000 человек в год), предполагая, что пожилой возраст является фактор риска опоясывающего герпеса и требует госпитализации. Согласно исследованию, проведенному в США с данными медстата marketcan, среди пожилых по сравнению с молодыми людьми было отмечено увеличение числа госпитализаций, бремени расходов, осложнений, амбулаторных посещений и рецептов на анальгетики. Постгерпетическая невралгия, бактериальные инфекции, поражение глаз, неврологическое поражение и распространенный опоясывающий лишай зарегистрированы как частые осложнения, требующие госпитализации при опоясывающем герпесе. Средняя продолжительность пребывания в стационаре для основного диагноза опоясывающего герпеса у пациентов в возрасте 50 лет и более в исследовании Stein et al. составила 6,8 дня. Тем не менее, то же самое исследование показало, что среднее время пребывания в больнице составляет 15,5 дней для пациентов с неосновным диагнозом [реабилитация, хроническая обструктивная болезнь легких (ХОБЛ), пневмония и т. д.] опоясывающего герпеса. В исследовании Ghaznawi et al., сравнивающем пациентов по возрасту в начале заболевания герпесом zoster ophthalmicus ( 250 клеток / мкл показали, что профилактика ацикловиром (400 мг два раза в день) снижает риск опоясывающего герпеса на 62%. Локализованный опоясывающий герпес у пациентов с ослабленным иммунитетом хорошо лечился местным ацикловиром. Мазь наносилась четыре раза в день в течение 10 дней. Местная терапия может помочь сократить период госпитализации, необходимый для внутривенного введения лекарств, и уменьшить побочные эффекты, связанные с внутривенным лечением. При опоясывающем герпесе у пациентов с основными злокачественными заболеваниями пероральный бривудин был столь же эффективен, как и внутривенный ацикловир. Рекомендуется 5-дневная пероральная доза 125 мг каждые 6 часов, которую можно назначать амбулаторно. Было показано, что амбулаторная терапия валацикловиром по 1-2 г три раза в день является экономически эффективной при опоясывающем герпесе у пациентов с ослабленным иммунитетом по сравнению с пациентами, получавшими ацикловир внутривенно в качестве стационарных больных. В исследовании Tyring с соавт. сравнивали эффективность фамцикловира и ацикловира при опоясывающем герпесе у 149 пациентов с ослабленным иммунитетом. Фамцикловир хорошо переносился и был рекомендован в качестве альтернативы ацикловиру. Пациент с ВИЧ, получавший валацикловир, плохо реагировал на препарат. Однако позже пациент достиг благоприятного исхода при применении внутривенного ацикловира. Для изучения эффективности валацикловира необходимы дальнейшие крупные клинические испытания. У пациентов, принимающих бортезомиб при множественной миеломе, ацикловир использовался с профилактическим средством для предотвращения опоясывающего герпеса.
Лечение постгерпетической невралгии
Противовирусные препараты являются основным средством лечения опоясывающего герпеса и снижения риска развития постгерпетической невралгии, однако, это не предотвращает постгерпетическую невралгию. Для уменьшения боли, связанной с опоясывающим герпесом, используются несколько анальгетиков, таких как ацетаминофен, НПВП, опиоиды, трициклические антидепрессанты, противосудорожные препараты и местные препараты.
Ранее в качестве первой линии в лечении постгерпетической невралгии использовались трициклические антидепрессанты. Однако позже из-за их усиленных побочных эффектов, включая антихолинергическое действие, предпочтение стали отдавать габапентину. Карбамазепин, антиконвульсант первого поколения, эффективен при лечении хронической нейропатической боли, но сообщалось о нескольких случаях синдрома Стивенса-Джонсона, вызванного карбамазепином, и токсического эпидермального некролиза, и, следовательно, он не рекомендуется. Габапентин показал хорошее влияние на сон и качество жизни пациентов. Однократная ежедневная доза гастропретенциозного габапентина в 600 мг сопровождалась быстрым уменьшением боли на 2-й день с уменьшением частоты побочных эффектов. В качестве первой линии в лечении постгерпетической невралгии часто рекомендуется прегабалин. Тем не менее, исследование Перес с соавт. не показало значительных различий в эффективности между габапентином и прегабалином. Габапентин действует путем связывания с α2δ-1-субъединицей ионно-кальциевого канала, управляемого напряжением, уменьшая их действие на ганглион дорсального корешка, ингибируя перенос мембран (от цитоплазмы к плазматической мембране) и перенос антероград (аксоплазматический транспорт). Габапентин также демонстрирует острые анальгетические эффекты, снижая высвобождение нейротрансмиттеров, таких как субстанция P. Габапентин и прегабалин следует применять с осторожностью у пациентов с почечной недостаточностью. Комбинированная терапия прегабалином и оксикодоном показала уменьшение интенсивности боли и улучшение качества жизни. Другое исследование, сравнивающее эффективность амитриптилина 25 мг и прегабалина 75 мг при лечении постгерпетической невралгии, показало лучшую эффективность прегабалина с хорошим улучшением в конце 8-й недели. 4-недельное исследование Xu с соавт. установило, что кобаламин эффективен при лечении боли и дискомфорта у пациентов с острой герпетической невралгией. Местная подкожная инъекция мекобаламина (MeB12) более безопасна и эффективна для пожилых пациентов, чем системная терапия. Внутривенное введение витамина С также показало свою эффективность при лечении боли, связанной с опоясывающим герпесом. Ранняя диагностика и лечение опоясывающего герпеса может уменьшить продолжительность опоясывающего герпеса и риск постгерпетической невралгии
Интратекальные и эпидуральные инъекции
Мощное противовоспалительное действие кортикостероидов может уменьшить повреждение нерва, тем самым предотвращая боль после герпетической невралгии. Исследования, сравнивающие интратекальный мидазолам и эпидуральный метилпреднизолон, показали пролонгированное анальгетическое действие на постгерпетическую невралгию пояснично-крестцового дерматома. Этот эффект может быть связан с антиноцицептивным действием этих препаратов на корешки спинного мозга. Исследование, проведенное на 598 пациентах старше 50 лет с острым опоясывающим герпесом, показало, что однократная эпидуральная инъекция метилпреднизолона и бупивакаина уменьшает острую зостер-ассоциированную боль в течение 1 месяца. Исследование не показало долгосрочной профилактики постгерпетической невралгии с этими препаратами. Согласно Pasqualucci с соавт., эпидуральное введение метилпреднизолона и местного анестетика (бупивакаина) предотвращает постгерпетическую невралгию через 12 месяцев, только у 1,6% пациентов отмечается боль в группе эпидурального анальгетика + стероид и 22,2% в группе ацикловир + стероид. Однако метаанализ, сравнивающий 5 клинических испытаний, показал, что кортикостероиды полезны для облегчения боли, связанной с опоясывающим герпесом, во время острой фазы инфекции и не оказывают влияния на предотвращение постгерпетической невралгии. Эпидуральные анестетики и стероиды, как было показано, уменьшают острую боль, связанную с опоясывающим герпесом, но для четкого понимания эффекта кортикостероидов в профилактике постгерпетической невралгии необходимы дополнительные исследования.
Криоаналгезия / Криотерапия межреберных нервов
Стимуляция спинного мозга
Устройство для стимуляции спинного мозга стимулирует сенсибилизированные нейроны дорсального рога, восстанавливая нарушенные возбуждающие и тормозящие функции. Техника работает только в том случае, если нет полной деафферентации или интраспинальной гибели нейронов из-за постгерпетической невралгии. Частота излечения 27–82% была отмечена при стимуляции спинного мозга с увеличением стоимости до 52 091 долл. США на пациента в течение 24 месяцев. Несколько исследований показали, что стимуляция спинного мозга является полезным вариантом для лечения постгерпетической невралгии. Временная стимуляция спинного мозга также была полезна для уменьшения подострой герпетической боли и предотвращения ее прогрессирования до хронической герпетической боли. Другое исследование из Японии показало хороший эффект временной стимуляции спинного мозга в уменьшении боли в персистирующей фазе после опоясывающего герпеса и предотвращении перехода к постгерпетическую невралгию. Временная стимуляция спинного мозга менее затратна и менее инвазивна, чем обычная стимуляция спинного мозга. Это более удобно для использования из-за отсутствия необходимости в применении МРТ. Микрохирургическое поражение дорзальной корневой зоны при стимуляции спинного мозга также является эффективным методом лечения постгерпетической невралгии. Стимуляция спинного мозга, проводимая пациентам с хронической болезнью почек с постгерпетической невралгией, также помогла справиться с болью. Глубокая стимуляция мозга контралатеральной перивентрикулярной серой области (PVG) и вентрального заднего латерального таламического ядра (VPL) была эффективна для контроля постгерпетической невралгии у 30-летнего пациента с 10-летним анамнезом правосторонней лицевой дистестии лица после опоясывающего герпеса в возрасте 20 лет. Оценка боли при последнем наблюдении через 6 месяцев была 0/10. Необходимы дополнительные исследования для подтверждения эффективности стимуляции таламуса при постгерпетической невралгии. Согласно Kolšek с соавт. чрескожная электрическая нервная стимуляция обеспечивала облегчение боли и разрешение кожных поражений с минимальными осложнениями при опоясывающем герпесе по сравнению с противовирусными средствами и рассматривалась как хорошее дополнение или даже альтернатива противовирусным препаратам при лечении острого опоясывающего герпеса и в снижении частоты возникновения постгерпетической невралгии. Чрескожная электрическая стимуляция нервов + местный метилкобаламин также показали хороший анальгетический эффект при постгерпетической невралгии.
Опоясывающий герпес может поражать любую возрастную группу с более высоким уровнем заболеваемости у пожилых пациентов и пациентов с ослабленным иммунитетом. Потребность в госпитализации и осложнения, связанные с опоясывающим герпесом, возрастают с возрастом. Необходимы дополнительные исследования для подтверждения гендерной специфики, сезонных колебаний и регионального распространения опоясывающего герпеса. Лечение противовирусными препаратами в течение 72 часов после появления сыпи показало уменьшение опоясывающего герпеса и его осложнений. Обнаружено, что фамцикловир превосходит валацикловир. Пероральный ацикловир и валацикловир предпочтительнее фамцикловира для пациентов с острым повреждением почек. Беременные женщины, дети и пациенты с ослабленным иммунитетом хорошо реагируют на ацикловир. Прегабалин и габапентин вместе с оксикодоном, инфузией витамина С и инфузией мекобаламина (MeB12) показали значительный эффект при лечении постгерпетической невралгии. Стимуляция спинного мозга эффективна в снижении и предотвращении постгерпетической невралгии, но при более высокой стоимости. Острые опоясывающие боли можно уменьшить с помощью эпидуральных анестетиков и стероидов. Необходимы дополнительные исследования эффективности криотерапии межреберных нервов и стимуляции таламуса в профилактике постгерпетической невралгии. Вакцинация против опоясывающего герпеса для людей в возрасте 60 лет и старше снижает заболеваемость, бремя болезней и заболеваемость, связанную с опоясывающим герпесом и постгерпетической невралгией. Постэкспозиционная профилактика зостер-иммуноглобулина при опоясывающем герпесе неясна. Несмотря на несколько методов лечения опоясывающего герпеса и его осложнений, лечение остается проблемой.