Болезнью грейвса что это
Диффузный токсический зоб (болезнь Грейвса, Базедова болезнь)
Аутоиммунное заболевание, обусловленное избыточной выработкой тиреоидных гормонов диффузной тканью щитовидной железы, которое приводит к отравлению организма этими гормонами — гипертиреозу (тиреотоксикозу).
Среди причин возникновения болезни Грейвса имеют значение наследственные факторы, инфекции, интоксикации, психические травмы и т.д.
Со стороны желудочно-кишечного тракта болезнь проявляется тошнотой и поносом. Сопровождающее расстройство щитовидной железы, поражение половых желез вызывает импотенцию у мужчин и нарушения менструального цикла у женщин. Болезнь Грейвса часто вызывает изменения кожных покровов, выражающиеся в повышенном потоотделении, эритемах (покраснения) и отеках.
Со стороны сердечно-сосудистой системы это нарушения ритма сердца, рост артериального давления, могущий привести к гипертонии, выраженные боли в сердечной области.
Различные офтальмопатиии (поражения глаз) также часто являются следствием расстройства функций щитовидной железы. Для больных характерна выпуклость глаз и увеличение их размеров, а также заметный отек век. Кровоснабжение глаза нарушено, что ведет к развитию различных воспалительных процессов, снижению остроты зрения, а в тяжелых случаях к потерям зрения.
Появление зоба указывает на наличие болезни Грейвса со значительной степенью вероятности, но само по себе не является однозначным указанием, так как появление зоба может быть симптомом и других заболеваний. С другой стороны, отсутствие признаков увеличения щитовидной железы делает маловероятным наличие болезни Грейвса, но не исключает его.
Как диагностируется болезнь Грейвса? Прежде всего, проводится анализ крови, позволяющий определить количество тиреоидных гормонов, вырабатываемых щитовидной железой.
Вторая часть обследования – это проведение ультразвукового исследования щитовидной железы.
Когда диагноз сомнителен, для его уточнения выполняется анализ клеток щитовидной железы. Клетки берутся с помощью тонкой иглы непосредственно из щитовидной железы под контролем УЗИ (тонкоигольная аспирационная биопсия).
Радиоизотопное исследование щитовидной железы при помощи йода также является надежным методом диагностики болезни Грейвса. При наличии заболевания наблюдается усиленное поглощение йода клетками щитовидной железы. Радиоизотопное исследование особенно часто проводится в том случае, если положение щитовидной железы является атипичным, и она не прощупывается при обычном исследовании.
Применяют медикаментозный метод (тиреостатические препараты). Основным препаратом является Мерказолил, который принимают непрерывно в течение 1,5-2 лет. Дозировку препарата подбирают строго индивидуально, которую в последующем корректируют, в зависимости от анализов крови. Необходимо каждые 10-14 дней проводить клинический анализ крови (при поддерживающей терапии мерказолилом — 1 раз в месяц).
Пациентам, у которых консервативная терапия Базедовой болезни оказалась неэффективной, рекомендуется радикальное лечение – оперативное вмешательство или лечение с использованием радиоактивного йода.
Операция проводится только при достижении состояния медикаментозной компенсации, так как в противном случае в раннем послеоперационном периоде может развиться тиреотоксический криз.
Выявление болезни на ранней стадии позволяет избежать или свести к минимуму многие осложнения, связанные с нарушением работы щитовидной железы.
Диагностика и лечение заболеваний щитовидной железы должно происходить с участием эндокринолога и хирурга в специализированном отделении.
Болезнь Грейвса
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
ММА имени И.М. Сеченова
Б олезнь Грейвса (болезнь Базедова, диффузный токсический зоб, БГ) – системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреоторопного гормона (ТТГ), клинически проявляющееся поражением щитовидной железы (ЩЖ) с развитием синдрома тиреотоксикоза в сочетании с экстратиреоидной патологией (эндокринная офтальмопатия, претибиальная микседема, акропатия). Одновременное сочетание всех компонентов системного аутоиммунного процесса встречается относительно редко и не является облигатным для постановки диагноза. В большинстве случаев наибольшее клиническое значение при БГ имеет поражение ЩЖ.
В США и Англии частота новых случаев БГ варьирует от 30 до 200 случае на 100 тысяч населения в год. Женщины заболевают БГ в 10–20 раз чаще. В регионах с нормальным йодным обеспечением болезнь Грейвса является наиболее частой причиной стойкого тиреотоксикоза, а в йододефицитных регионах в этиологической структуре токсического зоба БГ конкурирует с функциональной автономией ЩЖ (узловой и многоузловой токсический зоб). В России в качестве синонима термина болезнь Грейвса (болезнь Базедова) традиционно используется термин диффузный токсический зоб, который не лишен ряда существенных недостатков. Во–первых, он характеризует лишь макроскопическое (диффузный зоб) и функциональное (токсический) изменение ЩЖ, которое не является облигатным для болезни Грейвса: с одной стороны, увеличения железы может не быть, с другой – он может быть не диффузным. Вместе с тем, диффузное увеличение ЩЖ в сочетании с тиреотоксикозом может иметь место при других заболеваниях, в частности, при так называемой диффузной функциональной автономии. Использование более широкого термина «болезнь» (а не просто токсический зоб) применительно к обсуждаемому заболеванию, скорее всего, более оправдано, поскольку он в большей мере подчеркивает системность аутоиммунного процесса. Кроме того, во всем мире традиционно наиболее часто используется и, таким образом, узнается именно термин болезнь Грейвса, а в немецко–говорящих странах – болезнь Базедова.
БГ является мультифакториальным заболеванием, при котором генетические особенности иммунного реагирования реализуются на фоне действия факторов окружающей среды. Наряду с этнически ассоциированной генетической предрасположенностью (носительство гаплотипов HLA–B8, –DR3 и –DQA1*0501 у европейцев) в патогенезе БГ определенное значение придается психосоциальным и средовым факторам. Так, уже достаточно давно обсуждается значение инфекционных и стрессорных факторов, в частности, ряд работ выдвигает теорию «молекулярной мимикрии» между антигенами ЩЖ, ретробульбарной клетчатки и рядом стресс–протеинов и антигенов бактерий (Yersinia enterocolitica). Эмоциональные стрессорные и экзогенные факторы, такие как курение, могут способствовать реализации генетической предрасположенности к БГ. Так, была обнаружена временная взаимосвязь между манифестацией БГ и потерей супруга (партнера). Курение повышает риск развития БГ в 1,9 раз.
БГ в ряде случаев сочетается с другими аутоиммунными эндокринными заболеваниями (сахарный диабет 1 типа, первичный гипокортицизм); такое сочетание принято обозначать, как аутоиммунный полигландулярный синдром II типа.
В результате нарушения иммунологической толерантности, аутореактивные лимфоциты (CD4 + – и CD8 + –T–лимфоциты, B–лимфоциты) опосредованно адгезивными молекулами (ICAM–1, ICAM–2, E–селектин, VCAM–1, LFA–1, LFA–3, CD44) инфильтрируют паренхиму ЩЖ, где распознают ряд антигенов, которые презентируются дендридными клетками, макрофагами, В–лимфоцитами и HLA–DR–экспримирующими фолликулярными клеткам. В дальнейшем цитокины и сигнальные молекулы инициируют антигенспецифическую стимуляцию В–лимфоцитов, в результате чего начинается продукция специфических иммуноглобулинов против различных компонентов тироцитов. В патогенезе БГ основное значение придается образованию стимулирующих антител к рецептору ТТГ (АТ–рТТГ). Эти антитела связываются с рецептором ТТГ, приводят его в активное состояние, запуская внутриклеточные системы (каскады цАМФ и фосфоинозитолов), которые стимулируют захват ЩЖ йода, синтез и высвобождение тиреоидных гормонов, а также пролиферацию тироцитов. В результате развивается синдром тиреотоксикоза, доминирующий в клинической картине БГ.
Классическая мерзебургская триада (зоб, тахикардия, экзофтальм), описанная еще Карлом Базедовым, встречается примерно у 50% пациентов. Примерно в 2/3 случаев БГ развивается в возрасте после 30 лет, не менее, чем в 5 раз чаще – у женщин. В отдельных популяциях (Япония, Швеция) БГ почти в половине случаев манифестирует на протяжении первого года после родов.
Как указывалось, клиническая картина БГ определяется синдромом тиреотоксикоза, для которого характерны: похудение (часто на фоне повышенного аппетита), потливость, тахикардия и ощущение сердцебиения, внутреннее беспокойство, нервозность, дрожь рук (а порой, всего тела), общая и мышечная слабость, быстрая утомляемость и ряд других симптомов, подробно описанных в литературе. В отличие от многоузлового токсического зоба, который связан с функциональной автономией ЩЖ, при БГ, как правило, имеет место короткий анамнез: симптомы развиваются и прогрессируют быстро и в большинстве случаев приводят пациента к врачу в пределах 6–12 месяцев. У пожилых пациентов тиреотоксикоз любого генеза часто протекает олиго– или моносимптомно (вечерний субфебрилитет, аритмии) или даже атипично (анорексия, неврологическая симптоматика). При пальпаторном исследовании примерно у 80% пациентов удается выявить увеличение ЩЖ, порой весьма значительное: пальпаторно железа плотноватая, безболезненная.
В ряде случаев, при БГ на первое место могут выходить проявления эндокринной офтальмопатии (выраженный экзофтальм, нередко имеющий несимметричный характер, диплопия при взгляде в одну из сторон или вверх, слезотечение, ощущение «песка в глазах», отечность век). Здесь следует оговориться, что наличие у пациента выраженной эндокринной офтальмопатии (ЭОП) позволяет практически безошибочно установить пациенту этиологический диагноз уже по клинической картине, поскольку среди заболеваний, протекающих с тиреотоксикозом, ЭОП сочетается только с БГ.
Диагностика в типичных случаях не вызывает существенных трудностей (табл. 1). При подозрении на наличие у пациента тиреотоксикоза ему показано определение уровня ТТГ высокочувствительным методом (функциональная чувствительность не менее 0,01 мЕд/л). При обнаружении пониженного уровня ТТГ пациенту проводится определение уровня свободных Т4 и Т3: если хотя бы один из них повышен – речь идет о манифестном тиреотоксикоза, если они оба в норме – о субклиническом.
После подтверждения наличия у пациента тиреотоксикоза проводится этиологическая диагностика, направленная на выявление конкретного заболевания, которое его обусловило. При УЗИ примерно в 80% случаев БГ обнаруживается диффузное увеличение ЩЖ; кроме того, этот метод может выявить характерную для большинства аутоиммунных заболевания гипоэхогенность ЩЖ. По данным сцинтиграфии при БГ выявляется диффузное усиление захвата изотопа железой. Как и при всех других аутоиммунных заболеваниях ЩЖ, при БГ могут определяться высокие уровни классических антител к ЩЖ (антитела к тиреоидной пероксидазе – АТ–ТПО и антитела к тиреоглобулину – АТ–ТГ). Это наблюдается не менее чем в 70–80% случаев БГ. Таким образом, обнаружение классических антител не позволяет отличить БГ от хронического аутоиммунного, послеродового и «безболевого» («молчащего») тиреоидита, но может, в сумме с другими признаками, существенно помочь в дифференциальной диагностике БГ и функциональной автономии ЩЖ. Следует помнить о том, что классические антитела могут обнаруживаться у здоровых людей без каких–либо заболеваний ЩЖ. Большее диагностическое значение имеет определение уровня антител к рецептору ТТГ (АТ–рТТГ), которое, увы, пока не абсолютно из–за несовершенства имеющихся тестсистем. В таблице 2 представлена краткая характеристика других заболеваний, протекающих с тиреотоксикозом, с которыми необходимо дифференцировать БГ.
Прежде всего, планируя лечение, нужно отчетливо понимать, что при БГ речь идет об аутоиммунном заболевании, причиной которого является выработка антител к ЩЖ иммунной системой. Вопреки этому, к сожалению, очень часто приходится сталкиваться с представлением о том, что хирургическое удаление части ЩЖ само по себе способно вызвать ремиссию заболевания (т.е., по сути, аутоиммунного процесса), хотя как хирургия БГ, так и терапия радиоактивным йодом–131 идеологически должна восприниматься, лишь как удаление из организма «органа–мишени» для антител, ликвидирующее тиреотоксикоз. В настоящее время существует 3 метода лечения БГ, каждый из которых не лишен существенных недостатков.
Прежде всего, планируя лечение, нужно отчетливо понимать, что при БГ речь идет об аутоиммунном заболевании, причиной которого является выработка антител к ЩЖ иммунной системой. Вопреки этому, к сожалению, очень часто приходится сталкиваться с представлением о том, что хирургическое удаление части ЩЖ само по себе способно вызвать ремиссию заболевания (т.е., по сути, аутоиммунного процесса), хотя как хирургия БГ, так и терапия радиоактивным йодом–131 идеологически должна восприниматься, лишь как удаление из организма «органа–мишени» для антител, ликвидирующее тиреотоксикоз. В настоящее время существует 3 метода лечения БГ, каждый из которых не лишен существенных недостатков.
Консервативное лечение болезни Грейвса
Назначается для достижения эутиреоза перед оперативным лечением, а также в отдельных группах пациентов в качестве базового длительного курса лечения, который в некоторых случаях приводит к стойкой ремиссии. Длительную консервативную терапию имеет смысл планировать далеко не у всех пациентов. В первую очередь, речь идет о пациентах с умеренным увеличением объема ЩЖ (до 40 мл); при зобе больших размеров после отмены тиреостатиков неминуемо разовьется тиреотоксикоз. Кроме того, консервативную терапию нецелесообразно планировать у пациентов с крупными (более 1–1,5 см) узловыми образованиями в ЩЖ и при наличии выраженных осложнений тиреотоксикоза (мерцательная аритмия, выраженный остеопороз и др.). Практически бессмысленно (и главное – небезопасно для пациента) назначение повторных курсов лечения при развитии рецидива тиреотоксикоза спустя 12–24 месяца тиреостатической терапии. Важным условием планирования длительной тиростатической терапии является готовность пациента следовать рекомендациям врача (комплаентность) и доступность квалифицированной эндокринологической помощи.
В качестве основных тиреостатиков на протяжении многих десятилетий в клинической практике во всем мире используются препараты из группы тионамидов: тиамазол (Метизол) и пропилтиоурацил. Ключевой механизм действия тионамидов заключается в том, что, попадая в ЩЖ, они подавляют действие тиреоидной пероксидазы, ингибируют окисление йода, йодирование тиреоглобулина и конденсацию йодтирозинов. В результате прекращается синтез тиреоидных гормонов и купируется тиреотоксикоз. Наряду с этим выдвигается не всеми поддерживаемая гипотеза о том, что тионамиды, в первую очередь, тиамазол, обладают эффектами на иммунологические изменения, развивающиеся при БГ. В частности, предполагается, что тионамиды влияют на активность и количество некоторых субпопуляций лимфоцитов, снижают иммуногенность тиреоглобулина за счет уменьшения его йодирования, снижают продукцию простагландинов Е2, IL–1, IL–6 и продукцию тироцитами белков теплового шока. Именно с этим связывается тот факт, что в правильно отобранной группе пациентов с БГ, на фоне подержания тионамидами эутироза в течение 12–24 месяцев примерно в 30% случаев можно ожидать развития стойкой ремиссии заболевания.
После нормализации уровня свободного Т4 пациенту начинают снижать дозу тиреостатика и примерно через 2–3 недели переходят на прием поддерживающей дозы (10–15 мг в день). Параллельно, начиная от момента нормализации уровня Т4 или несколько позже, пациенту назначается левотироксин в дозе 50–100 мкг в день. Такая схема получила название «блокируй и замещай»: один препарат блокирует железу, другой замещает формирующийся дефицит тиреоидных гормонов. Схема «блокируй и замещай» проста в использовании, поскольку позволяет полностью заблокировать продукцию тиреоидных гормонов, что исключает возможность возвращений тиреотоксикоза. Критерием адекватности терапии является стойкое поддержание нормального уровня Т4 и ТТГ (последний может приходить в норму на протяжении нескольких месяцев от начала лечения). Вопреки бытующим представлениям тиамазол и пропилтиоурацил сами по себе не обладают так называемым «зобогенным» эффектом. Увеличение размера ЩЖ на фоне их приема закономерно развивается лишь при развитии медикаментозного гипотиреоза, которого можно легко избежать, назначив левотироксин в рамках схемы «блокируй и замещай».
Поддерживающая терапия «блокируй и замещай» (10–15 мг тиамазола и 50–100 мкг левотироксина) продолжается от 12 до максимум 24 месяцев (табл. 1). Дальнейшее увеличение объема ЩЖ на фоне проводимой терапии даже при условии стойкого поддержания эутиреоза (это закономерно произойдет при медикаментозном гипотиреозе или, наоборот, при недостаточной блокаде ЩЖ) существенно снижает шансы на успех лечения. На протяжении всего лечения у пациента с интервалом не менее чем 1 раз в месяц необходимо проводить определение уровня лейкоцитов и тромбоцитов. Редким (0,06%), но грозным осложнением тионамидов (как тиамазола, так, с практически одинаковой частотой пропилтиоурацила) является агранулоцитоз, казуистически редко – изолированная тромбоцитопения. После окончания курса лечения препараты отменяются; наиболее часто рецидив развивается в течение первого года после прекращения терапии.
По современным представлениям, целью оперативного лечения, равно как и обсуждаемой ниже терапии йодом–131, является удаление большей части ЩЖ, с одной стороны, обеспечивающее развитие послеоперационного гипотиреоза, а с другой (что наиболее принципиально) – исключающее любую возможность рецидива тиреотоксикоза. С этой целью рекомендуется проведение предельно субтотальной резекции ЩЖ с оставлением тиреоидного остатка не более 2–3 мл. Проведение субтотальных резекций, с одной стороны, несет высокий риск сохранения или отдаленного рецидива тиреотоксикоза, а с другой, отнюдь не исключает развития гипотиреоза. При выполнении так называемых «экономных резекций», объем которых во всем мире расцениваются, как неадекватный, следует понимать, что оставляя во время операции достаточную для продукции тиреоидных гормонов часть ЩЖ, в организме, по сути дела, остается «мишень» для антитиреоидных антител, продуцирующихся клетками иммунной системы.
Таким образом, полеоперационный гипотиреоз в настоящее время перестал рассматриваться, как осложнение оперативного лечения БГ, и является его целью. Предпосылкой для этого стало внедрение в широкую клиническую практику современных препаратов левотироксина, на фоне адекватного приема которых у пациента сохраняется стойкий эутиреоз и качество жизни, не отличающееся от обычного. На сегодняшний день можно без преувеличения сказать, что не существует такого гипотиреоза, компенсация которого при грамотном использовании современных препаратов тиреоидных гормонов была бы невозможна. Неудачи в лечении послеоперационного и любого другого гипотиреоза следует искать либо в недостаточной квалификации проводящего заместительную терапию, либо в несоблюдении пациентом достаточно простых рекомендаций по приему препарата.
Терапия радиоактивным йодом
Можно без преувеличения сказать, что во всем мире большая часть пациентов с БГ, равно как и с другими формами токсического зоба, в качестве лечения получает именно терапию радиоактивным йодом–131. Это связано с тем, что метод эффективен, неинвазивен, относительно дешев, лишен тех осложнений, которые могут развиться во время операции на ЩЖ. Единственными противопоказаниями к лечению йодом–131 являются беременность и грудное вскармливание.
Если в нашей стране по сей день продолжает бытовать мнение о том, что терапия йодом–131 показана лишь пожилым пациентам, которым по тем или иным причинам невозможно провести операцию, то на самом деле, уже не существует нижней возрастной границы для назначения йода–131, и во многих странах йод–131 с успехом используется для лечения БГ у детей. Было доказано, что независимо от возраста риск терапии йодом–131 существенно ниже такового при оперативном лечении.
Серьезной проблемой отечественной эндокринологии является фактическое отсутствие в распоряжении эндокринологов такого прекрасного способа лечения БГ, как терапия йодом–131.
БГ является одним из самых частых аутоиммунных заболеваний человека. Его клиническая картина и прогноз в большинстве случаев определяются стойким тиреотоксикозом, который при отсутствии адекватного лечения может привести к тяжелой инвалидизации пациента. Существующие на сегодняшний день принципы лечения БГ, хотя и не лишены недостатков, но позволяют полностью избавить пациента от тиреотоксикоза и обеспечить приемлемое качество жизни.
Тиреотоксикоз с диффузным зобом (E05.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
* термин, традиционно используемый в России и Казахстане
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
(Фадеев В.В.,Мельниченко Г.А., 2007)
Классификация зоба, рекомендованная ВОЗ (2001)
| Степень | Характеристики |
| 0 | Зоба нет (объем каждой доли не превышает объем дистальной фаланги большого пальца руки обследуемого) |
| 1 | Зоб пальпируется, но не виден при нормальном положении шеи; сюда же относят узловые образования, не приводящие к увеличению ЩЖ |
| 2 | Зоб четко виден при нормальном положении шеи |
| Степень | Характеристики |
|---|---|
| 0 | ЩЖ не пальпируется |
| I | Пальпаторно определяется увеличение перешейка ЩЖ |
| II | Пальпаторно определяются увеличенные боковые доли |
| III | Визуально определяется увеличение ЩЖ («толстая шея») |
| IV | Значительное увеличение ЩЖ (зоб ясно виден) |
| V | Зоб огромных размеров |
Патоморфологическая классификация ДТЗ
Этиология и патогенез
Эпидемиология
По данным литературы, 80-85% случаев синдрома тиреотоксикоза, диагностируемого во всем мире, вызвано диффузным токсическим зобом. В США и Англии частота новых случаев этой патологии варьирует от 30 до 200 случаев на 100 тыс. населения в год, соотношение больных женщин к мужчинам составляет 7:1.
Факторы и группы риска
Реализации генетической предрасположенности к диффузному токсическому зобу способствуют эмоциональные, стрессорные и экзогенные (курение) факторы.
Клиническая картина
Cимптомы, течение
Клиническая картина диффузного токсического зоба (ДТЗ) определяется синдромом тиреотоксикоза.
Характерные проявления тиреотоксикоза:
1. Поражение центральной и периферической нервной системы:
— возбудимость, повышенная раздражительность, плаксивость, суетливость, расстройство сна;
— тремор пальцев вытянутых рук (симптом Мари) и всего тела (симптом «телеграфного столба»);
— повышение сухожильных рефлексов;
— мышечная слабость, нарастающая при отсутствии лечения;
— в тяжелых случаях возможно развитие тиреотоксического психоза.
5. Синдром эктодермальных нарушений: ломкость ногтей, выпадение волос, горячая, бархатистая на ощупь кожа
Синдром тиреотоксикоза в 2/3 случаев развивается примерно на один год раньше ЭОП, которая у 50% больных имеет различную степень выраженности. При наличии выраженной ЭОП возможно практически безошибочно установить диагноз. Это связано стем, что уже по клинической картине среди заболеваний, протекающих с тиреотоксикозом, ЭОП сочетается преимущественно с ДТЗ.
Диагностика
Основные методы обследования
1. Анамнез: наличие аутоиммунной патологии щитовидной железы (ЩЖ) среди родственников, «короткая» история заболевания: симптомы развиваются и прогрессируют, как правило, быстро и в большинстве случаев приводят пациента к врачу через 6-12 месяцев от начала заболевания.
2. Физикальное обследование:
— определение веса, роста;
— исследование кожных покровов, волос, ногтей;
— определение АД, частоты и ритмичности пульса;
— определение тремора кончиков пальцев вытянутых рук, тела.
3. Осмотр и пальпация ЩЖ: определение размеров ШЖ, наличия пальпируемых узлов.
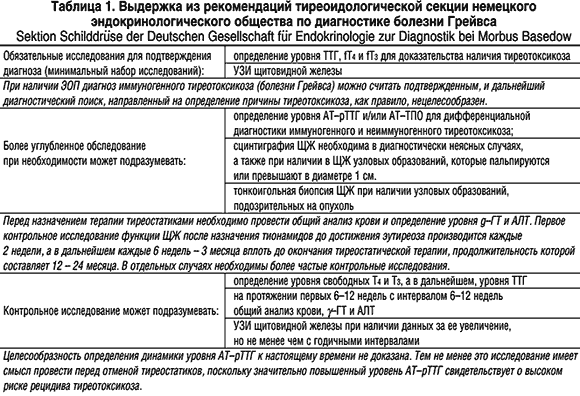
4. Офтальмологическое обследование: наличие экзофтальма, глазных симптомов, состояние глазного дна. Согласно рекомендациям тиреоидологической секции Немецкого эндокринологического общества по диагностике болезни Грейвса-Базедова, при наличии эндокринной офтальмопатии (ЭОП) диагноз иммуногенного тиреотоксикоза (диффузного токсического зоба) можно считать подтвержденным, поэтому дальнейший диагностический поиск, направленный на определение причины тиреотоксикоза, как правило, нецелесообразен.
5. УЗИ ЩЖ: диффузное увеличение объема ЩЖ, гипоэхогенность ткани, усиление ее кровотока.
6. Определение содержания ТТГ и свободного Т4 (св.Т4):
— уровень ТТГ снижен менее 0,2 МЕ/л или не определяется (подавлен);
— уровень св.Т4 повышен (при манифестной форме);
— если уровень св.Т4 определяется в пределах нормы, то показано определение св. Т3 для диагностики Т3-тиреотоксикоза.
Если содержание свободных фракций тиреоидных гормонов в пределах референсных значений, то имеет место субклинический тиреотоксикоз.
Дополнительные методы обследования (применяются по показаниям)
1. Изотопная сцинтиграфия (с 131I или 99mТс) позволяет выявить диффузное усиление захвата изотопа ЩЖ. Применяется в диагностически неясных случаях, а также при наличии в ЩЖ пальпируемых или превышающих в диаметре 1 см узловых образований.
Кормящим женщинам (при дифференциальной диагностике ДТЗ и послеродового тиреоидита) исследование проводят с изотопом 99mТс; после введения обычной дозы технеция кормление грудью безопасно для ребенка уже через 12 часов.
3. Тонкоигольная пункционная биопсия (ТАБ)
6. Общий анализ крови: возможны признаки нормоцитарной или железодефицитной анемии.
7. Биохимический анализ крови: возможно снижение уровня холестерина и триглицеридов в результате повышенного клиренса, повышение печеночных трансаминаз, ЩФ, гипергликемия, гиперкальциемия.
Лабораторная диагностика
1. Определение содержания ТТГ и свободного Т4 (св.Т4):
— уровень ТТГ снижен менее 0,2 МЕ/л или не определяется (подавлен);
— уровень св.Т4 повышен (при манифестной форме);
— если уровень св.Т4 определяется в пределах нормы, то показано определение св. Т3 для диагностики Т3-тиреотоксикоза.
Если содержание свободных фракций тиреоидных гормонов в пределах референсных значений, то имеет место субклинический тиреотоксикоз.
4. Общий анализ крови: возможны признаки нормоцитарной или железодефицитной анемии.
5. Биохимический анализ крови: возможно снижение уровня холестерина и триглицеридов в результате повышенного клиренса, повышение печеночных трансаминаз, ЩФ, гипергликемия, гиперкальциемия.
Дифференциальный диагноз
2. Хронический лимфоцитарный тиреоидит. При данном заболевании тиреотоксикоз встречается менее чем в 5% случаев и, как правило, бывает преходящим. ЩЖ может быть совсем не увеличена или очень сильно увеличена, но чаще всего имеется небольшой плотный зоб.
При пальпации ЩЖ безболезненна.
Наблюдается повышение общего T4, что связано с повреждением ткани железы.
Основные дифференциально-диагностические признаки хронического лимфоцитарного тиреоидита и ДТЗ:
На уровень тиреоидных гормонов в крови могут значительно повлиять изменения в связывании их с протеинами плазмы на фоне беременности, под влиянием некоторых медикаментов, при тяжелых нетиреоидных заболеваниях.
Наиболее частые причины сниженного уровня ТТГ в крови, не связанные с заболеваниями ЩЖ:
1.1 Тяжелые соматические заболевания.
1.2 Острый психоз. Общий T4 и свободный T4 (расчетный свободный T4) повышены почти у трети больных, госпитализированных с острым психозом. У 50% пациентов с повышенным уровнем T4 увеличен и уровень T3. Данные показатели нормализуются через 1-2 недели без лечения антитиреоидными средствами.
Предположительно повышение уровней тиреоидных гормонов вызвано выбросом ТТГ. Однако при первичном обследовании госпитализированных больных с психозом уровень ТТГ, как правило, снижен или находится на нижней границе нормы. Вероятно, уровень ТТГ может повышаться на ранней стадии психоза (до госпитализации). Действительно, у некоторых больных с пристрастием к амфетаминам, госпитализированных с острым психозом, находят недостаточное снижение уровня ТТГ на фоне повышенного уровня T4.
1.3 Высокий уровень хорионического гонадотропина (I триместр беременности, токсикоз беременных, беременность с пузырным заносом, хорионкарцинома).
У всех женщин во время беременности повышение уровня общего Т4 связано с повышением уровня ТСГ (тироксинсвязывающего глобулина) под действием избытка эстрогенов. В связи с этим для оценки функции ЩЖ во время беременности должен использоваться уровень свободного Т4 и ТТГ.
2. Лекарственные средства:
— прием высоких доз левотироксина натрия;
— лечение ГКС;
— прием бромокриптина.
Осложнения
Лечение
Цели лечения диффузного токсического зоба (ДТЗ):
1. Купирование проявлений тиреотоксикоза.
2. Нормализация лабораторных показателей уровня тиреоидных гормонов в крови.
3. Достижение иммунологической ремиссии заболевания.
Алгоритм лечения ДТЗ (Национальное руководство. Эндокринология, стр. 527)
Немедикаментозное лечение:
1. Ограничение поступления йодсодержащих препаратов (йодсодержащие контрастные вещества, витамины, содержащие йод и др.).
2. Исключение кофеина, курения, физических нагрузок.
3. Полноценное питание с достаточным количеством витаминов и микроэлементов.
4. Для восстановления нормального сна и снижения повышенной раздражительности пациента назначают седативные препараты.
Консервативная терапия
У пациентов с небольшим увеличением ЩЖ (объем менее 30 мл), при отсутствии в ней клинически значимых узловых образований, возможно проведение длительной (12-18 месяцев) консервативной терапии, которая в 30-40% случаев приводит к стойкой ремиссии заболевания.
Следует иметь в виду, при развитии рецидива заболевания после одного курса терапии тиреостатиками, назначение второго курса бесперспективно.
В медикаментозном лечении ДТЗ тиреостатиками выделяют две основные фазы.
Для предотвращения рецидивов тиреотоксикоза поддерживающие дозы тиреостатических препаратов рекомендовано применять в течение длительного времени (12-18 месяцев) без перерыва, под контролем общего анализа крови (лейкоциты и тромбоциты) 1 раза в месяц.
Начиная от момента нормализации концентрации Т4 или несколько позже, параллельно пациенту назначают левотироксин натрия в дозе 50-100 мкг/сут. Такая схема получила название «блокируй и замещай»: один препарат блокирует железу, другой замещает формирующийся дефицит тиреоидных гормонов. Поддерживающую терапию по данной схеме (10-15 мг тиамазола и 50-100 мкг левотироксина натрия) необходимо проводить от 12 до 24 месяцев.
Пациентам с высоким риском тиреотоксикоза (большой размер зоба, высокий титр антитиреоидных антител и тиреоидных гормонов при диагностике заболевания) может быть рекомендована комбинированная терапия, если по каким-либо причинам у них невозможно проведение более радикального лечения (хирургического или радиоактивным йодом).
В случае, если пациент не может регулярно контроль функции ЩЖ, ему также можно предложить данную схему лечения.
После окончания курса лечения препараты отменяют. Рецидив заболевания чаще всего развивается в течение первого года после отмены препаратов.
При лечении тиреотоксикоза по возможности следует ограничиться минимальной дозой для поддержания эутиреоидного состояния, поскольку высокие дозы тиреостатиков не снижают частоту рецидивов, но могут повышать частоту побочных реакций (аллергические реакции, гепатит, артрит, агранулоцитоз ).
Препараты йода (в дозе более чем 0,1 мг/кг массы тела) угнетают интратиреоидный транспорт йода и биосинтез тиронинов по принципу ультракороткой обратной связи, а также снижают скорость высвобождения тиреоидных гормонов в кровь.
В настоящее время их применение ограничено вследствие непродолжительного тиреостатического действия (не более 14-16 суток).
Йодиды, как правило, применяются для предоперационной подготовки больных ДТЗ в сочетании с тиреостатиками, а также в комплексе с другими лекарственными средствами для лечения тиреостатичсекого криза. Используется йод/калия йодид в дозе 3-5 капель 3 раза в сутки, 10-14 суток.
Терапия ß-адреноблокаторами
Применяется в качестве симптоматического лечения, которое направлено на ослабление симптомов тиреотоксикоза, вызванных действием катехоламинов:
— неселективные ß-блокаторы: пропраналол;
— селективные ß-блокаторы: атенолол, метопролол.
Данные препараты обладают способностью быстро смягчать симптомы тиреотоксикоза и обеспечивают быстрый положительный эффект от начала лечения, что делает их жизненно необходимыми в лечении ДТЗ.
Селективные ß-блокаторы предпочтительнее, поскольку они также уменьшают периферическую конверсию Т4 в Т3.
После достижения эутиреоза, ß-блокаторы отменяют.
Дозировка:
— атенолол внутрь 50 мг 1-2 раза/сут., до ликвидации клинических проявлений или
— метопролол внутрь 50 мг 2-3раза/сут., до ликвидации клинических проявлений или
— пропранолол внутрь 20-40 мг 3-4 раза/сут., до ликвидации клинических проявлений.
Хирургический метод
Оперативное лечение оптимально в следующих ситуациях:
— неэффективность консервативного лечения (наличие рецидивов, тяжелое течение ДТЗ);
— невозможность консервативного лечения (аллергия к антитиреоидным препаратам, агранулоцитоз и др.);
— беременность;
— детский возраст;
— большие размеры зоба с признаками сдавления близлежащих органов или узловая его форма, в том числе тиреотоксическая аденома и многоузловой токсический зоб;
— загрудинное расположение зоба.
Терапия радиоактивным йодом применяется в следующих случаях:
— рецидив тиреотоксикоза после оперативного лечения ДТЗ на фоне медикаментозного лечения;
— невозможность консервативного лечения;
— наличие выраженных сердечно-сосудистых нарушений у пациентов с небольшими размерами ЩЖ.
Сравнительная характеристика хирургического лечения и терапии радиоактивным йодом
| Хирургическое лечение | Терапия радиоактивным йодом |
| Предельно субтотальная резекция ЩЖ | Доза 150-200 гр. с расчетом активности на объем всей ЩЖ |
| Быстрая ликвидация тиреотоксикоза (несколько часов) | Ликвидация тиреотоксикоза в течение нескольких недель |
| Проводится на фоне эутиреоза, достигнутого тиреостатиками | Не требует подготовки; более дешевый метод |
| Крайне нежелательно при послеоперационном рецидиве тиреотоксикоза | Метод выбора при послеоперационном рецидиве тиреотоксикоза |
| Специфические осложнения: парез гортани и гипопаратиреоз | Абсолютное противопоказание: беременность и лактация |
| Предпочтительно при зобе большого размера | При большом размере зоба (более 60 мл) метод менее предпочтителен |
И при хирургическом лечении, и при терапии радиоактивным йодом возникающий гипотиреоз рассматривается не как осложнение, а как цель этих методов лечения. Как следствие, прием левотироксина натрия в индивидуальной дозе с заместительной целью назначается пожизненно.
После терапии радиоактивным йодом и хирургического лечения: контроль функции ЩЖ необходимо выполнять через 3 месяца, 6 месяцев, затем ежегодно.