Билиарная система что это такое простыми словами в медицине
Билиарная система что это такое простыми словами в медицине
Несмотря на то, что желчные протоки, проходя через печень, идут вдоль воротной вены, они при УЗИ обычно не видны. Внепеченочная часть билиар-ной системы состоит из правого и левого печеночных протоков, общего печеночного протока, пузырного протока, общего желчного протока и протока желчного пузыря. Правый и левый печеночные протоки, выйдя из печени, в области ворот образуют общий печеночный проток. Пузырный проток отходит от шейки желчного пузыря, после его соединения с обшим печеночным протоком образуется общий желчный проток. Общий желчный проток проходит позади двенадцатиперстной кишки к головке поджелудочной железы и открывается в нисходящей части двенадцатиперстной кишки в ампулу фатерова соска.
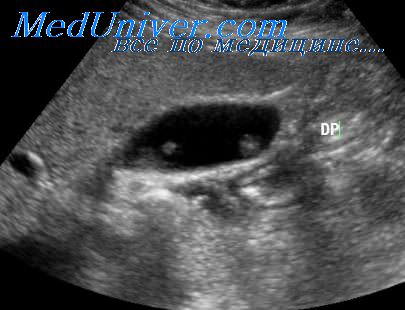
Ультрасонографический вид билиарного тракта. При обычном УЗИ неизмененные внутрипеченочные желчные протоки трудно выявить из-за слишком малых размеров. Расширенные внутрипеченочные желчные протоки, однако, выглядят как анэхогенные тубулярные структуры, прилежащие к венам воротной системы. Такой своеобразный вид обусловлен близким расположением ветвей воротной вены и желчных протоков при их прохождении в печеночной паренхиме.
При сканировании в поперечной плоскости неизмененная левая ветвь воротной вены выглядит как одиночная вертикальная тубулярная структура, напоминающая букву Т или I. При расширении внутрипеченочных желчных протоков вдоль левой ветви воротной вены можно увидеть похожую на нее тубулярную структуру. Это явление описывают как симптом параллельных каналов или признак того, что «трубок слишком много».
При УЗИ желчного пузыря врач может оценить большую часть внепеченочного билиарного тракта, за исключением нормального пузырного протока, который расположен между желчным пузырем и общим желчным протоком. Несмотря на внепеченочное расположение этого протока, у большинства пациентов он визуализируется с трудом. При сканировании в продольной плоскости общий печеночный проток выглядит как тубулярная структура, проходящая кпереди от воротной вены, он может быть легко визуализирован и измерен у большинства пациентов. Благодаря совершенствованию технологий УЗИ сегодняшние электронные датчики позволяют врачу легко увидеть неизмененный обший печеночный проток в большинстве случаев.
При измерении просвета желчного протока неодходимо всегда измерять расстояние от внутреннего края одной его стенки до внутреннего края другой, если вы хотите получить точный размер просвета протока. Поскольку общий печеночный проток располагается кпереди от воротной вены, имеющей округлое сечение с четкими контурами, он является важным ультразвуковым ориентиром при диагностическом поиске у больных с болями в правом подреберье.
При УЗИ нелегко обнаружить место, где общий печеночный проток переходит в общий желчный. Часть протока, расположенного кпереди от правой ветви воротной вены, обычно обозначают как общий печеночный проток. Общий желчный проток врачи определяют как дистальную часть тубулярной структуры, проходящую в головке поджелудочной железы. Способность визуализировать общий печеночный проток в руках опытного специалиста становится важным диагностическим инструментом. Почему? Потому, что эта тубулярная структура является классическим ориентиром для выявления дилятации внепеченочной части билиарного тракта.
Расширение гепатикохоледоха обычно наступает раньше, чем расширение внутрипеченочной части билиарного тракта, что легко обнаружить при измерении ширины этого протока. УЗИ является важным диагностическим инструментом при обследовании больных с желтухой, поскольку помогает врачу легко установить наличие билиарной гипертензии. Если при УЗИ определяется расширение общего желчного протока, необходимо установить уровень и причину обструкции. Laing с соавторами выделяют следующие уровни обструкции: панкреатический, супрапанкреатический и обструкцию в воротах печени. Расширение общего печеночного протока или более проксимальной части билиарного тракта происходит при блокаде на уровне ворот печени.
Расширение гепатикохоледоха между воротами печени и поджелудочной железой обозначается как супрапанкреатическое. Дилятация части протока, проходящей в поджелудочной железе, определяется как интрапанкреатический уровень обструкции. Наиболее часто обструкция наблюдается на уровне головки поджелудочной железы, что приводит к расширению внепеченочной части билиарного тракта. Частыми причинами дистальной обструкции являются холедохолитиаз, стриктуры протока, хронический панкреатит и злокачественные новообразования.
Первоначально сонографический вид нескольких желчных протоков, как внутри-, так и внепеченочных, может смутить врача. Расширение дистальной части билиарного тракта помогает отличить расширенные желчные протоки от ветвей воротной вены.
При сканировании в поперечной плоскости можно визуализировать только одну тубулярную структуру, входящую в ворота печени, — воротную вену. При обструкции гепатикохоледоха может визуализироваться две таких структуры, передняя из них представляет собой расширенный общий желчный проток.
Стенки расширенных внутрипеченочных протоков могут становиться неровными, приводя к образованию извилистых, по сравнению с ветвями воротной вены, структур. Нормальные внутрипеченочные протоки обычно не видны, однако при их расширении они могут визуализироваться даже в периферических отделах печени. Кзади от расширенных протоков может определяться акустическое усиление ультразвука.
Использование цветной допплерографии может помочь в дифференцировке расширенного внутрипеченочного желчного протока от расположенной рядом печеночной артерии. Те тубулярные структуры, которые будут окрашиваться, являются сосудами. Если предполагается расширение дистальной части внутрипеченочного билиарного тракта, цветовое картирование помогает поставить окончательный диагноз.
Актуальность проблемы
Дуодено-гастральный рефлюкс (ДГР) — одна из самых распространенных патологий верхних отделов желудочно-кишечного тракта, по данным разных источников, данное нарушение занимает 50-90% от всех заболеваний ЖКТ. Более того, за последние годы прослеживается рост количества заболевших. У пациентов с дуоденогастральным рефлюксом нередко также диагностируется хронический гастрит, в том числе рефлюкс-гастрит типа С, щелочной гастрит, язвенная болезнь желудка, функциональная диспепсия, грыжа пищеводного отверстия диафрагмы и ГЭРБ, пищевод Барретта, дуоденостаз, дисфункция сфинктера Одди, постхолецистэктомический синдром, рак желудка и целый ряд других заболеваний.
Следует знать, что ДГР способен привести к тяжелому гастриту и эзофагиту, стать причиной метаплазии желудка и пищевода, а также плоскоклеточного рака пищевода, который развивается на фоне метаплазии; это подтверждено клиническими исследованиями.
Таким образом, в результате патологического рефлюкса дуоденального содержимого в желудок течение многих органических и функциональных патологий ЖКТ может осложняться. Поэтому огромное значение должно уделяться своевременной диагностике, правильной клинической интерпретации и адекватной медикаментозной терапии.
При неэффективности консервативной коррекции показано хирургическое вмешательство, целью которого является укрепление пилорического жома, а также снижение количества забрасываемой желчи в желудок.
Есть данные о том, что на фоне ДГР желудка часто развиваются симптомы поражения системы дыхания, появляется синдром боли в грудной клетке, который не связан с коронарной патологией. Кроме того, у некоторых пациентов дуоденогастральный рефлюкс может вызвать рецидивирующий катаральный фарингит и пароксизмальный ларингоспазм. Однако у трети больных диагностируется «чистый» дуодено-гастральный рефлюкс, в этом случае можно говорить об изолированном диагнозе.
Причины дуодено-гастрального рефлюкса
Патогенетический механизм развития осложнений при ДГР
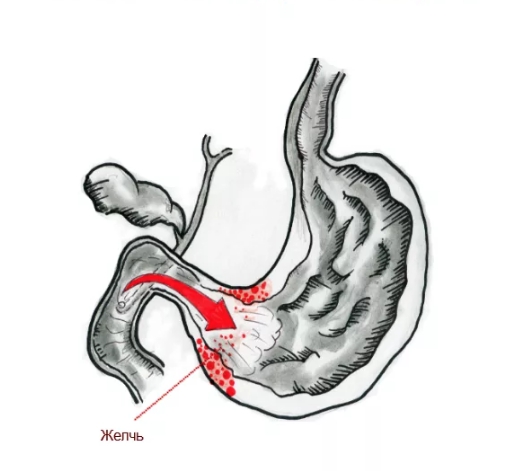
Желчь в составе рефлюксата при патологическом дуодено-гастральном рефлюксе ретроградно поступает из ДПК в органы, расположенные выше — желудок с пищеводом. Желчные кислоты, трипсин, лизолецитин — составляющие дуоденального содержимого — повреждают слизистую оболочку. Наиболее агрессивным действием при забросе дуоденального содержимого обладают желчные кислоты. Сегодня уже доказано, что при кислом рН среды лизолецитин и конъюгированные желчные кислоты (прежде всего тауриновые конъюгаты) сильнее повреждают слизистую желудка и пищевода, что определяет синергизм этих компонентов с соляной кислотой в развитии эзофагита и гастрита.
Неконъюгированные желчные кислоты и трипсин обладают более токсичным действием при слабощелочном и нейтральном рН, повреждающий эффект при дуодено-гастральном рефлюксе увеличивается при медикаментозном подавлении кислого рефлюкса. Их токсичность большей частью вызвана ионизированной формой, благодаря чему кислоты легко проникают через слизистую пищевода и желудка. Исходя из этого вполне объяснимо отсутствие адекватного ответа у 15-20% пациентов при монотерапии антисекреторными препаратами, если не будет учтен имеющийся дуодено-гастральный рефлюкс.
В результате действия на слизистую желудка желчных кислот, содержащихся в желчи, в течение длительного времени возникают изменения поверхностного эпителия желудка дистрофического и некробиотического характера, что ведет к развитию рефлюксгастрита — гастрита С. При имеющейся инфекции Нelicobacter pylori повреждающее действие рефлюксата на слизистую желудка возрастает. При наличии ДГР происходит заброс агрессивного содержимого в вышележащие отделы, что становится причиной нарушений в работе пищеварительной системы, воздействию подвергается мембранное и полостное пищеварение, возможность всасывания пищевых ингредиентов с микроэлементами и витаминами, изменяется водный баланс.
Признаком негативного воздействия ДГР являются признаки атрофии, метаплазии и дисплазии, это представляет опасность из-за риска развития рака желудка или пищевода. Кроме того, желчь в сочетании с панкреатическим соком из-за своей агрессивности разрушающе действует на слизистый барьер в желудке, при этом обратная диффузия водородных ионов усиливается. В результате этих процессов возникают эрозивные и язвенные поражения слизистой оболочки желудка.
Клинические проявления и диагностика дуодено-гастрального рефлюкса
Для ДГР характерно преобладание диспептических проявлений, пациента беспокоит отрыжка кислым содержимым или воздухом, изжога, тошнота, возможна рвота желчью, также появляется горечь во рту, которая не исчезает и даже усиливается при приеме ингибиторов протонной помпы.
Периодические боли в животе чаще схваткообразного характера, они могут возникать вследствие стресса или физической нагрузки.
Чаще дуоденогастральный рефлюкс сочетается с другими заболеваниями ЖКТ, в первую очередь с язвой желудка и ДПК, ГПОД, хроническим холециститом, панкреатитом и др. Соответственно, это отражается на симптоматике рефлюкса, существенно ее маскируя. В «чистом» виде ДГР появляется не так часто.
Дуодено-гастральный рефлюкс, в отличие от «классического» — желудочно-пищеводного рефлюкса кислой природы с изжогой, дисфагией и регургитацией — сопровождается не столь яркими клиническими проявлениями, но чаще проявляются признаки диспепсии. Кроме того, больных беспокоит боль в эпигастральной области, которая становится сильнее после приема пищи.
Диагностика основывается на результатах инструментальных методов обследования.
Лечение дуодено-гастрального рефлюкса
Консервативное лечение ДГР желудка отличается сложностью, целью терапии является нейтрализация агрессивного воздействия дуоденального содержимого на слизистую желудка и пищевода. Также в задачи лечения входит нормализация пропульсивной способности пищеварительного тракта. Назначения включают прокинетики, антациды, сорбенты, препараты урсодезоксихолевой кислоты (УДХК). При желчном рефлюксе терапия сочетается с базисным лечением основного заболевания. При этом огромное значение уделяется соблюдению диеты.
Медикаменты, используемые для устранения ДГР и восстановления моторики ЖКТ:
Следует учесть, что эритромицин в качестве прокинетика не рекомендован из-за побочных эффектов, цизаприд — не показан в клинической практике из-за вероятности нарушения сердечной проводимости, тегасерод — увеличивает вероятность инфаркта миокарда.
Фармакологическое действие домперидона (D2 антагонист) и метоклопрамида (5 НТ4 агонист и D2 антагонист) связано с блокадой рецепторов дофамина, антагонисты которых вызывают повышение тонуса нижнего сфинктера пищевода, увеличивают сократительную функцию желудка, а также препятствуют релаксации. Кроме того, благодаря антагонистам дофаминовых рецепторов улучшаются эвакуаторная способность желудка и антродуоденальная координация, что способствует устранению дуодено-гастрального рефлюкса.
Важно учесть, что клинические проявления рефлюкса с использованием медикаментозных препаратов уменьшаются, однако носят симптоматический характер. Добиться хороших результатов можно только при функциональных нарушениях, которые привели к ДГР. В остальных случаях консервативная терапия должна сочетаться с хирургическим лечением, способным устранить причину рефлюкса и укрепить пилорический клапан.
Хирургическое лечение дуодено-гастрального рефлюкса
При неэффективности консервативной терапии рекомендовано оперативное лечение, операция при этом проводится в нескольких направлениях:
При всех вышеперечисленных методиках используется лапароскопический доступ — через несколько (3-4) проколов на брюшной стенке.
Техника лапароскопической пилоропликации для уменьшения дуодено-гастрального рефлюкса
Прежде всего проводится ревизия пилородуодальной зоны, и оценивается выраженность спаечного процесса в зоне луковицы ДПК и привратника. Затем необходимо осмотреть связку Трейца, в случае необходимости она пересекается, тем самым улучшается прохождение пищи по двенадцатиперстной кишке. После ее мобилизации по Кохеру, что сделает ее более подвижной и снизит напряжение, накладываются швы в области привратника, что служит для профилактики несостоятельности.
Для пилоропликации поочередно накладываются серозно-мышечные швы симметрично к осе привратника, благодаря подобной методике передняя стенка луковицы ДПК сдвигается в проксимальном направлении, передняя полуокружность привратника погружается в просвет луковицы ДПК. Обычно четырех швов достаточно. Созданный антирефлюксный механизм способен препятствовать ДГР, не нарушая при этом эвакуации из желудка.
При необходимости проводится коррекция ГПОД или выполняется вмешательство на билиарном тракте. Следует помнить, что при лапароскопии возможно выполнение нескольких симультанных операций при наличии патологий в брюшной полости, малого таза или в забрюшинном пространстве, требующих оперативного лечения (киста почки, яичника, нефроптоз, миома и др.).
К настоящему времени нашими специалистами проведено более чем 600 оперативных вмешательств по поводу ГПОД и рефлюкс-эзофагита, а также связанных с хроническим нарушением дуоденальной проходимости. Накопленный опыт обобщен в 4-х монографиях: «Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии», «Грыжи пищеводного отверстия диафрагмы», «Ручной шов в эндоскопической хирургии» и «Технология дозированного лигирующего– электротермического воздействия на этапах лапароскопий». Кроме того, информация опубликована в многочисленных научных публикациях в разных профессиональных рецензируемых научных изданиях — российских и зарубежных.
После вмешательства на коже живота останется лишь несколько разрезов, длина которых не превышает 10 мм. Уже в день операции пациенты могут вставать, разрешается пить, на следующий день можно принимать теплую пищу в жидком виде. Клинику можно покинуть на 1-3 день — возможность выписки зависит от тяжести состояния. Но уже спустя 2-3 недели человек может вернуться к привычному образу жизни. Соблюдение строгой диеты необходимо в ближайшие два месяца, более мягкая разрешена через полгода после вмешательства. В дальнейшем человек, перенесший операцию, может обходится без медикаментов и не нуждается в строгом соблюдении диеты.
По желанию наши пациенты могут перед оперативным лечением пройти полное обследование, по результатам которого будет подобрана оптимальная тактика лечения и метод хирургического вмешательства.
На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие. Каждый день я по нескольку часов отвечаю на ваши письма. Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы. Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии.
Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи. Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами.
В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
Функциональные заболевания билиарной системы: клинические проявления, принципы лечения
Под функциональными заболеваниями билиарной системы (ФЗБС) рассматривают преимущественные нарушения моторики желчного пузыря (ЖП) и сфинктера Одди (СО). В современной классификации функциональной патологии пищеварительной системы они представлены в рубрике Е (Е1 — функциональное заболевание ЖП (ФЗЖП); Е2 — дисфункция СО (ДСО) билиарного типа и Е3 — ДСО панкреатического типа).
Частота ФЗЖП у пациентов с приступами билиарной боли при отсутствии органических изменений, по данным визуальных методик обследования, составляет до 8 и 20% у мужчин и женщин соответственно (Barbara L. et al., 1987). Распространенность ДСО в структуре причин билиарной боли несколько выше и также значительно чаще отмечается у женщин (Drossman D.A. et al., 1993). ДСО чаще наблюдают у пациентов, перенесших холецистэктомию: вероятно, удаление ЖП способствует манифестации уже существующей ДСО, что связано с повышением давления в билиарной системе, вызванным спазмом сфинктера при отсутствии ЖП (Lisbona R., 1992). Однако ДСО возникает и при интактном ЖП (Choudhry U. et al., 1993).
Моторно-эвакуаторные нарушения ЖП признают в качестве основных механизмов возникновения ФЗЖП, также возможна ассоциация с метаболическими нарушениями. У некоторых пациентов с ФЗЖП и ДСО одновременно наблюдают нарушения опорожнения желудка и кишечного транзита, что подтверждает гипотезу генерализованных нарушений моторики пищеварительного тракта (Penning C. et al., 1999).
Клинические проявления ФЗБС

При ДСО, напротив, часто наблюдают повышение уровней аланинаминотрансферазы, аспартатаминотрансферазы и щелочной фосфатазы, которые нормализуются в период между приступами. У пациентов с ДСО панкреатического типа уровни амилазы, липазы и эластазы-1 в плазме крови находятся в пределах нормы. С помощью визуальных методов исследования, как правило, выявляют расширение общего желчного протока (>8 мм в диаметре).
Несмотря на то что билиарную боль трактуют как печеночную или желчную колику, она чаще имеет постоянный, а не коликоподобный, характер. Классическое описание боли: интенсивный дискомфорт в правом верхнем квадранте живота или в области эпигастрия. Нередко боль иррадиирует в спину и сопровождается выраженным потоотделением, тошнотой, рвотой. Обычно болевой приступ, чаще умеренной интенсивности, продолжается не более 6 ч. Возможна связь симптомов с употреблением жирной пищи. Существенная доля пациентов предъявляют жалобы на ночную боль, пик которой приходится на полночь (Rigas B. et al., 1990). Довольно часто при ФЗЖП отмечают вздутие и урчание в животе (Kraag N. et al., 1995).
ФЗБС являются диагнозом исключения, поскольку течение ряда других заболеваний (желчнокаменная болезнь, пептическая язва, функциональная диспепсия, ишемическая болезнь сердца) может сопровождаться подобными симптомами.
Принципы лечения
В лечении пациентов с ФЗБС дифференцированно применяют консервативные, эндоскопические и хирургические методы в зависимости от клинической картины и результатов дополнительных исследований.
Наиболее эффективным методом лечения ФЗЖП признают холецистэктомию, которую следует выполнять лишь пациентам с наличием несомненных клинических критериев ФЗЖП и снижением пузырной фракции выброса (ПФВ) Коментарі
Алгоритм ведения пациентов с функциональными расстройствами билиарного тракта
Приведены признаки функциональных расстройств билиарного тракта (ФБР), методы обследования больных ФБР, общие подходы к лечению ФБР, включая медикаментозное, хирургическое и противорецидивное лечение.
Clinical presentations of functional disorders of biliary tract (FDB) and methods of examining patients suffering from FDB were considered, as well as general approaches to FDB treatment, including drug, surgical and anti-recurrence treatment.
Функциональные расстройства билиарного тракта (ФРБТ), или, как их еще нередко называют врачи-практики, дискинезии желчевыводящих путей, являются одним из самых распространенных видов патологии, связанным с нарушениями регулярного оттока желчи и панкреатического секрета. В экономически развитых странах ФРБТ встречается у 15–20% населения (частота встречаемости данной патологии растет по мере увеличения возраста пациентов), прогрессируя в органические заболевания [1].
В Римских критериях III пересмотра (2006 г.) ФРБТ обозначены как «Функциональные расстройства желчного пузыря и сфинктера Одди» и включают:
По мнению экспертов, участвовавших в разработке Римских критериев функциональных расстройств органов пищеварения, клиническую картину ФРБТ сложно отличить от других заболеваний желудочно-кишечного тракта (ЖКТ) — гастроэзофагеальной рефлюксной болезни, желчнокаменной болезни (ЖКБ), хронического панкреатита (ХП), функциональной диспепсии, синдрома раздраженного кишечника и других [2].
Одним из основных поводов для принятия III Римских критериев явилось общее желание специалистов избежать опасных диагностических и лечебных вмешательств, в первую очередь эндоскопической ретроградной холецистопанкреатографии (ЭРХПГ), так как в предыдущих рекомендациях эта методика, в сочетании с манометрией сфинктеров, рассматривалась как «золотой стандарт» диагностики данной патологии.
Тем не менее, несмотря на то, что в 2006 г. были определены III Римские критерии по ведению пациентов с ФРБТ, проблема верификации и лечения данной патологии продолжает оставаться актуальной.
Так, для практического применения сохраняет свою сложность вопрос о критериях диагностики ФРБТ. Согласно модифицированному авторами варианту, общими признаками для всех ФРБТ являются:
1. Боль в виде эпизодов или дискомфорт, локализованные в эпигастрии и/или в правом/левом верхнем квадранте живота (подреберьях), имеющие характеристики:
2. Боли могут сочетаться с подтверждающими симптомами:
3. Возможная сопутствующая симптоматика:
Отдельным вопросом, не до конца раскрытым в III Римских критериях, следует считать тему моторики. Так, традиционными для ФРБТ являются особенности гипер- и гипомоторных изменений, однако в последних и предыдущих рекомендациях о них не упоминается. Тем не менее, специалистам известно, что эти нарушения могут проявляться либо замедленным выделением желчи, ее застоем в желчном пузыре (ЖП) (гипомоторная дискинезия), либо, наоборот, в ускоренном выведении (гипермоторная дискинезия). Аналогична ситуация и для СО, в сократительной активности которого могут преобладать либо гипер-, либо гипомоторные расстройства. Поэтому рассмотрение индивидуальных особенностей ФРБТ следует производить с учетом моторных нарушений.
Методы обследования больных ФРБТ
Кроме жалоб, в качестве диагностических критериев при этой патологии учитывают: наличие ЖП или факт холецистэктомии, показатели печеночных трансаминаз, прямого билирубина и амилазы/липазы крови, данные ультразвукового исследования (УЗИ) брюшной полости. Последнее позволяет измерить ширину холедоха (в норме он менее 6 мм), частично исключить билиарный сладж, ЖКБ, ХП, а также оценить сократимость ЖП при выполнении динамических проб с пищевыми раздражителями.
Проведение УЗИ со стимуляцией пищей, богатой жирами, или введением холецистокинина или секретина можно рассматривать как скрининговый тест для выявления признаков дисфункции СО. Диаметр желчных протоков измеряют с интервалом в 15 мин в течение 1 часа. Расширение желчного протока после употребления жирной пищи (введения холецистокинина) на 2 мм и более указывает на нарушение эвакуации желчи, преходящее расширение панкреатического протока после введения секретина — на нарушение выведения панкреатического сока. В целом, однако, чувствительность и специфичность этой методики недостаточно высоки.
Если имеются подозрения на наличие мелких конкрементов или изменения большого дуоденального сосочка (БДС), целесообразно проведение эндоскопической ультрасонографии. Еще более прогрессивным подходом представляется эндоскопическое УЗИ со стимуляцией секретином, что позволяет выявить микролиты и опухоли в зоне сфинктера.
Для исключения микрохолелитиаза целесообразно оценивать желчь, взятую путем дуоденального зондирования, но данная методика доступна только специализированным учреждениям.
ЭРХПГ, применяемая ранее в качестве «золотого стандарта» диагностики указанной патологии, позволяет прицельно осмотреть фатеров сосочек и контрастировать протоки. Однако эта процедура сопряжена с высоким риском осложнений (острый панкреатит развивается с частотой до 24%) и имеет ряд ограничений [3].
В III Римских критериях были конкретизированы показания для проведения ЭРХПГ, которую рекомендуется выполнять в специализированных центрах, где это исследование можно дополнить при необходимости манометрии сфинктера и хирургическим вмешательством.
«Золотой стандарт» диагностики ФРСО — прямая эндоскопическая манометрия, позволяющая определить базальное давление в сфинктере (в норме не превышает 40 мм рт. ст.) и зарегистрировать периодические сокращения (в норме в это время давление в сфинктере не должно превышать 240 мм рт. ст., а частота сокращений не должна быть более 10 в минуту). При манометрии можно зафиксировать парадоксальный ответ сфинктера на холецистокинин. Наиболее важным показателем, позволяющим прогнозировать положительный эффект эндоскопической папиллосфинктеротомии (ЭПСТ), является высокое базальное давление в сфинктере.
Процедура эндоскопической манометрии технически сложна и несет риск осложнений, поэтому показания к ее проведению также необходимо строго обосновывать.
Одним из экспертных и объективных методов оценки моторики СО и ЖП является динамическая гепатобилисцинтиграфия (ДГБСГ), при проведении которой с помощью провокационных проб в виде желчегонного завтрака или внутривенного введения холецистокинина можно выявить наличие гипер- и гипомоторных изменений ЖП и СО. Так, в норме после стимуляции холецистокинином объем ЖП уменьшается на 40% и более. Однако при оценке результата необходимо учитывать влияние других факторов, в том числе особенности питания и приема препаратов, влияющих на сократимость гладкомышечных волокон.
Наиболее современным методом исследования пациентов с ФРБТ является проведение магнитно-резонансной холангиопанкреатографии, применяемой также со стимуляцией секретином. Секретин усиливает секрецию панкреатического сока и отделение желчи, что обеспечивает хорошую визуализацию протоков. Данное исследование существенно безопаснее, чем инвазивные методы.
ФРЖП — изменение сократительной активности ЖП по гипер- или гипомоторному типу, обусловленное первичными функциональными нарушениями при отсутствии, по крайней мере в начале, гиперсатурации желчи холестерином.
Диагностические критерии ФРЖП:
Подтверждающие критерии ФРЖП:
ФРСО — это расстройства моторики СО и/или панкретического сфинктера у больных, перенесших холецистэктомию, или рецидивирующие билиарные/панкреатические боли у больных с неизмененным ЖП, нормальным составом пузырной желчи и неизмененной поджелудочной железой.
Согласно накопленным данным, ФРСО представляют одну из наиболее часто встречающихся форм так называемых постхолецистэктомических расстройств, развивающихся не менее чем у 20% больных, перенесших операцию [4]. Возможно, это объясняется тем, что в условиях отсутствия ЖП функцию депонирования желчи отчасти берет на себя холедох.
В основе ФРСО лежит нарушение его сократительной активности, выражающееся в повышении базального давления и/или парадоксальных сокращениях гладкомышечных волокон. Такие изменения связывают с неадекватным ответом сфинктера на холецистокинин.
К факторам, предрасполагающим к развитию этой патологии, относят женский пол, изменения гормонального фона (предменструальный период, беременность, прием гормональных контрацептивов), сахарный диабет, стрессы, заболевания органов, связанных с механизмами желчевыведения (печень, поджелудочная железа, двенадцатиперстная кишка (ДПК)), операции на желудке и желчных путях, сопровождающиеся нарушением иннервации и изменением секреции гастроинтестинальных гормонов (холецистокинин, мотилин, секретин, гастрин).
Типичными клиническими проявлениями ФРСО служат боль «билиарного» и/или «панкреатического» типа (в зависимости от того, какая порция мышечных волокон сфинктера вовлечена в патологический процесс). Боль обычно носит приступообразный характер (схваткообразный или постепенно стихающий) различной продолжительности: от минут до нескольких часов, иногда она бывает персистирующей. Первоначально боль обычно локализуется в подложечной области с иррадиацией в левое подреберье при панкреатическом типе и в правое — при билиарном. Кроме того, боль может иррадиировать в грудную клетку и симулировать приступ стенокардии. При этом боль купируется нитроглицерином, так как препарат оказывает расслабляющее действие на гладкомышечные клетки.
Приступы боли могут развиваться через 2–3 часа после употребления жирной или жареной пищи, в части случаев провоцируются эмоциональными стрессами. Достаточно часто наблюдается развитие атак боли и в отсутствие причинных факторов, особенно в ночные часы, во сне. Такие крайние проявления, как лихорадка, озноб, желтуха, — отсутствуют.
По данным биохимического анализа крови, вскоре после приступа болей билиарного типа может быть зафиксировано более чем двукратное повышение активности печеночных трансаминаз, ЩФ, билирубина. Особенно важен факт повышения данных показателей после двух и более эпизодов болей. При приступах по типу «панкреатической» боли может отмечаться кратковременное повышение активности липазы/амилазы в крови и моче.
Диагностические критерии билиарного ФРСО:
Подтверждающие критерии билиарного ФРСО:
Диагностические критерии панкреатического ФРСО:
Подтверждающие критерии панкреатического ФРСО:
Формулировка диагноза ФРБТ
При постановке диагноза ФРБТ важны следующие характеристики:
Примеры формулировки диагноза:
Дальнейшее проведение дифференциальной диагностики при ФРБТ включает поиск других причин повышения активности АЛТ, ЩФ, ГГТП, амилазы/липазы, уровня билирубина.
Кроме того, к данной патологии относят формы, связанные со стенозом и стриктурами БДС, объединяя, таким образом, не только функциональные, но и структурные нарушения СО (табл. 1).
Как следует из данных, представленных в табл. 1, I тип ФРСО соответствует органическим изменениям и является прерогативой эндоскопических хирургов, III тип относится к чисто функциональным проявлениям и лечится терапевтами, а изменения при II типе носят промежуточный характер и могут вначале купироваться медикаментозно.
Стеноз — сужение зоны сфинктера вследствие хронического воспаления и фиброза. Распространенность этого структурного нарушения составляет 2–3%. В качестве причин воспаления, приводящего к развитию стеноза, рассматриваются холедохолитиаз, панкреатит (в том числе аутоиммунный), глютеновая энтеропатия, хирургические вмешательства в данной области, юкстапапиллярные дивертикулы ДПК. Помимо рубцового стеноза, некоторые авторы к ФБРСО относят также случаи опухолей ампулы или сосочка, так как они могут проявляться сходной симптоматикой.
Еще во II Римских критериях была определена тактика ведения пациентов после холецистэктомии, что, однако, привело к необходимости широкого проведения ЭРХПГ и разобщило понимание данной патологии хирургами и терапевтами. Для преодоления разночтений была предложена балльная оценка состояния СО по данным ДГБСГ (табл. 2).
Как следует из табл. 2, возможно проведение неинвазивной диагностики для дифференциации типов ФРБТ на основании оценки временных нарушений оттока желчи и панкреатического секрета. При визуализации протоков при этом могут определяться преходящее расширение холедоха, панкреатического протока, задержка эвакуации радиофармпрепарата в ДПК. Сумма баллов, равная 5 или более, указывает на наличие патологии. Эта система показала практически 100% чувствительность и специфичность в сравнении с «золотым стандартом» [5]. Вариант ее практического применения указан в алгоритме (приложение).
К сожалению, указанный способ оценки не нашел широкого использования специалистами, как, впрочем, и само понимание необходимости проведения ДГБСГ.
Лечение ФРБТ
Общие подходы к лечению ФРБТ состоят из разделов:
1. Улучшение реологических свойств желчи
1.1. Улучшение реологических свойств желчи с помощью диеты
В целом вопросы улучшения реологических свойств желчи лежат в разделе общепопуляционного здоровья, что предполагает проведение профилактических мероприятий путем внедрения здорового образа жизни и питания. Тема правильного питания при ФРБТ имеет важное значение, состоящее в учете влияния конкретных продуктов и блюд на моторику желчевыводящей системы и состав кишечной микрофлоры.
Кроме того, важен режим питания больного, пищу рекомендуется принимать небольшими объемами, не менее 4–5 раз в день. Из рациона обязательно исключаются жирное, жареное, копченое, острое, настои (включая алкогольные — коньяк, виски и пр.). На этапе обострения исключаются продукты, оказывающие желчегонное действие, в том числе щелочные минеральные воды.
Основа питания пациентов с ФРБТ включает продукты, способствующие желчеоттоку, и естественные пребиотики (пшеничная, овсяная и гречневая крупы, зерновой или отрубный хлеб, овощи, нежирные сорта рыбы).
1.2. Лекарственное улучшение реологических свойств желчи
В период активной клинической симптоматики, в первую очередь наличия болевого абдоминального синдрома, использование желчегонных лекарственных средств не рекомендуется [6].
При этом единственным фармакологическим средством, обладающим доказанным воздействием на реологию желчи, является урсодезоксихолиевая кислота (УДХК), терапия которой общепризнанно рассматривается основой базисного лечения всех пациентов с ФРБТ. Как было указано экспертами в III Римских критериях, УДХК, являясь гидрофильной кислотой, может иметь дополнительный терапевтический потенциал в виде уменьшения избытка холестерина в мышечных клетках ЖП у пациентов с литогенной желчью. Она также нормализует эффекты окислительного стресса, что делает применимым данное лекарственное средство при всех видах ФРБТ.
Терапию УДХК следует проводить с целью нормализации физико-химических и реологических свойств желчи, уменьшения в желчи количества микролитов, предупреждения камнеобразования и возможного растворения имеющихся мелких конкрементов. УДХК назначается в постепенно увеличивающейся дозе до 15 мг/кг массы тела. Прием осуществляется 3 раза в день за 30 минут до еды, возможен прием всей дозы однократно вечером, через час после ужина или на ночь. Длительность приема зависит от клинической ситуации, составляя примерно интервал от 3 до 24 месяцев.
При наличии болевого абдоминального и диспептического синдромов дозу УДХК следует титровать, начиная с минимальной 250 мг, через час после ужина, примерно на 7–14 дней с дальнейшим повышением на 250 мг через аналогичные временные интервалы до максимально эффективной. При этом целесообразным является терапия прикрытия, включающая параллельное применение селективных спазмолитиков, действующих прицельно на желчевыводящие пути.
2. Восстановление проходимости СО, а также сфинктеров общего панкреатического и желчного протоков, нормализация моторики ЖП, тонкой кишки
Лечебное пособие при ФРБТ, как указывалось выше, включает мероприятия по коррекции оттока из поджелудочной железы и желчевыводящих путей с помощью эндоскопии (при наличии органических изменений — рубцового стеноза СО, кальцинатов и конкрементов в протоках) и/или с помощью лекарственных препаратов.
2.1. Медикаментозные методы лечения
Средствами консервативной терапии являются препараты, оказывающие спазмолитическое и эукинетическое действие. Широко используемые в клинической практике холинолитики и спазмолитики не имеют дозозависимого эффекта и обладают низкой тропностью к желчевыводящей системе.
При дисфункции II и III типов предпочтение следует отдать лекарственным препаратам, расслабляющим гладкую мускулатуру СО. Применяют спазмолитики — блокаторы М-холинорецепторов, блокаторы кальциевых каналов (нифедипин), нитраты пролонгированного действия, а также гимекромон (синтетический аналог холецистокинина). Эти препараты снижают базальное давление в сфинктере и могут уменьшить выраженность симптомов.
Механизм действия неселективных спазмолитиков в целом сводится к ингибированию фосфодиэстеразы или активизации аденилатциклазы, блокаде аденозиновых рецепторов. Их недостатками являются существенные различия в индивидуальной эффективности, кроме того, отсутствует селективное действие на сфинктер Одди, имеют место нежелательные эффекты, обусловленные воздействием на гладкую мускулатуру сосудов, мочевыделительной системы, ЖКТ.
Антихолинергические препараты (Бускопан, Платифиллин, Метацин), блокирующие мускариновые рецепторы на постсинаптических мембранах органов-мишеней, реализуют свое действие благодаря блокаде кальциевых каналов, прекращению проникновения ионов кальция в цитоплазму гладкомышечных клеток и, как следствие, снятию мышечного спазма. При сравнительно низкой эффективности, ограничивающим их применение у данной категории пациентов фактором является широкий спектр побочных действий (сухость во рту, задержка мочеиспускания, тахикардия, нарушение аккомодации и т. д.), наиболее важным из которых является дуоденостаз.
Одновременно со спазмолитиками целесообразно назначать антисекреторные препараты для уменьшения явлений дуоденита, а в ряде случаев также психотропные препараты, однако правила выбора последних еще не определены.
2.2. Эндоскопические и хирургические методы лечения
Как указывалось выше, основная задача снижения давления в СО — обеспечение оттока желчи и панкреатического секрета в ДПК, поэтому при неэффективности медикаментозного применяют эндоскопическое и хирургическое лечение [7, 8].
Эндоскопическая папиллосфинктеротомия (ЭПСТ) в настоящее время рассматривается как стандартный метод лечения дисфункции СО при неэффективности консервативной терапии. В контролируемых исследованиях при долговременном наблюдении больных показана эффективность этого метода и низкая частота осложнений [9]. Во время вмешательства целесообразно проведение диатермического разделения билиарной и панкреатической порций сфинктера. ЭПСТ — современный стандарт лечения при I типе дискинезии и II типе с высоким базальным давлением в сфинктере, при этом эффективность вмешательства составляет более 90%. При II типе с нормальным давлением в сфинктере и III типе ЭПСТ может проводиться только при отсутствии ответа на консервативное лечение, а ее эффективность не превышает 7–55%.
Наиболее частое осложнение ЭПСТ — панкреатит (до 5% случаев), для его профилактики рекомендуется назначать препараты нитроглицерина, Дюспаталин и проводить временную установку стента [10].
Другой тип эндоскопического вмешательства — баллонное расширение и стентирование — позволяет сохранить замыкательную функцию сфинктера и добиться лишь снижения давления в нем. Однако отдаленные результаты стентирования рассматриваются как не совсем удовлетворительные [11].
Хирургический метод лечения — трансдуоденальная сфинктеропластика. В неконтролируемых исследованиях было показано, что такая процедура способствует регрессии симптомов на 1–2 года. Рандомизированных исследований, в которых бы проводилось сравнение трансдуоденальной сфинктеропластики и ЭПСТ, не проводилось.
Как альтернативный метод лечения дисфункции СО рассматривается инъекция ботулинического токсина в дуоденальный сосочек — «химическая папиллосфинктеротомия», вызывающая временное расслабление мускулатуры за счет блокады высвобождения ацетилхолина нервными окончаниями. Раздельная инъекция ботулинического токсина в билиарную или панкреатическую порцию сфинктера имеет одновременно диагностическое и лечебное значение, но в широкой клинической практике данная методика пока распространения не получила [12].
3. Нормализация процессов пищеварения и всасывания
Для решения этой задачи применяются буферные антациды и полиферментные препараты. Показанием для назначения буферных антацидов (Маалокс, Фосфалюгель) у пациентов с ФРБТ является их способность:
Буферные антациды применяются через 1,5 часа после еды и на ночь, сроком до 4 недель.
Обоснованием для назначения полиферментных лекарственных средств является:
Для коррекции указанных изменений целесообразно использовать ферментные препараты с высоким содержанием липазы, устойчивые к действию соляной кислоты, пепсина, с оптимумом действия при рН 5–7, в виде минимикросфер с максимальной поверхностью соприкосновения с химусом типа Креон 10 000–25 000 ЕД. Данные лекарственные средства применяются во время приема пищи, курсом 4–8 недель.
4. Восстановление нормального состава кишечной микрофлоры
Важным разделом в лечении ФРБТ выступает антибактериальная терапия. Вполне адекватным требованием является назначение антибиотиков в случаях выявления сопутствующих нарушений кишечного микробиоценоза [13]. Эмпирически используются производные 8-оксихинолина (ципрофлоксацин), создающие вторичную высокую концентрацию в желчевыводящих протоках, а также имипенем, цефуроксим, цефотаксим, ампиокс, азитромицин. Ограничением для применения цефтриаксона является образование билиарного сладжа при его приеме. В то же время ряд антибактериальных препаратов (тетрациклин, рифампицин, изониазид, амфотерицин) не рекомендуются к использованию ввиду токсического действия на ацинарные клетки поджелудочной железы.
Как правило, у большинства пациентов с ФРБТ выявляются различной степени выраженности нарушения кишечного микробиоценоза, существенно влияющие на течение заболевания, темпы регрессии болевого абдоминального и диспепсического синдромов. Оптимальным для его коррекции рассматривается невсасывающийся в кишечнике антибиотик рифаксимин (Альфа нормикс), который назначается 3 раза в день, в дозе 1200 мг/сут, курсом 7 дней.
Обязательным является сочетание этапа санации кишки с использованием пробиотиков (живые культуры симбионтных микроорганизмов) и пребиотиков (не содержащие живых микроорганизмов препараты, стимулирующие рост и активность симбионтной флоры кишечника). Доказанным пребиотическим действием обладает лактулоза (Дюфалак). Дюфалак является препаратом с наибольшим содержанием лактулозы и наименьшим количеством остаточных сахаров и примесей. Он относится к синтетическим дисахаридам, основной механизм действия которых связан с их метаболизмом бактериями толстой кишки до короткоцепочечных жирных кислот, выполняющих важные физиологические функции, как локальные, в толстой кишке, так и системные, на уровне целостного организма. В клинических исследованиях доказано наличие у Дюфалака выраженных пребиотических свойств, реализующихся за счет бактериальной ферментации дисахаридов и усиленного роста бифидо- и лактобактерий, а также физиологичного слабительного эффекта.
С учетом изложенных подходов лечения ФРБТ, на практике при конкретных формах предполагается их индивидуализация. Указанные схемы представлены в виде ступенчатой терапии, которая может проводиться как одновременно, так и последовательно, в зависимости от клинической ситуации (приложение).
5. Противорецидивное лечение при ФРБТ
Для предотвращения рецидивов клинической симптоматики при ФРБТ рассматривают разделы:
Профилактику нарушений реологии желчи и желчеоттока проводят с помощью диеты, УДХК, желчегонных и гидрохолеретиков. К последним относятся щелочные минеральные воды (Белинска киселка, Боржоми, Ессентуки 4, 17 и пр.) по 1 стакану, без газа, за 30 мин до еды, 3 раза в день, курсом до 1–3 месяцев, до 2–3 раза в год.
УДХК в дозе 4–15 мг/кг массы тела принимается однократно вечером. Продолжительность курса 3 месяца, 2 раза в год или постоянная поддерживающая терапия. Для профилактики абдоминальной боли возможна комбинация с Дюспаталином по 400 мг/сут, внутрь в 2 приема, за 20 мин до еды, курсом до 4–8 недель.
Желчегонные средства по механизму действия подразделяются на:
а) истинные холеретики, усиливающие секрецию желчи. К ним относятся средства, содержащие желчные кислоты (в том числе ферменты, содержащие компоненты желчи), синтетические препараты (Никодин, Оксафенамид), препараты растительного происхождения (на основе чистотела, артишока, бессмертника, шиповника, куркумы, дымянки и пр.);
б) холекинетики, которые раздражают рецепторы слизистой оболочки ДПК, вызывают выработку холецистокинина и, таким образом, стимулируют желчеотделение, сокращение ЖП и расслабление СО. К ним относятся берберина бисульфат, ксилит, сорбит, магния сульфат, циквалон, Олиметин, Холагол, гимекромон.
Как правило, желчегонные применяют по 1–2 курса в год, по 1–2 месяца, по 3–4 раза в день.
Профилактику кишечного дисбиоза проводят с помощью применения пре- и пробиотиков. Одним из оптимальных является Дюфалак по 2,5–5 мл (чайной ложке) 1 раз в день, с утра до еды, запивать стаканом жидкости, 200–500 мл на курс. Курс 1 раз в 6 месяцев.
Таким образом, несмотря на то, что III Римские критерии остаются несовершенными и не отвечают на все практические вопросы специалистов, но благодаря им унифицирована клиническая картина ФРБТ; уточнены показания для диагностических манипуляций; оптимизирована фармакотерапия, которая является универсальной для всех ФРБТ; определена хирургическая тактика.
Литература
С. Н. Мехтиев*, **, доктор медицинских наук, профессор
О. А. Мехтиева***, кандидат медицинских наук
* ООО «Поликлиника Эксперт», ** ГОУ ВПО СПбГМУ им. ак. И. П. Павлова Росздрава РФ, *** ГБОУ ВПО СЗГМУ им. И. И. Мечникова МЗ РФ, Санкт-Петербург

_575.gif)
_575.gif)
_575.gif)
_575.gif)