Бессонница при болезни паркинсона что делать
Стандарты лечения болезни Паркинсона
Лечение при появлении моторных флуктуаций и/или дискинезий
Уменьшение длительности действия средств, содержащих леводопу. При усилении симптомов паркинсонизма к концу действия очередной дозы средства, содержащего леводопу, прибегают к одной из следующих мер:
Если выбранная мера оказалась неэффективной, следует применить комбинацию препаратов (уровень С).
Замедленное наступление или отсутствие эффекта разовой дозы средства, содержащего леводопу. Если отдельные дозы препарата леводопы, принятые в течение дня, оказываются неэффективными, рекомендуют:
Непредсказуемые колебания эффекта разовой дозы средств, содержащих леводопу, в течение дня (синдром «включения-выключения»). При появлении эпизодов внезапного усиления симптомов паркинсонизма на фоне действия очередной дозы леводопы следует предпринять следующее:
Кроме того, показаны меры, аналогичные рекомендуемым, при замедленном наступлении или отсутствии эффекта разовой дозы средства, содержащего леводопу.
Насильственные движения на высоте действия разовой дозы средства, содержащего леводопу (дискинезия пика дозы). Если на высоте действия препарата леводопы появляются насильственные движения, ограничивающие жизнедеятельность пациента, нужно предпринять следующие действия:
Насильственные движения в начале и конце действия разовой дозы средства, содержащего леводопу (двухфазные дискинезии). При двухфазных дискинезиях нужно предпринять следующие меры:
Дистония, вызванная прекращением действия очередной дозы средства, содержащего леводопу. При болезненных дистониях, вызываемых прекращением действия очередной дозы средства, содержащего леводопу, необходимы следующие меры:
Если, несмотря на коррекцию схемы приема противопаркинсонических средств, сохраняются непроизвольные движения или нестабильность эффекта средств, содержащих леводопу, которые существенно ограничивают жизнедеятельность пациента (снижают трудоспособность или возможность самообслуживания), показана консультация нейрохирурга, специализирующегося в стереотаксической нейрохирургии, для решения вопроса о целесообразности нейрохирургического вмешательства.
Лечение нарушений сна
При пробуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночная акинезия), прибегают к одной из следующих мер:
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу (уровень С), а если эта мера оказывается недостаточной, то на ночь назначают клоназепам (уровень С). При неэффективности указанных мер дополнительно назначают золпидем, 10–20 мг на ночь (уровень С), антидепрессант с седативным действием (тразодон — 75–150 мг, амитриптилин — 25–50 мг или миртазапин — 15–30 мг) (уровень С).
Лечение больных БП с нарушением познавательных функций
Ухудшение познавательных функций требует в первую очередь оптимизации противопаркинсонической терапии с обеспечением адекватного уровня двигательных функций. Основным противопаркинсоническим средством у больных с выраженными познавательными нарушениями должны быть препараты, содержащие леводопу, которые у этой категории больных реже вызывают побочные эффекты (уровень С). Назначение антихолинергических средств противопоказано в связи с высоким риском ухудшения психических функций и развития психотических расстройств (уровень В).
Кроме того, при ухудшении познавательных функций необходимы:
Для улучшения познавательных функций у больных БП с деменцией могут применяться:
Консультация психиатра и наблюдение за больными с психическими нарушениями показаны при развитии тяжелых психотических расстройств (депрессии, психопатоподобные нарушения, галлюциноз, параноидный синдром, делирий).
При зрительных галлюцинациях на фоне ясного сознания, сохранности ориентации и критики проводится плановая коррекция противопаркинсонической терапии (уровень В). В первую очередь снижают дозу или отменяют недавно назначенное или наименее эффективное средство (уровень В), часто в следующем порядке: холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов — ингибитор КОМТ (уровень С).
При сохранении галлюцинаций следует снизить дозу средства, содержащего леводопу, до минимального эффективного уровня, обеспечивающего необходимый уровень двигательной активности (уровень В). При неэффективности этой меры или невозможности снизить дозу средства, содержащего леводопу, из-за нарастания двигательного дефекта назначается клозапин в дозе от 6,25 до 50 мг на ночь (уровень В); после регресса галлюциноза препарат постепенно отменяют в течение 2–3 нед (уровень С). В течение всего срока лечения клозапином необходимо 1 раз в неделю исследовать содержание лейкоцитов в крови. При снижении их уровня ниже 3 тыс./мкл препарат должен быть отменен.
При неэффективности или непереносимости клозапина вместо него может быть назначен кветиапин, 25–200 мг/сут (уровень С), ингибитор холинэстеразы (уровень С).
При сочетании зрительных галлюцинаций с бредовыми нарушениями или при их возникновении на фоне спутанности сознания с развитием делирия необходимо, помимо указанных выше мер, следующее:
Следует избегать назначения на ночь бензодиазепинов с длительным действием (диазепам, хлордиазепоксид и т. д.), способных спровоцировать спутанность сознания.
Лечение акинетического криза
Акинетический криз — внезапное стойкое усиление гипокинезии и ригидности с развитием обездвиженности и нарушения бульбарных функций (дизартрии и дисфагии), возникающее спонтанно или связанное с прекращением приема, снижением дозы средств, содержащих леводопу, нарушением их всасывания в желудочно-кишечном тракте, развитием интеркуррентной инфекции.
Лечение осуществляется в условиях стационара. Проводится исследование причин акинетического криза (прекращение приема или снижение дозы противопаркинсонических средств, заболевание желудочно-кишечного тракта, вызывающее нарушение всасывания препаратов леводопы, интеркуррентная инфекция, цереброваскулярное заболевание, декомпенсация соматического заболевания).
Лекарственная терапия назначается индивидуально на основании данных анамнеза и ежедневного осмотра пациента. При дисфагии необходимо введение назогастрального зонда для кормления и введения лекарств. Показан комплекс мер по предупреждению пролежней, прежде всего повороты в постели каждые 2 ч, регулярная обработка мест костных выступов камфорным спиртом, использование противопролежневых матрасов.
Если акинетический криз возник в результате внезапного прекращения приема средства, содержащего леводопу, то его следует назначить вновь в более низкой дозе (50–100 мг 3–4 раза в сутки), затем постепенно увеличивать дозу каждые 3 дня до получения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
Если акинетический криз возник вследствие снижения дозы, то ее следует увеличить на 100 мг каждые 3 сут до достижения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
При дисфагии (но при нормальной функции желудочно-кишечного тракта) препараты леводопы вводят в растворенном виде через зонд.
В качестве дополнительного средства, особенно при нарушении глотания и всасывания препаратов в желудочно-кишечном тракте, назначают амантадина сульфат — 200 мг/500 мл в/в капельно со скоростью 60 капель в 1 мин 1–2 раза в сутки в течение 5–10 дней (уровень С) с последующим обязательным переходом на прием амантадина внутрь (100–200 мг 3 раза в день).
При дегидратации с целью достижения эуволемии вводят физиологический раствор, раствор Рингера, 0,45% раствор хлорида натрия и 5% раствор глюкозы, раствор альбумина, Реополиглюкин (уровень С).
Для профилактики тромбоза глубоких вен голени и тромбоэмболических осложнений показано назначение прямых антикоагулянтов (Гепарин, 2,5–5 тыс. единиц подкожно 2 раза в день или Фраксипарин 0,3 мл подкожно 2 раза в сутки) до разрешения акинетического криза (уровень С).
До восстановления глотания питание проводится через назогастральный зонд. При нарушении функции желудочно-кишечного тракта проводится парентеральное питание.
При появлении дыхательной недостаточности, острой сердечной недостаточности и тяжелой дисфагии, создающей угрозу аспирации, больной переводится в отделение интенсивной терапии, где проводится интубация, а при необходимости и искусственная вентиляция легких. Реабилитация, включающая лечебную гимнастику и массаж, осуществляется после купирования криза и стабилизации состояния.
По вопросам литературы обращайтесь в редакцию.
О. С. Левин, доктор медицинских наук, профессор
РМАПО, Центр экстрапирамидных заболеваний, Москва
Бессонница при болезни паркинсона что делать
Российская медицинская академия последипломного образования; Центр экстрапирамидных заболеваний, Москва
НИИ скорой помощи им. Н.В. Склифосовского, Москва
Ночные симптомы болезни Паркинсона и подходы к их коррекции
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(12): 62-66
Кулуа Т. К., Федорова Н. В. Ночные симптомы болезни Паркинсона и подходы к их коррекции. Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(12):62-66.
Kulua T K, Fedorova N V. Nocturnal symptoms of Parkinson’s disease and approaches to their correction. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2013;113(12):62-66.
Российская медицинская академия последипломного образования; Центр экстрапирамидных заболеваний, Москва
В исследование были включены 73 пациента с болезнью Паркинсона (БП). Они были разделены на 2 группы в зависимости от наличия (53 больных) или отсутствия (20 больных) ночных симптомов заболевания. В контрольную группу вошли 10 здоровых. Наиболее часто у пациентов с ночными симптомами встречались никтурия (71,8%), аффективные нарушения (52,4%), акинезия (41,7%) и крампи (30,15%). Эти симптомы были более выраженными при акинетико-ригидной форме БП, большей тяжести и прогредиентности заболевания. При использовании для коррекции ночных симптомов сталево было отмечено его выраженное терапевтическое действие.
Российская медицинская академия последипломного образования; Центр экстрапирамидных заболеваний, Москва
НИИ скорой помощи им. Н.В. Склифосовского, Москва
Синдром беспокойных ног (СБН) характеризуется неприятными ощущениями в нижних конечностях в покое в вечернее и ночное время, вынуждающим больного совершать устраняющие их движения и приводящие к нарушению сна. СБН выявляется у 6,3-19,5% пациентов с БП [4, 18]. Нарушения сна при СБН усугубляют периодические движения конечностями (ПДК), которые возникают во сне у 80% больных с СБН во время фазы медленного сна. Преимущественно вовлекаются нижние конечности, возникают разгибание большого пальца, тыльное сгибание стопы и голени. В отличие от миоклоний, ПДК продолжаются более длительное время (от 0,5 до 5 с), могут быть односторонними и ритмично повторяются каждые 4-90 с. Отмечаются обычно в первой половине ночи, нарастают с возрастом. В легких случаях ни больные, ни их родственники не подозревают о наличии ПДК, и они могут быть выявлены только с помощью полисомнографии. В тяжелых случаях ПДК не прекращаются всю ночь и могут быть причиной частых пробуждений [3, 20, 21].
Двигательная активность во время фазы сна с быстрым движением глазных яблок (БДГ) выявляется примерно у 20% больных. Психомоторное возбуждение во сне с БДГ может проявляться сноговорением, криком, стонами, элементарными или более сложными движениями конечностей и туловища, иногда весьма активными и чреватыми опасностью травмы больного или лежащего рядом с ним родственника. Иногда симптом появляется за несколько месяцев или лет до основных моторных симптомов БП и может рассматриваться как первый признак заболевания [6, 18].
Психические расстройства также возможны на любой стадии БП, в 50-60% случаев на поздних стадиях развиваются спонтанно, но чаще бывают связаны с действием противопаркинсонических средств, при назначении нового препарата, либо при повышении дозы или изменении схемы приема ранее назначенного средства. Спектр психических расстройств, наблюдаемых при БП, весьма широк и он может включать и психотические состояния с галлюцинациями, иллюзиями, бредом и делирием. Своеобразным эквивалентом психотических расстройств являются яркие устрашающие сновидения и ночные кошмары, которые нередко предшествуют более явным психотическим нарушениям или сопровождают их.
Основными причинами развития моторных флюктуаций, в том числе ночной акинезии при БП, являются колебания концентрации леводопы в плазме крови из-за короткого периода полужизни двухкомпонентных препаратов (леводопа/ингибитор ДДК), что в свою очередь ассоциируется с пульсирующей нефизиологической стимуляцией дофаминовых рецепторов.
Фармакокинетическое исследование биодоступности однократной дозы 200 мг трехкомпонентной формы леводопы/карбидопы/энтакапона, принятой перед сном, показало, что концентрация леводопы в плазме крови была более стабильной после приема трехкомпонентного препарата, чем после приема 200 мг леводопы с постепенным высвобождением лекарственного средства [12].
Задачей настоящего исследования являлось изучение эффективности нового трехкомпонентного препарата леводопы сталево в коррекции ночных моторных симптомов заболевания при приеме однократной вечерней дозы.
Материал и методы
В Центре экстрапирамидных заболеваний были обследованы 73 пациента с БП.
В процессе исследования пациенты с БП были распределены на две группы. В основную группу вошли 53 больных БП с ночными симптомами, группу сравнения составили 20 больных БП без симптомов, проявляющихся в ночное время. Для изучения частоты и характера ночных симптомов была выбрана контрольная группа из 10 практически здоровых людей соответствующего возраста. Все три группы были сопоставимы по полу и возрасту. В группе исследования коррекция ночных симптомов БП была максимально индивидуализирована. У каждого пациента определялся спектр ночных симптомов и, в зависимости от их характера, проводилась коррекция дофаминергической терапии с использованием трехкомпонентного препарата леводопы сталево; 63 больным БП с ночными симптомами вечерний прием леводопы заменялся на сталево в дозе, эквивалентной той дозе леводопы, которую пациент принимал в составе двухкомпонентного препарата. Пациенты принимали сталево однократно перед сном на протяжении 3 мес.
Пациенты, включенные в исследование, не подвергались круглосуточному наблюдению медицинского персонала и полисомнографическому контролю во время ночного сна. Тщательный опрос пациентов, родственников, ухаживающего персонала, спящих в одной комнате с больным, а также использование современных шкал позволили получить объективные данные.
Статистический анализ проводился с использованием программного пакета Statistica 6.
Результаты и обсуждение
Наиболее частыми ночными симптомами БП у обследованных больных были никтурия (71,8%), аффективные расстройства (52,4%), акинезия (41,7%) и крампи (30,1%). Отмечалась также дневная сонливость (62,2%). Выявлена корреляция между выраженностью ночных симптомов и клинической формой БП (r= –0,4; p
Динамика выраженности нарушений сна в основной группе до и после коррекции ночных симптомов представлена в табл. 3.
Таким образом, выявлено статистически достоверное уменьшение выраженности ночных симптомов БП, в том числе нарушений сна в основной группе после их коррекции (p
У 33,1% пациентов основной группы достоверно (на 33,1%) (p
Стандарты лечения болезни Паркинсона
Статья основана на положениях «Протокола ведения пациентов с болезнью Паркинсона», разработанного группой экспертов, в которую вошли ведущие отечественные специалисты по болезни Паркинсона (БП), и утвержденного Минздравсоцразвития РФ в 2005 г. Положения Протокола основаны на анализе в соответствии с принципами доказательной медицины контролируемых исследований, проведенных в нашей стране и за рубежом [1, 2, 4–7, 9–11, 13, 15], и в целом соответствуют недавно опубликованным рекомендациям по лечению БП Европейской федерации неврологических обществ [8] и Американской академии неврологии [12, 14, 16]. Текст Протокола опубликован в журнале «Проблемы стандартизации в здравоохранении» [3]. В Протоколе используется следующая шкала убедительности доказательств данных: А — доказательства убедительны (есть веские доказательства предлагаемому утверждению), B — относительная убедительность доказательств (есть достаточно доказательств в пользу того, чтобы рекомендовать данное предложение), C — достаточных доказательств нет (имеющиеся доказательства недостаточны для вынесения рекомендаций, но они могут быть даны с учетом иных обстоятельств).
Начальный этап лечения
Общие принципы. Поскольку на данный момент нейропротекторный потенциал ни одного средства при БП убедительно не доказан, лечение основывается главным образом на симптоматическом действии противопаркинсонических средств, которые принято назначать в том случае, когда хотя бы одно из проявлений заболевания приводит к ограничению жизнедеятельности пациента.
Лечение начинается с монотерапии. Если препарат оказался неэффективным (нет регресса симптоматики в течение месяца после достижения оптимальной дозы) или плохо переносится, его заменяют средством той же или другой фармакологической группы. При выборе препарата и его дозы следует стремиться не к полному устранению симптомов, а к существенному улучшению функций, позволяющему поддерживать бытовую и профессиональную активность. При частичном эффекте (недостаточное улучшение функций) к принимаемому препарату последовательно добавляют лекарственные средства иной фармакологической группы.
Принципы выбора противопаркинсонического препарата. Выбор препарата на начальном этапе лечения проводят с учетом возраста, выраженности двигательного дефекта, трудового статуса, состояния нейропсихологических функций, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента. Помимо достижения оптимального симптоматического контроля, выбор препарата определяется необходимостью отсрочить момент развития моторных флуктуаций и дискинезий (табл.).
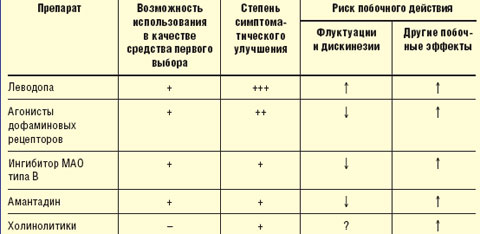 |
| Таблица Выбор препарата для начального лечения болезни Паркинсона |
У лиц моложе 50 лет при умеренной выраженности двигательных нарушений в отсутствие выраженных когнитивных нарушений назначают один из следующих препаратов: агонист дофаминовых рецепторов, ингибитор моноаминооксидазы (МАО) типа В (селегилин), амантадин, антихолинергические средства (тригексифенидил, бипериден).
Лечение предпочтительнее начинать с одного из агонистов дофаминовых рецепторов, которые хотя и не позволяют достичь того же уровня симптоматического контроля, как препараты леводопы, способны обеспечить поддержание уровня жизнедеятельности пациентов в течение длительного времени, отсрочить назначение леводопы и тем самым развитие осложнений долгосрочной терапии леводопой (уровень А). Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности, и избежать побочного действия (уровень С). Неэрголиновые агонисты (пирибедил, прамипексол) ввиду более благоприятного профиля побочных эффектов предпочтительнее, чем эрголиновые (бромокриптин).
Лечение пирибедилом начинают с дозы 50 мг 1 раз в день (днем или вечером — после основного приема пищи), в дальнейшем суточную дозу увеличивают на 50 мг 1–2 раза в неделю — до достижения необходимого эффекта, но не выше 250 мг/сут (50 мг 5 раз в день). Лечение прамипексолом начинают с дозы 0,125 мг 3 раза в день (после еды), затем еженедельно дозу последовательно увеличивают до 0,25 мг 3 раза в день, 0,5 мг 3 раза в день, при недостаточном эффекте — до 1 мг 3 раза в день и 1,5 мг 3 раза в день (максимальная доза — 4,5 мг/сут). Лечение бромокриптином начинают с дозы 2,5 мг 3 раза в день, в дальнейшем ее еженедельно последовательно увеличивают до 5 мг 3 раза в день, 7,5 мг 3 раза в день, 10 мг 3 раза в день, 10 мг 4 раза в день (максимальная доза — 40 мг/сут). При появлении тошноты в период титрования назначают домперидон. При неэффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы (уровень С).
Антихолинергические средства показаны при наличии выраженного тремора покоя и сохранности нейропсихологических функций (уровень С). Хотя у этой категории лиц они могут применяться в качестве средств первого выбора, более целесообразно их добавление к агонисту дофаминовых рецепторов, если последний не обеспечивает достаточного подавления тремора. Лечение тригексифенидилом начинают с дозы 1 мг 2 раза в день, в дальнейшем дозу не чаще чем 1 раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза — 10 мг/сут). Лечение бипериденом начинают с дозы 1 мг 2 раза в день, в дальнейшем дозу не чаще чем 1 раз в неделю последовательно увеличивают до 2 мг 2 раза в день, 2 мг 3 раза в день, 2 мг 4 раза в день (максимальная доза — 10 мг/сут).
Лечение амантадином начинают с дозы 100 мг 2 раза в день, при недостаточном эффекте она может быть увеличена до 100 мг 3 раза в день, в дальнейшем — до 100 мг 4–5 раз в день (максимальная доза — 500 мг/сут). Лечение селегилином начинают с дозы 5 мг утром, через 1 нед ее увеличивают до 5 мг 2 раза в день.
Если указанные препараты и их комбинация в максимально переносимых дозах не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат, содержащий леводопу (стандартный препарат или препарат с замедленным высвобождением) в минимальной эффективной дозе (уровень А).
У лиц в возрасте 50–70 лет при умеренном двигательном дефекте и относительной сохранности нейропсихологических функций лечение начинают с одного из агонистов дофаминовых рецепторов. Если максимальные переносимые дозы одного из этих препаратов не обеспечивают достаточного функционального улучшения, к нему последовательно добавляют по указанным выше схемам один из следующих препаратов: селегилин, амантадин или холинолитик (при наличии тремора покоя). Больным после 65 лет тригексифенидил и другие антихолинергические средства не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов (уровень В). При недостаточной эффективности к комбинации из двух-трех указанных выше препаратов добавляют средство, содержащее леводопу, в минимальной эффективной дозе (200–400 мг/сут).
У лиц в возрасте 50–70 лет при выраженном двигательном дефекте, ограничивающем трудоспособность и/или возможность самообслуживания, а также при наличии выраженных когнитивных нарушений и необходимости получения быстрого эффекта, лечение начинают с препаратов, содержащих леводопу. Для лечения могут быть использованы как стандартные препараты, так и препараты с замедленным высвобождением. Если небольшие дозы леводопы (200–400 мг/сут) не обеспечивают необходимого улучшения, к ним последовательно добавляют по указанным выше схемам следующие препараты: агонист дофаминовых рецепторов, амантадин, селегилин.
У лиц старше 70 лет лечение следует начинать со средств, содержащих леводопу. Для лечения могут применяться как стандартные препараты, содержащие леводопу, так и препараты с замедленным высвобождением (уровень В).
Другие меры. Поскольку дофаминергические препараты у больных с глаукомой могут повысить внутриглазное давление, перед их назначением у всех пациентов старше 40 лет следует измерить внутриглазное давление. В дальнейшем его измерение проводят после подбора противопаркинсонической терапии (обычно на втором месяце лечения) либо при появлении жалоб на ухудшение зрения. Больным с запорами и другими проявлениями нарушения моторики желудочно-кишечного тракта показана диета с высоким содержанием пищевых волокон (уровень С); при снижении массы тела показана диета с повышенным содержанием белковых продуктов, а также продуктов, богатых витаминами и микроэлементами (уровень С); для подбора диеты назначается консультация врача-диетолога.
При ограничении подвижности и наличии скелетно-мышечных болей показано проведение лечебной физкультуры, включающей упражнение на растяжение мышц, поддержание гибкости и тренировку координации движений (уровень С), физиотерапии (уровень С), рефлексотерапии (уровень С); в связи с этим назначаются консультации врача лечебной физкультуры, физиотерапевта, рефлексотерапевта. Больному рекомендуется посильная двигательная активность с ежедневными занятиями лечебной гимнастикой, по показаниям — занятия с логопедом. В зависимости от тяжести двигательных расстройств больной может продолжать прежнюю работу, перейти на более легкую, изменить условия работы (неполный рабочий день). При стойкой утрате трудоспособности больному определяется группа инвалидности (вопросы трудоспособности определяются МСЭК).
Алгоритм лечения БП представлен на рисунке.
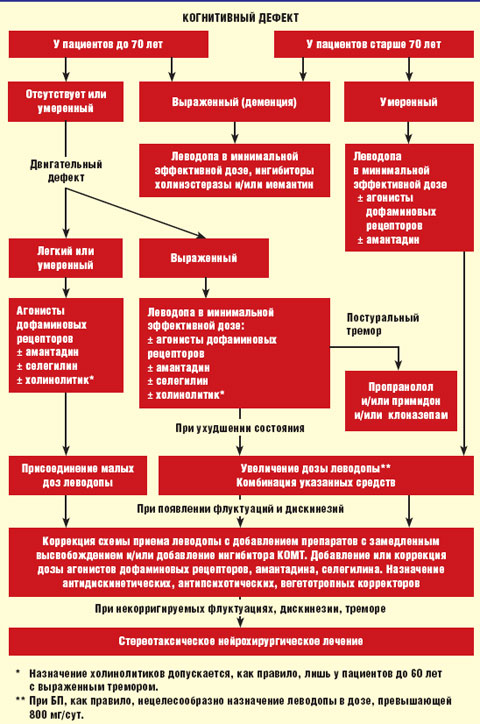 |
| Рисунок. Алгоритм лечения болезни Паркинсона |
Дальнейшая терапия при стабильной реакции на противопаркинсонические средства
Общие принципы лечения. Индивидуальную эффективную дозу препаратов подбирают путем медленного титрования, стремясь получить адекватный эффект, необходимый для продолжения профессиональной деятельности или поддержания повседневной активности, и избежать побочного действия. При необходимости для усиления эффекта противопаркинсонической терапии проводятся следующие мероприятия.
Особенности лечения больных с тремором. При выраженном дрожательном гиперкинезе, нарушающем функции конечностей, особенно если он имеет постурально-кинетический компонент, к противопаркинсоническим средствам при отсутствии противопоказаний добавляют пропранолол (уровень В). Лечение пропранололом начинают с дозы 10 мг 3 раза в день. В дальнейшем дозу последовательно увеличивают не чаще чем 1 раз в неделю до 20 мг 3 раза в день, 40 мг 3 раза в день, 40 мг 4 раза в день (максимально до 320 мг/сут в 3–4 приема). При наличии противопоказаний к применению пропранолола (брадиаритмия, сахарный диабет, заболевания периферических сосудов), непереносимости или неэффективности препарата назначают примидон (уровень С). Первоначально препарат назначают в дозе 31,25 мг на ночь, затем дозу последовательно увеличивают 1 раз в 7–10 дней до 62,5 мг на ночь, 125 мг на ночь, 250 мг на ночь (максимально до 750 мг/сут в 2–4 приема или однократно на ночь).
Если пропранолол вызвал недостаточное улучшение, то к нему добавляют примидон в указанных дозах (уровень С). Клоназепам может быть добавлен к пропранололу или примидону при наличии выраженного кинетического компонента тремора (уровень С). Клоназепам первоначально назначают в дозе 0,5 мг на ночь, затем 1 раз в 7–10 дней дозу последовательно увеличивают до 0,5 мг 2 раза в день, 1 мг 2 раза в день, 2 мг 2 раза в день, пока не будет достигнуто существенное ослабление дрожания. При выраженном треморе может быть также использован клозапин в дозе 12,5–50 мг/сут (уровень В).
Особенности лечения больных с аффективными нарушениями. При наличии аффективных нарушений назначается консультация врача-психотерапевта для решения вопроса о целесообразности проведения аутогенной тренировки или других методов психотерапии. При наличии депрессии у больных без выраженных нарушений познавательных функций лечение следует начинать с одного из агонистов дофаминовых рецепторов (прамипексол, пирибедил), способных корригировать легкую депрессивную симптоматику, или их сочетания с малыми дозами леводопы (уровень В). При выраженной депрессивной симптоматике после консультации с психиатром показано назначение одного из следующих антидепрессантов: амитриптилин (25–150 мг на ночь), имипрамин (50–150 мг/сут), циталопрам (20–40 мг/сут), флуоксетин (20–40 мг/сут), сертралин (50–100 мг/сут), пароксетин (10–20 мг/сут), миртазапин (7,5–30 мг/сут), венлафаксин (75–225 мг/сут). После получения лечебного эффекта продолжительность назначения антидепрессанта в эффективной дозе должна быть не менее 6 мес (уровень С).
Продолжение читайте в следующем номере.
О. С. Левин, доктор медицинских наук, профессор
РМАПО, Центр экстрапирамидных заболеваний, Москва
