Берлитион 600 или тиогамма 600 что лучше
Берлитион 600 ЕД : инструкция по применению
Лекарственная форма
Концентрат для приготовления раствора для инфузий 600 мг/24 мл
Состав
24 мл концентрата содержат:
вспомогательные вещества: вода для инъекций, азот, аргон.
Описание
Прозрачный зеленовато-желтый раствор
Фармакотерапевтическая группа
Прочие препараты для лечения заболеваний желудочно-кишечного тракта и нарушений обмена веществ. Различные прочие препараты для лечения заболеваний ЖКТ и обмена веществ. Тиоктовая кислота
Фармакологические свойства
Тиоктовая кислота в высокой степени подвергается эффекту первого прохождения через печень. В системной биодоступности тиоктовой кислоты имеются значительные индивидуальные колебания. Тиоктовая кислота биотрансформируется путем окисления боковой цепи и коньюгации.
Тиоктовая кислота реагирует in vitro с комплексами ионов металлов (например, с цисплатином). Тиоктовая кислота с молекулами сахара вступает в труднорастворимые комплексные соединения.
Тиоктовая кислота является витаминоподобным, но эндогенным веществом, выполняющим функцию кофермента в окислительном декарбоксилировании альфа-кетокислот. Вызванная сахарным диабетом гипергликемия приводит к отложению глюкозы на матричных протеинах кровеносных сосудов и образованию конечных продуктов прогрессирующего гликозилирования («Advanced Glycosylation End Products»). Этот процесс приводит к уменьшению эндоневрального кровотока и к эндоневральной гипоксии/ишемии, что связано с повышенной выработкой свободных кислородных радикалов, которые повреждают периферические нервы. В периферических нервах также было установлено обеднение антиоксидантами, например, глутатионом. Экспериментальные исследования показывают, что тиоктовая кислота участвует в данных биохимических процессах, уменьшая образование конечных продуктов гликозилирования, улучшая эндоневральный кровоток и увеличивая физиологические уровни антиоксиданта глютатиона. Она также действует как антиоксидант для свободных радикалов кислорода в нервах, пораженных диабетом. На основании данных эффектов, наблюдаемых в ходе эксперимента, можно предположить, что тиоктовая кислота улучшает функциональность периферических нервов. Это касается нарушений чувствительности при диабетической полиневропатии, которые могут проявляться в виде дизестезии и парестезии (например, жжение, боль, чувство онемения или формикации). Клинические исследования демонстрируют благоприятное воздействие тиоктовой кислоты при симптоматическом лечении диабетической полиневропатии, при таких известных симптомах, как жжение, парестезии, ощущение онемения и боли.
Берлитион 600 или тиогамма 600 что лучше
В соответствии с Федеральным законом от 22 декабря 2014 г. N 429 взаимозаменяемым лекарственным препаратом является лекарственный препарат с доказанной терапевтической эквивалентностью или биоэквивалентностью в отношении референтного лекарственного препарата, имеющий эквивалентные ему качественный состав и количественный состав действующих веществ, состав вспомогательных веществ, лекарственную форму и идентичные путь введения и способ применения, произведенные в соответствии с требованиями правил надлежащей производственной практики.
Референтный лекарственный препарат должен отвечать двум требованиям: быть зарегистрированным в Российской Федерации первым из всех возможных аналогов и его качество, эффективность и безопасность должны быть доказаны на основании результатов доклинических исследований лекарственных средств и клинических исследований лекарственных препаратов, проведенных в соответствии с требованиями части 3 ст. 18 Федерального закона от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств» [1].
Тиоктовая кислота (ТК) (Thioctic acid) или Альфа-липоевая кислота (Alpha-lipoic acid), Липоевая кислота была выделена из экстрактов говяжьей печени в 1951 году, с 1952 года производится ее синтез. У здорового человека потребности в ТК составляют 1 – 2 грамма в сутки. ТК в организм поступает из пищи (говядина, печень, дрожжи, картофель), эндогенный синтез в норме осуществляется кишечной микрофлорой. В организме человека содержание ТК в норме составляет 1-50 нг/мл. ТК – естественный коэнзим митохондриального комплекса, катализирующего окислительное декарбоксилирование α-кетокислот (пирувата и α-кетоглутарата), то есть регулирует аэробные процессы энергообразования в клетке, связанные с окислением углеводов и жиров. ТК влияет на перекисное окисление липидов в митохондриях и микросомах, в виде дигидролипоевой кислоты участвует в каскаде восстановления антиоксидантов (аскорбиновая кислота, глутатион, коэнзим Q10 и витамин Е) с использованием ионов железа и меди. У животных с экспериментальным сахарным диабетом (СД), ожирением и инсулинорезистентностью определяется дефицита синтетазы ТК, что ведет к снижению синтеза эндогенной ТК с активацией маркеров воспаления (фактора некроза опухолей – α (TNF-α), моноцит-хемоаттрактивного протеина-1 (MCP-1), в результате происходит рост перекисного окисления липидов и усиление окислительной модификации белков [2]. Введение ТК восстанавливает антиоксидантный потенциал, ускоряет окисление глюкозы, ее фосфорилирование, гликолиз [3]. ТК как в эксперименте, так и у больных СД сдвигает спектр липидов в сторону ненасыщенных жирных кислот, обеспечивая синтез белка, накоплению гликогена в печени, обладает антигипергликемическим, антигипертензивным эффектами и, нормализуя образование митохондриального супероксида аниона, блокирует образование конечных продуктов гликирования, снижает инсулинорезистентность [4]. Уникальность ТК в том, что она может существовать как в окисленной, так и в восстановленной форме, проявляя как липофильные (липоевая кислота), так и гидрофильные (дегидролипоевая кислота) свойства [5]. Синтезированная ТК представляет собой смесь сферических R(+) и S(-) изомеров, хорошо растворяющихся как в воде, так и в липофильных растворителях. При поступлении в организм ТК восстанавливается в основном из R(+)-изоформы до дигидролипоевой кислоты, которая и обеспечивает основные терапевтические эффекты. Дигидролипоевая кислота не используется в качестве лекарственного препарата, т. к. при хранении легко окисляется. Липофильность обеспечивает проникновение ТК через биологические мембраны и гистио-гематические барьеры, в первую очередь, гематоэнцефалический барьер.
Применение препаратов тиоктовой кислоты
Состав препаратов ТК для перорального применения, зарегистрированных в России
Липоевая кислота, Уралбиофарм, Россия
Жировая дистрофия печени, цирроз печени, хронический гепатит А, интоксикация (в т.ч. солями тяжелых металлов, бледной поганкой), гиперлипидемия.
Взрослые – по 2 таблетки (50 мг) 3-4 раза в сутки.
Дети старше 6 лет – по 1 таблетке (25 мг) 2-3 раза в сутки
Липоевая кислота – 25 мг
Состав ядра: декстроза моногидрат (глюкоза), крахмал картофельный, сахароза (сахар), кальция стеарат (кальция стеарат 1-водный), тальк.
Состав оболочки: кремния диоксид коллоидный (аэросил), воск пчелиный, титана диоксид, магния карбонат основной, повидон (поливинилпирролидон), сахароза (сахар), тальк, желтый водорастворимый краситель (КФ 6001).
Липоевая кислота, Марбиофарм, Россия
Жировая дистрофия печени, цирроз печени, хронический гепатит А, интоксикация (в т.ч. солями тяжелых металлов, бледной поганкой), гиперлипидемия.
Взрослые – по 2 таблетки (50 мг) 3-4 раза в сутки.
Дети старше 6 лет – по 1 таблетке (25 мг) 2-3 раза в сутки
Липоевая кислота (тиоктовая кислота) – 12 мг или 25 мг Вспомогательные вещества таблетки-ядра: сахар (сахароза) – 52,917 мг или 105,22 мг, глюкоза (декстроза) – 21,3 мг или 41,7 мг, крахмал картофельный – 10,1 мг или 20,7 мг, кальция стеарат 1-водный (кальция стеарата моногидрат) – 0,5 мг или 1,0 мг, стеариновая кислота – 0,5 мг или 1,0 мг, тальк (магния гидросиликат) – 2,5 мг или 5,0 мг.
Вспомогательные вещества оболочки: аэросил (кремния диоксид коллоидный) – 0,77 мг или 1,08 мг, титана диоксид – 1,689 мг или 2,35 мг, магния карбонат основной (магния гидроксикарбонат) – 13,976 мг или 18,0 мг, масло вазелиновое – 0,014 мг или 0,02 мг, поливинилпирролидон низкомолекулярный медицинский (повидон) – 0,665 мг или 0,93 мг, сахар (сахароза) – 57,6 мг или 77,24 мг, тальк (магния гидросиликат) – 0,085 мг или 0,12 мг, краситель хинолиновый желтый Е-104 – 0,18 мг или 0,23 мг
Состав препаратов ТК для парентерального применения, зарегистрированных в России для лечения диабетической и алкогольной нейропатии
трометамоловая соль ТК* – 39,7 мг в пересчете на ТК- 25 мг
*образуется в результате взаимодействия ТК 25 мг и трометамола 28,5 мг
трометамол – 28,5 мг
0,5 М раствор трометамола – до pH 8,2 – 8,5
вода для инъекций – до 1,0 мл.
меглуминовая соль ТК – 1167,70 мг в пересчете на ТК – 600 мг.
макрогол 300 – 4000,00 мг, меглумин, вода для инъекций до 50 мл.
этилендиамин – 0,155 г
вода для инъекций – до 24 мл.
этилендиаминовая соль ТК – 32,3 мг в пересчете на ТК- 25 мг
тиоктата трометамол – 952,2876 в пересчете на ТК – 600 мг.
(полиэтиленгликоль 400), повидон (коллидон® 17 PF или пласдон С-15), вода для инъекций
Макрогол (макрогол-300) – 2400 мг; – 4800 мг
Меглюмин от 12,5 мг до 35 мг
от 25 мг до 70 мг (до pH 8,0 – 9,0);
Вода для инъекций до 12 мл; до 24 мл меглюмина тиоктат** образуется в результате взаимодействия ТК 300 мг (600 мг) и меглюмина 283,86 мг (567,72 мг)
этилендиамин – 87,4 мг в пересчете
вода для инъекций до 10 мл
1 мл раствора содержит: тиоктовая кислота 30,0 мг в виде меглюмина тиоктата – 58,382 мг
Меглюмин (N-метилглюкамин) – 29,5 мг, макрогол 300 (полиэтиленгликоль 300) – 20 мг, вода для инъекций – до 1 мл.
Первоначально препараты ТК применялись в относительно небольших суточных дозах как для приема внутрь (дозе 75 мг – 150 мг), так и в растворе для внутримышечного введения (0,01 – 0,02 г) [8]. В России с 1984 года зарегистрированы и применяются препараты для лечения интоксикаций, заболеваний печени.
В 90-х годах эффекты ТК в лечении периферической и кардиоваскулярной автономной нейропатии у пациентов с сахарным диабетом (СД) были изучены в ходе рандомизированного, двойного слепого, многоцентрового, плацебо-контролируемого исследования ALADIN (Alpha-Lipoic Acid in Diabetic Neuropathy). В 1997 году препарат зарегистрирован в России. Наличие доказательной базы позволило препарату ТИОКТАЦИД 600 Т МЕДА Фарма ГмбХ и Ко.КГ (Германия) в форме для внутривенного введения стать референтным препаратом Тиоктовой кислоты.
Исследования ALADIN привело к пересмотру рекомендаций. Это трехнедельное исследование было проведено на 328 больных диабетом 2 типа с диабетической нейропатией (ДНП). Препарат трометамоловой соли ТК исследовался в форме для внутривенных инфузий в трех разных дозах (100 мг, 600 мг или 1200 мг). Участники исследования были рандомизированы либо по этим трем группам, либо в группу плацебо-контроля. Интенсивность и частота возникновения боли и других вариантов сенсорных нарушений оценивались с помощью анкет, заполнявшихся в начале исследования и в ходе наблюдения. Порог вибрационной чувствительности определялся с помощью камертона, кроме этого оценивалась тепловая чувствительность. Эффективность ТК в дозе 100 мг была на уровне группы плацебо-контроля, в то время как эффект больших доз был значительно более мощным по всем параметрам. Дозы ТК в 600 и 1200 мг приводили к ослаблению сенсорных нарушений любого происхождения, а также боли. При обеих этих дозах было отмечено значительное улучшение тепловой чувствительности, нормализация порога вибрационной чувствительности. Доля больных, у которых был зарегистрирован ответ на применение ТК, была максимальной (82,5 %) в группе, получавшей ежедневно дозу в 600 мг. При этом эффективность дозы в 1200 мг ежедневно не превосходила таковую дозы в 600 мг; однако, при первом дозовом режиме в значительной степени была повышена частота гастроинтестинальных побочных эффектов. Доза в 600 мг оказалась эффективной и хорошо переносилась, а вызываемые ею побочные эффекты по частоте не превышали уровень группы плацебо-контроля [9].
Сравнительное изучение трометамоловой и этилендиаминовой солей ТК было проведено в двойном слепом плацебоконтролируемом перекрестном исследовании. При этом не было замечено нежелательного системного действия. Однако анализ местных побочных реакций показал, что инъекционная форма этилендиаминовой соли достоверно уступала (р = 0,016) лекарственной форме трометамоловой соли. Больные чаще жаловались на боль и другие расстройства чувствительности, а также местное раздражение при инъекции после назначения этилендиаминовой соли. Из всех стабилизаторов, применяемых для изготовления лекарственных форм ТК, наимение токсичным является меглюмин. Солюбилизатором (поверхностно – активное вещество) в препаратах ТК является полиэтиленгликоль (макрогол). Он формирует обратимые комплексы с активными субстанциями, повышая их растворимость и делая возможным повысить их растворимость. Полиэтиленгликоли с молекулярной массой до 600 смешиваются с водой в любых отношениях. Они обладают выраженной низкой острой и хронической токсичностью, которая ниже глицерина. Не проявляют эмбритоксичности. Полиэтиленгликоли могут рассматриваться, как практически нетоксичные вещества [10].
С препаратом Тиоктацид для внутривенного введения и для приема внутрь было проведено целый ряд исследований: ALADIN I, ALADIN II, ALADIN III, ORPIL, NATHAN, DECAN, SYDNEY, подтвердивших эффективность и безопасность ТК [11].
Клинико – фармакологические параметры препаратов ТК для перорального применения, зарегистрированных в России для лечения диабетической и алкогольной нейропатии
Максимальная концентрация в плазме крови (Cmax) после приема 1 таблетки ТК быстрого высвобождения составляет 4 мкг/мл, время ее достижения – 25–30 мин, т.е. к моменту приема пищи ЛВ уже в крови
Клиническая фармакология препаратов ТК
В 1996 году было проведено исследование на здоровых добровольцах препаратов ТК для перорального применения. Сравнивались клинико – фармакологические параметры после приема эталонного раствора ТК и таблетированной формы ТК. Это было вызвано тем, что смесь сферических R(+) и S(-) изомеров, из которых состоит обычная таблетированная форма ТК, при всасывании не создавала концентрации, необходимой для получения желаемого терапевтического эффекта. В данном случае проблема сфероизомеров суммировалась с эффектом первого прохождения через печень [12]. Это позволило отнести ТК к веществам с критической биодоступностью или критическим типом влияния параметров растворения на биодоступность и терапевтический эффект [13].
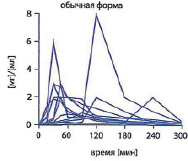
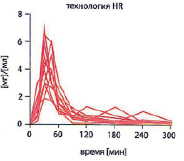
Известно, что еда значительно ухудшает всасывание ТК при пероральном приеме, поэтому такие препараты рекомендовано принимать более, чем за 30 минут до еды, чтобы избежать возможной «потери» лекарственного вещества (ЛВ), происходящей при взаимодействии с пищей. Для ТК свойственны значительные колебания времени достижения пиков максимальной концентрации в плазме крови, с существенным выходом времени пиков концентрации за пределы 30 минут, причем существенная разница наблюдается не только между пациентами, но и у одного пациента при приеме им ТК в разные дни терапии. С учетом этих особенностей фармакокинетики ТК достижение терапевтической концентрации и лечебные эффекты ТК становятся трудно прогнозируемыми, а рекомендованная дозировка сложно определяемой. При этом увеличение дозы перорального препарата ТК на случай непредсказуемой «потери» ЛВ при взаимодействии ТК с пищей также не представляется целесообразным из-за дозозависимых побочных эффектов ТК со стороны ЖКТ. Решением проблемы стало создание препарата ТК с быстрым высвобождением – Тиоктацид БВ (производство Меда), который представляет собой оптимизированную лекарственную форму ТК для перорального применения. Технология HR (англ. high release – быстрое высвобождение) обеспечивает повышенную скорость растворения и всасывания ТК при приеме препарата внутрь, что позволяет избежать высокой вариабельности концентрации ТК в плазме крови, смещая пики максимальной концентрации в плазме крови после приема 1 таблетки ТК быстрого высвобождения к интервалу до 30 минут (рисунок). Технология HR одновременно позволяет предупредить и нежелательное взаимодействия ТК с пищей, так как при приеме Тиоктацида БВ за 30 мин до еды всасывание ТК к моменту приема пищи уже полностью завершено.
Относительная биодоступность ТК в форме Тиоктацида БВ более 60 %, что также является улучшенным показателем по сравнению с другими пероральными препаратами ТК (30 % – 40 %). Абсолютная биодоступность составляет 20 %, Т1/2 – 25 мин. Таким образом, при пероральном приёме наблюдается разница в биодоступности и интериндивидуальная вариабельность обычной формы (59 %) по сравнению с формой таблеток быстрого высвобождения (22 %) [14]. Основные пути метаболизма ТК – окисление и конъюгация. Эти характеристики при доказанной эффективности объясняют, почему, несмотря на то, что в исследованиях не было показано значительного накопления препарата в тканях, а плазменные уровни свободной ТК после перорального применения практически ничтожны ввиду высокой скорости клиренса, ТК способна проявлять свои мощные антиоксидантные свойства, по сути, с момента всасывания. Из-за своих гидрофобных и гидрофильных признаков ТК работает в гидрофильных (цитоплазма и плазма крови) и гидрофобных (клеточная мембрана и липопротеины) средах. ТК в незначительных количествах и ее метаболиты (80–90 %) выводятся почками, поэтому почечная экскреция не играет значимой роли, вещество можно безопасно применять у пациентов с терминальной стадией почечной недостаточности [15].
С использованием таблетированной формы ТК БВ неоднократно проводились исследования по выявлению безопасного и эффективного диапазона доз препаратов ТК у пациентов с ДПН [11]. В настоящее время необходимой и достаточной считается доза 600 мг в сутки, однократно, для парентерального или перорального применения, что нашло отражение в инструкции по применению. Данное положение доказано только для Тиоктацида БВ.
Вспомогательные вещества, входящие в препараты ТК и их влияние на абсорбцию
Еще один аспект, отражающий влияние вспомогательных веществ на эффективность и безопастность препаратов ТК для перорального применения, связан с содержанием во многих препаратах ТК лактозы. При ферментопатиях (дефицит лактазы) нарушение переваривания лактозы приводит к бактериальной ферментации, влияет на осмос и ускоряет перистальтику, что, в свою очередь, сокращает время контакта между лактозой и ферментами и далее уменьшает гидролиз лактозы [16]. Конституциональная лактазная недостаточность в России составляет 16–18 % [17]. Проблема использования лактозосодержащих компонентов в качестве вспомогательных веществ в производстве лекарственных средств пристально изучается. Так, по результатам исследования, проведенного в Великобритании на препаратах, применяемых в гастроэнтерологии, сделан вывод о том, что присутствие лактозы в таблетке может быть значимо для абсорбции и носит дозозависимый характер [18]. Многие препараты ТК содержат лактозу. При этом только в инструкции к препарату Тиогамма в разделе «Особые указания» есть предупреждение о том, что пациенты с редкой наследственной непереносимостью фруктозы, глюкозо-галактозным синдромом мальабсорбции или глюкозо-изомальтозным дефицитом не должны принимать препарат Тиогамма® (См. табл. 4).
Состав препаратов ТК для перорального применения, зарегистрированных в России для лечения диабетической и алкогольной нейропатии
Эффективность тиоктовой (альфа-липоевой) кислоты в терапии диабетической полинейропатии
Эффективность тиоктовой (альфа-липоевой) кислоты в терапии диабетической полинейропатии
О.А. Шавловская
Первый Московский государственный медицинский университет им. И.М. Сеченова, г.Москва
Тиоктовая кислота (ТК) – эндогенный антиоксидант. В организме образуется при окислительном декарбоксилировании альфа-кетокислот. В медицинской практике использование ТК в большей степени связано с развитием представлений об окислительном стрессе и перекисном окислении липидов как о достаточно универсальных патогенетических механизмах повреждения клеток и тканей. Одним из препаратов, активное вещество которого ТК, является Тиогамма. Эффективность данного препарата показана при лечении диабетической полинейропатии: снижались как выраженность клинических проявлений (боли, жжения, онемения, парестезии), так и электронейромиографические показатели. Схема применения Тиогаммы: внутривенные инфузии готового раствора в течение 10 дней (во флаконах 50 мг раствора для инфузий 12 мг/мл) с последующим назначением таблетированной формы (600 мг/сут) в течение 50 дней.
Ключевые слова: антиоксидант, диабетическая полинейропатия, диабет, Тиогамма
Efficacy of Thioctic (Alpha-Lipoic) Acid in Treatment of Diabetic Polyneuropathy
O.A. SHAVLOVSKAYA,
First Moscow State Medical University named after I.M. Sechenov
Thioctic acid (TA) is an endogenous antioxidant, in the body is formed by the oxidative decarboxylation of alpha-ketoacids. In medical practice the use of TA is largely connected with the development of ideas about «oxidative stress» and lipid peroxidation, as a universal pathogenetic mechanism of cell and tissue damages. One of the drugs, active substance of which TC is Thiogamma, the effectiveness of which is shown in the treatment of diabetic polyneuropathy, to improve clinical manifestations of sensitive manifestations (pain, burning, numbness, paresthesia) and electroneuromyographic (EMG) data. The scheme of appointment of Thiogamma includes: intravenous infusion of the prepared solution of drug for 10 days (in vials of 50 mg solution for infusion 12 mg/ml), followed by the appointment of a per os form of the drug (600 mg/s) for 50 days.
Тиоктовая (альфа-липоевая) кислота (ТК) – мощный липофильный антиоксидант. Поэтому она по праву считается золотым стандартом патогенетического лечения диабетической полинейропатии [1–3].
ТК синтезируется в организме и выполняет функцию коэнзима при окислительном декарбоксилировании альфа-кетокислот [4–6]. Она представляет собой этилендиаминовую соль альфа-липоевой кислоты, которая, являясь простетической группой мультиферментных комплексов, играет важную роль в метаболизме клетки. ТК как эндогенный антиоксидант связывает свободные радикалы [4, 5, 7]. Именно этим свойством в первую очередь обусловлен возрастающий интерес клиницистов к ТК: открываются новые возможности в терапии заболеваний и патологических состояний, в основе которых лежит дисбаланс окислительно-антиоксидантного гомеостаза. Нормализация клеточного метаболизма происходит посредством инактивации свободных радикалов за счет их связывания SH-группами препарата [4].
ТК потенцирует противовоспалительное действие глюкокортикостероидов и оказывает иммуностимулирующее воздействие. Кроме того, она близка по фармакологическим свойствам к витаминам группы В и способна уменьшать уровень глюкозы в крови и увеличивать содержание гликогена в печени [5].
Использование ТК в медицинской практике связано с развитием представлений об окислительном стрессе и перекисном окислении липидов как о достаточно универсальных патогенетических механизмах повреждения клеток и тканей [8]. Антиоксидантный эффект ТК обусловлен наличием двух тиоловых групп в молекуле, способностью связывать свободные радикалы и свободное тканевое железо, предотвращая таким образом его участие в перекисном окислении липидов [9]. ТК не только обладает самостоятельным антиоксидантным потенциалом, но и поддерживает работу других антиоксидантных звеньев организма [10]. В этом отношении ее протективное действие тесно связано с гомеостазом в системе «глутатион – убихинон» [2]. Выработка активных форм кислорода значительно возрастает при воспалении, иммунологических расстройствах, гипоксии, гипероксии, воздействии лекарств, излучении, дефиците антиоксидантов.
ТК является коэнзимом ключевых ферментов цикла Кребса, что и объясняет ее эффективность. Дополнительным ее преимуществом считается четко зафиксированный эффект утилизации глюкозы [11].
Высокая эффективность и патогенетическое действие ТК доказаны многочисленными экспериментальными и клиническими исследованиями. Так, M. Nagamatsu и соавт. (1995) [12] провели экспериментальное исследование эффективности альфа-липоевой кислоты на животных моделях (крысах) с стрептозотоцин-индуцированной диабетической нейропатией. Альфа-липоевую кислоту в дозах 20, 50 и 100 мг/кг вводили внутрибрюшинно пять раз в неделю через месяц после появления симптомов сахарного диабета. Оценивались показатели улучшения периферического кровотока, скорость проведения импульса по нерву. Скорость кровотока у крыс с диабетом снижалась на 50%, так же как и скорость проведения импульса по нервам. Через месяц применения альфа-липоевой кислоты в дозе 100 мг/кг (дозозависимый эффект) оба показателя нормализовались. Таким образом, на фоне лечения альфа-липоевой кислотой был продемонстрирован эффект уменьшения воздействия окислительного стресса на дистальные участки конечности.
В основе адекватного и рационального способа применения препаратов ТК лежат результаты таких исследований, как ALADIN I, II и III, ORPIL, NATHAN, DECAN, SYDNEY [13–18]. В них отрабатывались доза, кратность приема и длительность курса терапии (табл. 1).

K.J. Ruhnau и соавт. (1999) [19] провели рандомизированное исследование эффективности перорального приема препарата ТК (600 мг/сут) у 12 пациентов с полинейропатией, развившейся на фоне сахарного диабета 2 типа, по сравнению с плацебо (n = 12). Длительность исследования составила три недели. Эффективность оценивалась по динамике нейропатической симптоматики (боли, жжения, парестезии, онемения). Авторы отметили положительную динамику и отсутствие значимых побочных реакций.
В рамках многоцентрового рандомизированного двойного слепого исследования SYDNEY II анализировалась эффективность ТК у больных диабетической полинейропатией [13, 20]. Работа проводилась с 2004 по 2006 г. В исследовании приняли участие 87 пациентов с сахарным диабетом 1 и 2 типа, находившихся на стационарном и амбулаторном лечении. Комплексное клинико-нейрофизиологическое исследование пациентов продемонстрировало, что наиболее ранним электронейромиографическим показателем поражения чувствительного нерва при сахарном диабете является снижение потенциала действия. Уменьшение боли происходило со второй недели применения ТК в дозе 1800 мг/сут, с четвертой недели – в дозе 1200 мг/сут и только к пятой неделе – в дозе 600 мг/сут [13]. Был сделан вывод: внутривенное введение альфа-липоевой кислоты в течение трех недель способствует достоверному ослаблению нейропатических симптомов и объективной неврологической симптоматики. Учитывая дозозависимый характер развития побочных явлений, оптимальной признана доза 600 мг.
В другом исследовании у пациентов с диабетической полинейропатией (n = 24) на фоне трехнедельной терапии ТК в дозе 1800 мг в сутки уменьшились нейропатические симптомы и неврологический дефицит. Частота побочных эффектов в группах ТК и плацебо была сопоставимой [17].
В медицинской практике ТК представлена тремя солями: этилендиаминовой, трометамоловой и меглюминовой [21].
Одним из препаратов, активное вещество которого ТК, является Тиогамма® (компания «Верваг Фарма», Германия). Тиогамма® содержит меглюминовую соль ТК. В качестве солюбилизатора используется полиэтиленгликоль. Препарат подавляет образование свободных радикалов, улучшает энергетический метаболизм нейронов, восстанавливает эндоневральный кровоток. Выпускается в виде таблеток, содержащих 600 мг препарата, и раствора для внутривенных инфузий во флаконах, содержащих 600 мг препарата.
Препарат в таблетированной форме назначается один раз в сутки в дозе 300–600 мг. Таблетка не разжевывается и запивается небольшим количеством жидкости.
Согласно данным исследования ALADIN I [15], действие альфа-липоевой кислоты в дозах 600 и 1200 мг на позитивные нейропатические симптомы практически не различается. При трехнедельном внутривенном введении побочные эффекты (головная боль, тошнота, рвота) чаще развивались при дозе 1200 мг (32,6%), чем при дозе 600 мг (19,8%) или при введении плацебо (20,7%). Был сделан вывод: доза 600 мг оптимальна и с точки зрения частоты развития побочных реакций, и с точки зрения клинической эффективности.
Основными механизмами действия Тиогаммы являются [2]:
1) влияние на энергетический метаболизм, обмен глюкозы и липидов (участие в окислительном декарбоксилировании кетокислот) с активацией цикла Кребса: усиление захвата и утилизации глюкозы клеткой и потребления кислорода, повышение основного обмена, нормализация глюконеогенеза и кетогенеза, торможение образования холестерина;
2) цитопротективное действие: повышение антиоксидантной активности (прямое и опосредованное через системы витаминов С/Е, цистин/цистеин и глютатионовую), стабилизация митохондриальных мембран;
3) влияние на реактивность организма: стимуляция ретикулоэндотелиальной системы, иммунотропное действие, противовоспалительная и обезболивающая активность, связанная с антиоксидантным действием;
4) нейротропные эффекты: стимуляция роста аксонов, положительное влияние на аксональный транспорт, уменьшение негативного влияния на нервные клетки свободных радикалов, нормализация аномального поступления глюкозы к нерву, предупреждение и уменьшение повреждения нервов при экспериментальном диабете;
5) гепатопротективное действие: накопление гликогена в печени, торможение накопления липидов в печени (при некоторых патологических состояниях), повышение активности ряда ферментов, улучшение функциональной активности печени;
6) дезинтоксикационное действие (фосфорорганические соединения, свинец, мышьяк, ртуть, сулема, цианиды, фенотиазиды и др.).
Тиогамма® показана для лечения заболеваний, сопровождающихся неврологической симптоматикой, и прежде всего диабетической полинейропатии [5].
В настоящее время ТК, в частности Тиогамма®, считается наиболее эффективным средством терапии периферической полинейропатии, что подтвердили широкомасштабные многоцентровые многолетние исследования, такие как ALADIN [22].
Однако ТК вследствие ее антиоксидантной активности используется и в других областях медицины [9] (табл. 2).

Известно, что причиной снижения на 50–70% скорости инсулинозависимого трансмембранного переноса глюкозы при сахарном диабете является окислительный стресс. Дефицит альфа-липоевой кислоты у пациентов с сахарным диабетом служит обоснованием применения препаратов ТК для лечения диабетической полинейропатии. Альфа-липоевая кислота повышает биодоступность глюкозы в инсулинозависимых и инсулиннезависимых тканях, увеличивает поглощение глюкозы периферическими нервами до нормального уровня, а также способствует повышению эндоневральных запасов глюкозы, что приводит к восстановлению энергетического метаболизма нервов. Считается, что назначение ТК целесообразно при инсулинрезистентных формах сахарного диабета [9]. В начале лечения оптимальным является внутривенное капельное введение раствора альфа-липоевой кислоты в течение трех недель (15 капельниц) с последующим переходом на пероральный прием препарата в дозе 600 мг один раз в день за 30–40 минут до еды в течение одного-двух месяцев [2].
Эффективность Тиогаммы при диабетической полинейропатии убедительно продемонстрирована во многих клинических исследованиях. Так, Т. Танкова и соавт. (2000) [6, 23] провели рандомизированное открытое плацебоконтролируемое исследование эффективности Тиогаммы при двухэтапном применении: сначала препарат вводили внутривенно в течение 10 дней, затем принимали перорально в течение 50 дней. Использовалась постоянная доза – 600 мг в сутки. Выраженный клинический эффект отмечен после первых 10 дней терапии. По сравнению с контрольной группой у пациентов, получавших Тиогамму, на 40% снизилась интенсивность спонтанных болевых ощущений в ногах, на 35% увеличилась вибрационная чувствительность, определявшаяся в различных зонах стопы. К концу терапии зафиксирована положительная динамика в отношении выраженности боли (оценивалась по визуальной аналоговой шкале) и вибрационной чувствительности. Кроме того, получена положительная динамика показателей, характеризующих тяжесть поражения вегетативной нервной системы: проявления вегетативной нейропатии сократились на 40% и в 2,5 раза уменьшилось падение систолического артериального давления при ортостатической пробе.
В рамках другого моноцентрового рандомизированного двойного слепого плацебоконтролируемого исследования обследованы 120 больных сахарным диабетом 1 и 2 типа. 60 из них получали плацебо, 60 – aльфа-липоевую кислоту в дозе 600 мг в 225 мл физиологического раствора. Препарат вводился внутривенно капельно в течение 30–40 минут [20].
Длительность наблюдения – четыре недели. Оценивалось влияние aльфа-липоевой кислоты на клинические проявления диабетической полинейропатии, электронейромиографические показатели, показатели количественного сенсорного и автономного тестирования. Позитивные нейропатические симптомы были выбраны в качестве основного критерия клинической эффективности. Показана высокая эффективность препарата в отношении большинства изученных показателей состояния периферических нервов. На фоне терапии альфа-липоевой кислотой боль, жжение, онемение, парестезии, ухудшающие качество жизни больных, уменьшились благодаря улучшению функции периферических нервов. Сделан вывод: препараты ТК с успехом могут использоваться в лечении симптомной диабетической полинейропатии.
В исследовании Е.Ю. Комелягиной и соавт. (2006) [14] сравнивалась эффективность двух вариантов терапии диабетической полинейропатии препаратами ТК: пероральный прием 1800 мг в сутки (600 мг три раза в сутки) в течение четырех недель (n = 15) и пероральный прием 600 мг в сутки в течение трех месяцев (n = 15). Показано, что оба режима терапии способствуют достоверному снижению выраженности нейропатических проявлений у больных сахарным диабетом с удовлетворительным контролем заболевания. Авторы констатировали: выбор режима терапии ТК при диабетической полинейропатии зависит от конкретной ситуации: при выраженной болевой симптоматике – более короткий по продолжительности курс с высокой суточной дозой препарата (1800 мг в течение четырех недель), при невыраженных симптомах – более длительный курс с меньшей суточной дозой (600 мг в течение трех месяцев).
Исследование И.И. Матвеевой и соавт. (2007) [24], проводимое в Ижевском эндокринологическом центре, продемонстрировало, что препарат ТК является высокоэффективным при дистальной диабетической нейропатии: улучшаются клиническая симптоматика, состояние периферических нервов, уменьшаются окислительный стресс, инсулинорезистентность. В исследовании участвовали 126 пациентов с впервые выявленным сахарным диабетом 2 типа (скрининг), которые применяли препарат в дозе 600 мг в сутки в течение 10 дней внутривенно, затем перорально в той же дозе в течение восьми – десяти недель.
И.И. Пимонова (2010) [25] изучала эффективность Тиогаммы у 50 больных диабетической и гипотиреоидной дистальной симметричной сенсомоторной полинейропатией. Все участники получали препарат в следующем режиме: 600 мг внутривенно капельно в течение 10 дней (по одной инъекции в день, скорость введения – не более 50 мг/мин), далее перорально по 600 мг утром натощак в течение 30 дней. При лечении диабетической полинейропатии наибольший эффект достигнут у пациентов с острой сенсорной полинейропатией и радикулоплексопатией, достоверные изменения – у пациентов с прогрессирующей сенсомоторной полинейропатией. При лечении гипотиреоидной полинейропатии высокая эффективность отмечена в отношении купирования болевого синдрома, однако положительная динамика четко коррелировала с адекватной заместительной терапией тиреоидными гормонами.
Спектр применения препаратов, содержащих ТК, как в качестве монотерапии, так и в составе комплексной терапии постоянно расширяется. Так, в сравнительном открытом рандомизированном исследовании, проведенном В.Г. Артамоновой и соавт. (2011) [26], оценивалась эффективность препарата ТК в комплексной терапии вегетативно-сенсорной полинейропатии конечностей как проявления вибрационной болезни. Применение ТК в дозе 600 мг в сутки в составе комплексной терапии в течение 21 дня достоверно снижало частоту субъективных жалоб пациентов, приводило к стойкому уменьшению рецидивов болевого синдрома в конечностях, частоты приступов ангиоспазмов и усиливало эффект терапии в целом. Показана положительная динамика в отношении сосудистого тонуса, кровенаполнения и венозного оттока, что, по мнению авторов, обусловливает развитие противовоспалительного, противоотечного, анальгезирующего эффектов и способствует нормализации гомеостаза.
Е.И. Чуканова и соавт. (2001–2014) [27–29] оценивали эффективность применения ТК при дисциркуляторной энцефалопатии и сосудистых когнитивных нарушениях (в составе комплексной патогенетической терапии). В отношении 49 пациентов с дисциркуляторной энцефалопатией показано, что применение препарата в дозе 600 мг два раза в день в течение семи дней с переходом в дальнейшем на прием 600 мг один раз в день в течение 53 дней перорально (за 30 минут до еды) позволяет добиться положительного эффекта. Последний наблюдался уже к седьмому дню терапии. Несмотря на снижение дозы, положительная динамика неврологического статуса сохранялась и достигла максимума к 60-му дню. Кроме того, отмечена положительная динамика нейропсихологического статуса. ТК оказалась эффективной не только при лечении пациентов с дисциркуляторной энцефалопатией, имевших повышенный уровень глюкозы в крови, но и у пациентов с церебральной сосудистой недостаточностью без сахарного диабета [28].
Фармакоэкономический анализ эффективности лечения препаратом ТК проведен у больных с хронической церебральной сосудистой недостаточностью разной степени [29]. В исследование были включены 128 пациентов с дисциркуляторной энцефалопатией. Препарат ТК назначался перорально в суточной дозе 600 мг два раза в день в течение семи дней с последующим переходом на 600 мг один раз в день в течение 23 дней (принимался за 30 минут до еды). У больных дисциркуляторной энцефалопатией первой степени отмечен регресс астенического синдрома, вестибулярной атаксии, аксиальных рефлексов, второй степени – улучшение показателей шкалы «движение», атаксии, псевдобульбарного синдрома, третьей степени – положительная динамика показателей шкалы «движение», атаксии (лобной и мозжечковой), псевдобульбарного синдрома, которая сохранялась до 12-го месяца наблюдения. Показано также статистически достоверное влияние терапии на проявления амиостатического синдрома. Сделан вывод: применение ТК приводит к значительному клиническому улучшению, снижает риск инсультов и уменьшает прогрессирование дисциркуляторной энцефалопатии первой и второй степени. При этом побочные эффекты развиваются редко. ТК хорошо переносится, в том числе и пациентами старших возрастных групп. Такая терапия предпочтительна и с экономической точки зрения.
Исследования М. Senoglu и соавт. (2009) [30] продемонстрировали эффективность альфа-липоевой кислоты в отношении таких клинических симптомов, как боль, парестезии, гипостезия, у пациентов с компрессионной радикулопатией вследствие дискорадикулярного конфликта. Данные результаты коррелируют с результатами исследования M. Ranieri и соавт. (2009) [31], в котором сравнивалась эффективность шестинедельной реабилитационной программы и таковой с добавлением комбинации альфа-липоевой и гамма-линоленовой кислот у пациентов с дискогенной радикулопатией. E. Battisti и соавт. (2013) [32] применяли ТК в дозе 600 мг в сутки в комплексной терапии 98 пациентов с болями в нижней части спины. Длительность лечения составила 60 дней. Результаты свидетельствовали о том, что на фоне использования ТК прием анальгетиков сокращается: если в начале лечения их принимали 73,5% пациентов, в конце – только 8%. Антиоксиданты (ТК) могут успешно использоваться в мультимодальной стратегии лечения больных с хроническими болями в спине.
Таким образом, имеющиеся на сегодняшний день данные позволяют рекомендовать Тиогамму для лечения пациентов с нейропатией соматогенного происхождения. С высокой степенью эффективности применяется двухэтапная схема терапии: внутривенные инфузии готового раствора в течение 10 дней (во флаконах 50 мг раствора для инфузий 12 мг/мл, что эквивалентно 600 мг ТК, вводится 30–40 минут капельно) с последующим переходом на таблетированную форму препарата (600 мг в сутки) в течение 50 дней. С точки зрения клинической эффективности и риска развития побочных эффектов оптимальной считается доза 600 мг в сутки. При выраженном болевом синдроме предпочтение следует отдавать более короткому по продолжительности курсу с высокой суточной дозой препарата (1800 мг в течение четырех недель), при менее выраженном – более длительному курсу с меньшей суточной дозой (600 мг в течение трех месяцев).
Назначение ТК целесообразно при инсулинорезистентных формах сахарного диабета: введение раствора альфа-липоевой кислоты внутривенно капельно в течение трех недель (15 капельниц) с последующим приемом 600 мг препарата в виде таблеток (один раз в день за 30–40 минут до еды) в течение одного-двух месяцев.
Важно отметить, что преимуществом препарата Тиогамма® является форма выпуска, которая позволяет вводить препарат внутривенно капельно и не требует предварительного разведения.