Бдс не визуализируется что это значит
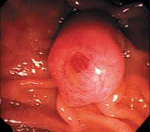
Рак большого дуоденального сосочка
Рак большого дуоденального сосочка – злокачественная опухоль фатерова сосочка, расположенного в области двенадцатиперстной кишки. Характерен медленный рост и позднее метастазирование при раннем появлении механической желтухи. Наблюдаются боли, периодическое повышение температуры тела, увеличение печени и желчного пузыря. На поздних стадиях возможны кровотечения. Диагноз устанавливают с учетом симптоматики, данных рентгенографии, фиброгастродуоденоскопии и результатов биопсии. Лечение оперативное: гастропанкреатодуоденальная резекция, папиллэктомия, дуоденэктомия, паллиативные вмешательства.
Общие сведения
Рак большого дуоденального сосочка – злокачественная неоплазия большого дуоденального (фатерова) соска, локализующегося в нисходящей части двенадцатиперстной кишки и представляющего собой соустье главного панкреатического протока и общего желчного протока. Составляет 40% от общего количества онкологических поражений пилородуоденальной зоны, 5% от общего числа неоплазий ЖКТ и 1-2% от общего количества раков различных локализаций. Рак большого дуоденального сосочка является третьей по распространенности причиной возникновения механической желтухи. Обычно поражает пожилых пациентов, средний возраст больных составляет 54 года. Очень редко выявляется у детей. Женщины страдают реже мужчин. Лечение осуществляют специалисты в сфере онкологии, гастроэнтерологии и абдоминальной хирургии.
Причины рака фатерова сосочка
Причины возникновения опухоли точно не выяснены. Специалисты отмечают, что определенное значение имеет наследственная предрасположенность – заболевание нередко диагностируется в семьях, члены которой страдают семейным полипозом. Кроме того, у некоторых пациентов выявляется генетическая мутация K-ras. Установлено, что неоплазия может развиться в результате малигнизации аденомы фатерова соска. В список факторов риска также включают хронический панкреатит и заболевания гепатобилиарной системы.
Источником рака большого дуоденального сосочка являются трансформировавшиеся клетки эпителия слизистой двенадцатиперстной кишки, панкреатического протока либо общего желчного протока. Для новообразования характерен медленный экзофитный рост. По внешнему виду неоплазия напоминает папиллому, разрастание грибовидной формы или в виде соцветья цветной капусты. Реже выявляются эндофитные формы. При экзофитных формах рака большого дуоденального сосочка желтуха чаще ремиттирующая, при эндофитных – постоянная. Диаметр узла при его хирургическом удалении в среднем составляет 3 мм.
При микроскопическом исследовании выявляются клеточные скопления и отдельно лежащие эндокринные клетки веретенообразной, треугольной и цилиндрической формы. Число эндокринных клеток уменьшается по мере снижения уровня дифференцировки неоплазии. Обычно рак большого дуоденального сосочка прорастает общий желчный проток, возможно также поражение поджелудочной железы и стенки двенадцатиперстной кишки, лимфогенное и отдаленное метастазирование. Лимфогенные метастазы обнаруживаются у 21-51% больных. Отдаленные вторичные очаги выявляются достаточно редко. Обычно поражается печень, реже – кости, головной мозг, легкие и надпочечники.
Рак большого дуоденального сосочка может полностью обтурировать просвет желчного протока, реже выявляется стеноз. Даже при частичном сдавлении из-за отечности слизистой возникают грубые расстройства оттока желчи, становящиеся причиной развития механической желтухи. Появляется билиарная гипертензия, сопровождающаяся дилатацией желчевыводящих путей и протоков поджелудочной железы. Кишечная непроходимость развивается очень редко. При распространении процесса возможно прорастание стенки кишечника и распад неоплазии с развитием внутреннего кровотечения.
Симптомы рака фатерова сосочка
Первым проявлением болезни часто становится механическая желтуха, возникшая на фоне соматического благополучия. Вначале желтуха обычно перемежающаяся, нормализация биохимических показателей крови обусловлена уменьшением отека в области стенозированного желчного протока. При прогрессировании рака большого дуоденального сосочка желтуха становится более стойкой, изменение цвета кожи выявляется после интенсивных болей, сопровождающихся ознобами и проливными потами. Пациенты жалуются на выраженный зуд. Интермиттирующий характер желтухи на поздних стадиях (выявляется в 51% случаев) обусловлен распадом рака большого дуоденального сосочка, сопровождающегося временным восстановлением проходимости желчного протока.
При пальпации определяется гепатомегалия. У 60% пациентов под нижним краем печени прощупывается увеличенный желчный пузырь (симптом Курвуазье). При продолжительной обтурации желчевыводящих путей возникают цирроз печени и хронический панкреатит. При инвазии рака большого дуоденального сосочка в стенку кишечника и последующем распаде опухоли возможны кровотечения (острые массивные либо повторяющиеся незначительные) с развитием анемии. При региональном метастазировании отмечается изменение болевого синдрома.
Характерной особенностью рака большого дуоденального сосочка является ранняя потеря веса. Причиной похудания становятся стеноз либо обструкция панкреатических протоков, из-за которых в ЖКТ перестают поступать ферменты, необходимые для расщепления белков и жиров. Нарушение проходимости общего желчного протока еще больше усугубляет расстройства всасывания жиров и ухудшает всасываемость витаминов. Снижение веса и авитаминоз становятся причиной адинамии.
У больных раком большого дуоденального сосочка часто наблюдаются поносы, сопровождающиеся вздутием и болями в животе. Каловые массы зловонные, глинисто-серые. В запущенных случаях может выявляться жировой кал. При появлении регионарных метастазов отмечается изменение характера болевого синдрома. На поздних стадиях определяются истощение и расстройства функций органов, пораженных отдаленными метастазами.
Диагностика рака фатерова сосочка
Постановка диагноза сопряжена с существенными затруднениями из-за неспецифичности симптоматики. В процессе диагностики онколог ориентируется на жалобы, данные объективного осмотра, рентгенографии, чреспеченочной или внутривенной холангиографии, дуоденального зондирования, фиброгастродуоденоскопии и других исследований. При желтухе определяется высокий уровень билирубина с преобладанием прямой фракции, стеркобилин в кале отсутствует. На поздних стадиях рака большого дуоденального сосочка выявляется анемия.
Достаточно достоверным исследованием является дуоденальное зондирование, при проведении которого часто удается обнаружить кровь в дуоденальном содержимом. Иногда в ходе этого исследования выявляются клетки неоплазии и ферменты поджелудочной железы. Рентгенографическими признаками рака большого дуоденального сосочка являются неровность контуров либо дефект наполнения в зоне внутренней стенки двенадцатиперстной кишки, а также отсутствие проходимости либо деформация желчного протока в зоне, приближенной к фатеровому соску.
При проведении фиброгастродуоденоскопии обнаруживают опухолевидное образование и выполняют эндоскопическую биопсию подозрительного участка. В некоторых случаях диагноз рака большого дуоденального сосочка не удается установить при помощи стандартных методик, для уточнения характера патологии приходится проводить лапаротомию, рассекать фатеров сосок, осуществлять забор ткани, а затем принимать решение об объеме операции на основании данных срочного гистологического исследования. Дифференциальный диагноз осуществляют с гепатитом, раком головки поджелудочной железы и раком желчных путей.
Лечение рака фатерова сосочка
Основным способом лечения данной патологии является оперативное вмешательство, которое, в зависимости от распространенности процесса, может быть радикальным либо паллиативным. Группа паллиативных операций включает в себя около десяти различных вариантов анастомозов, позволяющих восстановить отток желчи в пищеварительный тракт либо (реже) предотвратить сдавление двенадцатиперстной кишки растущим раком большого дуоденального сосочка.
Радикальная операция является тяжелым и сложным вмешательством, поэтому проводится только после тщательного отбора пациентов в соответствии со стандартами, включающими в себя допустимую степень истощения, уровень белков в крови, определенные показатели пульса и жизненной емкости легких и т. д. Больным раком большого дуоденального сосочка проводят гастропанкреатодуоденальную резекцию. При наличии противопоказаний к радикальному вмешательству выполняют условно радикальные операции: папиллэктомию, дуоденэктомию либо экономную панкреатодуоденальную резекцию. Радиотерапия и химиопрепараты при раке большого дуоденального сосочка малоэффективны.
Комплексное лечение дисфункций большого дуоденального сосочка
Рассмотрены классификация, клиническая картина и клинические типы дисфункции большого дуоденального сосочка (БДС), методы диагностики, включая дифференциальную диагностику функциональных и органических поражений сфинктера БДС, и подходы к лечению.
An examination was provided on classification, clinical picture and clinical types of dysfunction of major duodenal papilla (MDP), the methods of diagnostics, including differential diagnostics of the functional and organic failures of sphincter MDP, and approaches to the treatment.
Дисфункции большого дуоденального сосочка (БДС) — функциональные заболевания, проявляющиеся нарушением механизмов расслабления и сокращения сфинктера Одди с преобладанием повышения тонуса и спазма (гипермоторная, гиперкинетическая) или расслабления и атонии (гипомоторная, гипокинетическая), без органических и воспалительных изменений, вызывающие нарушение поступления желчи и панкреатического сока в двенадцатиперстную кишку.
Дискинезия желчных протоков обычно возникает в результате нарушения нейрогуморальной регуляции механизмов расслабления и сокращения сфинктеров Одди, Мартынова–Люткенса и Мирицци. В одних случаях преобладают атония общего желчного протока и спазм сфинктера Одди вследствие повышения тонуса симпатического отдела вегетативной нервной системы, в других — гипертония и гиперкинезия общего желчного протока при расслаблении упомянутого выше сфинктера, что связано с возбуждением блуждающего нерва. В клинической практике чаще встречается гипермоторная дискинезия. Причина — психогенное воздействие (эмоциональные перенапряжения, стрессы), нейроэндокринные расстройства, воспалительные заболевания желчного пузыря, поджелудочной железы, двенадцатиперстной кишки. Дисфункции БДС часто сочетаются с гипермоторными и гипомоторными дискинезиями желчного пузыря.
Классификация:
1. Дисфункция по гипертоническому типу:
2. Дисфункция по гипотоническому типу (недостаточность сфинктера Одди):
Клиника:
Клинические типы дисфункции БДС:
1. Билиарный (встречается чаще): характерны боли в эпигастрии и правом подреберье, иррадиирующие в спину, правую лопатку:
2. Панкреатический — боли в левом подреберье, иррадиируют в спину, уменьшаются при наклоне вперед, не отличаются от болей при остром панкреатите, могут сопровождаться повышением активности панкреатических ферментов при отсутствии причин (алкоголь, желчнокаменная болезнь):
3. Смешанный — боли в эпигастрии или опоясывающие, могут сочетаться с признаками как билиарного, так и панкреатического типа дисфункции.
Диагноз «гипертония сфинктера Одди» ставят в случаях, когда фаза закрытого сфинктера длится дольше 6 мин, а выделение желчи из общего желчного протока замедлено, прерывисто, иногда сопровождается сильной коликообразной болью в правом подреберье.
Недостаточность БДС — чаще всего бывает вторичной, у больных желчнокаменной болезнью, хроническим калькулезным холециститом, вследствие прохождения конкремента, воспаления поджелудочной железы, слизистой двенадцатиперстной кишки, при дуоденальной непроходимости. При дуоденальном зондировании сокращается фаза закрытого сфинктера Одди менее 1 мин или отмечается отсутствие фазы закрытия сфинктера, отсутствие тени желчного пузыря и протоков при холецистохолангиографии, заброс контрастного вещества в желчные протоки при рентгеноскопии желудка, наличие газа в желчных протоках, снижение показателей остаточного давления при холангиоманометрии, уменьшение времени поступления радиофармпрепарата в кишку менее 15–20 мин при гепатобилисцинтиграфии.
Диагностика
1. Трансабдоминальная ультрасонография. Ультразвуковой скрининговый метод обследования занимает ведущее место в диагностике дискинезий (табл.), позволяет с высокой точностью выявить:
Ультразвуковые признаки дискинезий:
2. Ультразвуковая холецистография. Дает возможность исследовать моторно-эвакуаторную функцию желчного пузыря в течение 1,5–2 часов от момента приема желчегонного завтрака до достижения первоначального объема. В норме через 30–40 мин после стимуляции желчный пузырь должен сократиться на 1/3–1/2 объема. Удлинение латентной фазы более 6 мин свидетельствует об усилении тонуса сфинктера Одди.
3. Динамическая гепатобилисцинтиграфия. Основана на регистрации временных показателей пассажа короткоживущих радионуклидов по билиарному тракту. Позволяет оценить поглотительно-выделительную функцию печени, накопительно-эвакуаторную функцию желчного пузыря (гипермоторная, гипомоторная), проходимость терминального отдела общего желчного протока, выявить обструкцию желчных путей, недостаточность, гипертонус, спазм сфинктера Одди, стеноз БДС, дифференцировать органические и функциональные нарушения при помощи пробы с Нитроглицерином или Церукалом. При гипертонусе сфинктера Одди отмечается замедление поступления препарата в двенадцатиперстную кишку после желчегонного завтрака. Этот метод наиболее точно позволяет установить тип дискинезии и степень функциональных нарушений.
4. Фракционное хроматическое дуоденальное зондирование. Дает информацию о:
5. Гастродуоденоскопия. Позволяет исключить органические поражения верхних отделов желудочно-кишечного тракта, оценить состояние БДС, поступление желчи.
6. Эндоскопическая ультрасонография. Позволяет более четко визуализировать терминальный отдел общего желчного протока, БДС, головку поджелудочной железы, место впадения вирсунгова протока с целью диагностики конкрементов, дифференциальной диагностики органических поражений БДС и гипертонуса.
7. Эндоскопическая ретроградная холангиопанкреатография. Метод прямого контрастирования желчных путей, позволяет выявить наличие конкрементов, стеноз БДС, расширение желчных путей, произвести прямую манометрию сфинктера Одди, играет большое значение в дифференциальной диагностике органических и функциональных заболеваний.
8. Компьютерная томография. Позволяет выявить органическое поражение печени и поджелудочной железы.
9. Лабораторная диагностика. При первичных дисфункциях лабораторные анализы не имеют отклонений от нормы, что имеет значение для дифференциальной диагностики. Транзиторное повышение уровня трансаминаз и панкреатических ферментов может отмечаться после приступа при дисфункции сфинктера Одди.
Лечение
Основная цель — восстановление нормального оттока желчи и панкреатического сока в двенадцатиперстную кишку.
Основные принципы лечения:
1) нормализация процессов нейрогуморальной регуляции механизмов желчевыделения — лечение неврозов, психотерапия, устранение гормональных расстройств, конфликтных ситуаций, отдых, правильный режим питания;
2) лечение заболеваний органов брюшной полости, которые являются источником патологических рефлексов на мускулатуру желчного пузыря и желчных протоков;
3) лечение дискинезии, которое определяется ее формой;
4) устранение диспептических проявлений.
Лечение при гипертонической форме дискинезии
1. Устранение невротических расстройств, коррекция вегетативных нарушений:
4. Прокинетики: Церукал (метоклопрамид) — 10 мг 3 раза в сутки за 1 час до еды.
5. Одестон (гимекромон) — обладает спазмолитическим действием, расслабляет сфинктер желчного пузыря, желчных протоков и сфинктер Одди, не влияя на моторику желчного пузыря — 200–400 мг 3 раза в сутки в течение 2–3 недель.
Лечение при гипотонической форме дискинезии
2. Холеретики — стимулируют желчеобразовательную функцию печени:
3. Оказывающие спазмолитическое и желчегонное действие:
4. Холекинетики — повышают тонус желчного пузыря, снижают тонус желчных путей:
6. «Слепой тюбаж» — дуоденальное зондирование и дуоденальное промывание с теплой минеральной водой, введение 20% раствора сорбита, что уменьшает или устраняет спазм сфинктеров, усиливает отток желчи — 2 раза в неделю.
Одестон эффективен в случаях одновременного наличия гипомоторной дисфункции желчного пузыря и гипермоторной дисфункции сфинктера Одди. При сочетании гиперкинетической, нормокинетической дисфункции желчного пузыря и гиперкинетической дисфункции сфинктера Одди эффективность терапии Но-шпой достигает 70–100%. При сочетании гипокинетической дисфункции желчного пузыря и гиперкинетической сфинктера Одди показано назначение Церукала или Мотилиума, возможно в сочетании с Но-шпой. При сочетании гипермоторной дисфункции желчного пузыря и гипомоторной сфинктера Одди эффективно назначение экстракта артишоков 300 мг 3 раза в сутки.
Спазмолитики являются основным медикаментозным средством для лечения гипертонических, гиперкинетических дисфункций желчного пузыря и сфинктера Одди при остром болевом приступе и болях в межприступный период. Миотропные спазмолитики оказывают целенаправленное воздействие на гладкую мускулатуру всей желчевыводящей системы. Результаты многочисленных исследований показали, что дротаверин (Но-шпа) является препаратом выбора из группы миотропных спазмолитиков, позволяет купировать болевой синдром, восстановить проходимость пузырного протока и нормальный отток желчи в двенадцатиперстную кишку, устранить диспептические нарушения. Механизм действия — ингибирование фосфодиэстеразы, блокирование Ca2+-каналов и кальмодулина, блокирование Na+-каналов, в результате снижение тонуса гладкой мускулатуры желчного пузыря и желчных протоков. Лекарственные формы: для парентерального применения — ампулы 2 мл (40 мг) дротаверина, для приема внутрь — 1 таблетка препарата Но-Шпа (40 мг дротаверина), 1 таблетка препарата Но-Шпа форте (80 мг дротаверина).
Преимущества препарата Но-Шпа:
Таким образом, обзор результатов многочисленных клинических исследований свидетельствует, что Но-шпа является эффективным препаратом для быстрого купирования спазмов и болей при гипертонических, гиперкинетических формах дискинезии желчного пузыря и сфинктера Одди.
Литература
А. С. Воротынцев, кандидат медицинских наук, доцент
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития России, Москва
Актуальность проблемы
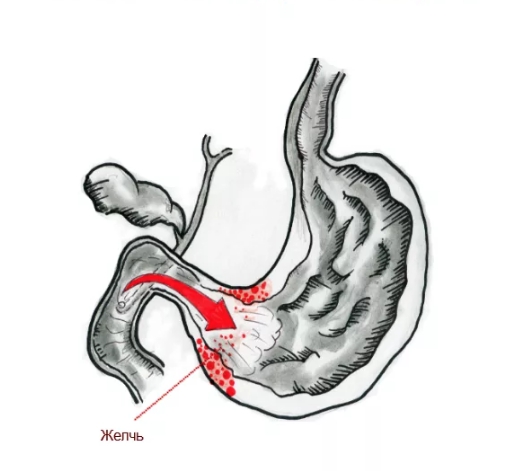
Дуодено-гастральный рефлюкс (ДГР) — одна из самых распространенных патологий верхних отделов желудочно-кишечного тракта, по данным разных источников, данное нарушение занимает 50-90% от всех заболеваний ЖКТ. Более того, за последние годы прослеживается рост количества заболевших. У пациентов с дуоденогастральным рефлюксом нередко также диагностируется хронический гастрит, в том числе рефлюкс-гастрит типа С, щелочной гастрит, язвенная болезнь желудка, функциональная диспепсия, грыжа пищеводного отверстия диафрагмы и ГЭРБ, пищевод Барретта, дуоденостаз, дисфункция сфинктера Одди, постхолецистэктомический синдром, рак желудка и целый ряд других заболеваний.
Следует знать, что ДГР способен привести к тяжелому гастриту и эзофагиту, стать причиной метаплазии желудка и пищевода, а также плоскоклеточного рака пищевода, который развивается на фоне метаплазии; это подтверждено клиническими исследованиями.
Таким образом, в результате патологического рефлюкса дуоденального содержимого в желудок течение многих органических и функциональных патологий ЖКТ может осложняться. Поэтому огромное значение должно уделяться своевременной диагностике, правильной клинической интерпретации и адекватной медикаментозной терапии.
При неэффективности консервативной коррекции показано хирургическое вмешательство, целью которого является укрепление пилорического жома, а также снижение количества забрасываемой желчи в желудок.
Есть данные о том, что на фоне ДГР желудка часто развиваются симптомы поражения системы дыхания, появляется синдром боли в грудной клетке, который не связан с коронарной патологией. Кроме того, у некоторых пациентов дуоденогастральный рефлюкс может вызвать рецидивирующий катаральный фарингит и пароксизмальный ларингоспазм. Однако у трети больных диагностируется «чистый» дуодено-гастральный рефлюкс, в этом случае можно говорить об изолированном диагнозе.
Причины дуодено-гастрального рефлюкса
Патогенетический механизм развития осложнений при ДГР
Желчь в составе рефлюксата при патологическом дуодено-гастральном рефлюксе ретроградно поступает из ДПК в органы, расположенные выше — желудок с пищеводом. Желчные кислоты, трипсин, лизолецитин — составляющие дуоденального содержимого — повреждают слизистую оболочку. Наиболее агрессивным действием при забросе дуоденального содержимого обладают желчные кислоты. Сегодня уже доказано, что при кислом рН среды лизолецитин и конъюгированные желчные кислоты (прежде всего тауриновые конъюгаты) сильнее повреждают слизистую желудка и пищевода, что определяет синергизм этих компонентов с соляной кислотой в развитии эзофагита и гастрита.
Неконъюгированные желчные кислоты и трипсин обладают более токсичным действием при слабощелочном и нейтральном рН, повреждающий эффект при дуодено-гастральном рефлюксе увеличивается при медикаментозном подавлении кислого рефлюкса. Их токсичность большей частью вызвана ионизированной формой, благодаря чему кислоты легко проникают через слизистую пищевода и желудка. Исходя из этого вполне объяснимо отсутствие адекватного ответа у 15-20% пациентов при монотерапии антисекреторными препаратами, если не будет учтен имеющийся дуодено-гастральный рефлюкс.
В результате действия на слизистую желудка желчных кислот, содержащихся в желчи, в течение длительного времени возникают изменения поверхностного эпителия желудка дистрофического и некробиотического характера, что ведет к развитию рефлюксгастрита — гастрита С. При имеющейся инфекции Нelicobacter pylori повреждающее действие рефлюксата на слизистую желудка возрастает. При наличии ДГР происходит заброс агрессивного содержимого в вышележащие отделы, что становится причиной нарушений в работе пищеварительной системы, воздействию подвергается мембранное и полостное пищеварение, возможность всасывания пищевых ингредиентов с микроэлементами и витаминами, изменяется водный баланс.
Признаком негативного воздействия ДГР являются признаки атрофии, метаплазии и дисплазии, это представляет опасность из-за риска развития рака желудка или пищевода. Кроме того, желчь в сочетании с панкреатическим соком из-за своей агрессивности разрушающе действует на слизистый барьер в желудке, при этом обратная диффузия водородных ионов усиливается. В результате этих процессов возникают эрозивные и язвенные поражения слизистой оболочки желудка.
Клинические проявления и диагностика дуодено-гастрального рефлюкса
Для ДГР характерно преобладание диспептических проявлений, пациента беспокоит отрыжка кислым содержимым или воздухом, изжога, тошнота, возможна рвота желчью, также появляется горечь во рту, которая не исчезает и даже усиливается при приеме ингибиторов протонной помпы.
Периодические боли в животе чаще схваткообразного характера, они могут возникать вследствие стресса или физической нагрузки.
Чаще дуоденогастральный рефлюкс сочетается с другими заболеваниями ЖКТ, в первую очередь с язвой желудка и ДПК, ГПОД, хроническим холециститом, панкреатитом и др. Соответственно, это отражается на симптоматике рефлюкса, существенно ее маскируя. В «чистом» виде ДГР появляется не так часто.
Дуодено-гастральный рефлюкс, в отличие от «классического» — желудочно-пищеводного рефлюкса кислой природы с изжогой, дисфагией и регургитацией — сопровождается не столь яркими клиническими проявлениями, но чаще проявляются признаки диспепсии. Кроме того, больных беспокоит боль в эпигастральной области, которая становится сильнее после приема пищи.
Диагностика основывается на результатах инструментальных методов обследования.
Лечение дуодено-гастрального рефлюкса
Консервативное лечение ДГР желудка отличается сложностью, целью терапии является нейтрализация агрессивного воздействия дуоденального содержимого на слизистую желудка и пищевода. Также в задачи лечения входит нормализация пропульсивной способности пищеварительного тракта. Назначения включают прокинетики, антациды, сорбенты, препараты урсодезоксихолевой кислоты (УДХК). При желчном рефлюксе терапия сочетается с базисным лечением основного заболевания. При этом огромное значение уделяется соблюдению диеты.
Медикаменты, используемые для устранения ДГР и восстановления моторики ЖКТ:
Следует учесть, что эритромицин в качестве прокинетика не рекомендован из-за побочных эффектов, цизаприд — не показан в клинической практике из-за вероятности нарушения сердечной проводимости, тегасерод — увеличивает вероятность инфаркта миокарда.
Фармакологическое действие домперидона (D2 антагонист) и метоклопрамида (5 НТ4 агонист и D2 антагонист) связано с блокадой рецепторов дофамина, антагонисты которых вызывают повышение тонуса нижнего сфинктера пищевода, увеличивают сократительную функцию желудка, а также препятствуют релаксации. Кроме того, благодаря антагонистам дофаминовых рецепторов улучшаются эвакуаторная способность желудка и антродуоденальная координация, что способствует устранению дуодено-гастрального рефлюкса.
Важно учесть, что клинические проявления рефлюкса с использованием медикаментозных препаратов уменьшаются, однако носят симптоматический характер. Добиться хороших результатов можно только при функциональных нарушениях, которые привели к ДГР. В остальных случаях консервативная терапия должна сочетаться с хирургическим лечением, способным устранить причину рефлюкса и укрепить пилорический клапан.
Хирургическое лечение дуодено-гастрального рефлюкса
При неэффективности консервативной терапии рекомендовано оперативное лечение, операция при этом проводится в нескольких направлениях:
При всех вышеперечисленных методиках используется лапароскопический доступ — через несколько (3-4) проколов на брюшной стенке.
Техника лапароскопической пилоропликации для уменьшения дуодено-гастрального рефлюкса
Прежде всего проводится ревизия пилородуодальной зоны, и оценивается выраженность спаечного процесса в зоне луковицы ДПК и привратника. Затем необходимо осмотреть связку Трейца, в случае необходимости она пересекается, тем самым улучшается прохождение пищи по двенадцатиперстной кишке. После ее мобилизации по Кохеру, что сделает ее более подвижной и снизит напряжение, накладываются швы в области привратника, что служит для профилактики несостоятельности.
Для пилоропликации поочередно накладываются серозно-мышечные швы симметрично к осе привратника, благодаря подобной методике передняя стенка луковицы ДПК сдвигается в проксимальном направлении, передняя полуокружность привратника погружается в просвет луковицы ДПК. Обычно четырех швов достаточно. Созданный антирефлюксный механизм способен препятствовать ДГР, не нарушая при этом эвакуации из желудка.
При необходимости проводится коррекция ГПОД или выполняется вмешательство на билиарном тракте. Следует помнить, что при лапароскопии возможно выполнение нескольких симультанных операций при наличии патологий в брюшной полости, малого таза или в забрюшинном пространстве, требующих оперативного лечения (киста почки, яичника, нефроптоз, миома и др.).
К настоящему времени нашими специалистами проведено более чем 600 оперативных вмешательств по поводу ГПОД и рефлюкс-эзофагита, а также связанных с хроническим нарушением дуоденальной проходимости. Накопленный опыт обобщен в 4-х монографиях: «Симультанные лапароскопические оперативные вмешательства в хирургии и гинекологии», «Грыжи пищеводного отверстия диафрагмы», «Ручной шов в эндоскопической хирургии» и «Технология дозированного лигирующего– электротермического воздействия на этапах лапароскопий». Кроме того, информация опубликована в многочисленных научных публикациях в разных профессиональных рецензируемых научных изданиях — российских и зарубежных.
После вмешательства на коже живота останется лишь несколько разрезов, длина которых не превышает 10 мм. Уже в день операции пациенты могут вставать, разрешается пить, на следующий день можно принимать теплую пищу в жидком виде. Клинику можно покинуть на 1-3 день — возможность выписки зависит от тяжести состояния. Но уже спустя 2-3 недели человек может вернуться к привычному образу жизни. Соблюдение строгой диеты необходимо в ближайшие два месяца, более мягкая разрешена через полгода после вмешательства. В дальнейшем человек, перенесший операцию, может обходится без медикаментов и не нуждается в строгом соблюдении диеты.
По желанию наши пациенты могут перед оперативным лечением пройти полное обследование, по результатам которого будет подобрана оптимальная тактика лечения и метод хирургического вмешательства.
На все ваши письма я отвечаю всегда только сам. Я помню, что вы доверяете мне самое ценное — свое здоровье, свою судьбу, свою семью, своих близких и делаю все возможное, чтобы оправдать ваше доверие. Каждый день я по нескольку часов отвечаю на ваши письма. Направляя мне письмо с вопросом, вы можете быть уверены, что я внимательно изучу вашу ситуацию, при необходимости запрошу дополнительные медицинские документы. Огромный клинический опыт и десятки тысяч успешных операций помогут мне разобраться в вашей проблеме даже на расстоянии.
Многим пациентам требуется не хирургическая помощь, а правильно подобранное консервативное лечение, в то время как другие нуждаются в срочной операции. И в том, и в другом случае я намечаю тактику действий и при необходимости порекомендую прохождение дополнительных обследований или неотложную госпитализацию. Важно помнить, что некоторым больным для успешной операции требуется предварительное лечение сопутствующих заболеваний и правильная предоперационная подготовка.
В письме обязательно (!) укажите возраст, основные жалобы, место проживания, контактный телефон и адрес электронной почты для прямой связи. Чтобы я мог детально ответить на все ваши вопросы, прошу высылать вместе с вашим запросом сканированные заключения УЗИ, КТ, МРТ и консультаций других специалистов. После изучения вашего случая, я направлю вам либо подробный ответ, либо письмо с дополнительными вопросами.
В любом случае я постараюсь вам помочь и оправдать ваше доверие, которое является для меня наивысшей ценностью.
_500.gif)