Бдс 12 перстной кишки что такое
Рак большого дуоденального сосочка
Рак большого дуоденального сосочка – злокачественная опухоль фатерова сосочка, расположенного в области двенадцатиперстной кишки. Характерен медленный рост и позднее метастазирование при раннем появлении механической желтухи. Наблюдаются боли, периодическое повышение температуры тела, увеличение печени и желчного пузыря. На поздних стадиях возможны кровотечения. Диагноз устанавливают с учетом симптоматики, данных рентгенографии, фиброгастродуоденоскопии и результатов биопсии. Лечение оперативное: гастропанкреатодуоденальная резекция, папиллэктомия, дуоденэктомия, паллиативные вмешательства.
Общие сведения
Рак большого дуоденального сосочка – злокачественная неоплазия большого дуоденального (фатерова) соска, локализующегося в нисходящей части двенадцатиперстной кишки и представляющего собой соустье главного панкреатического протока и общего желчного протока. Составляет 40% от общего количества онкологических поражений пилородуоденальной зоны, 5% от общего числа неоплазий ЖКТ и 1-2% от общего количества раков различных локализаций. Рак большого дуоденального сосочка является третьей по распространенности причиной возникновения механической желтухи. Обычно поражает пожилых пациентов, средний возраст больных составляет 54 года. Очень редко выявляется у детей. Женщины страдают реже мужчин. Лечение осуществляют специалисты в сфере онкологии, гастроэнтерологии и абдоминальной хирургии.
Причины рака фатерова сосочка
Причины возникновения опухоли точно не выяснены. Специалисты отмечают, что определенное значение имеет наследственная предрасположенность – заболевание нередко диагностируется в семьях, члены которой страдают семейным полипозом. Кроме того, у некоторых пациентов выявляется генетическая мутация K-ras. Установлено, что неоплазия может развиться в результате малигнизации аденомы фатерова соска. В список факторов риска также включают хронический панкреатит и заболевания гепатобилиарной системы.
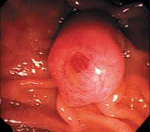
Источником рака большого дуоденального сосочка являются трансформировавшиеся клетки эпителия слизистой двенадцатиперстной кишки, панкреатического протока либо общего желчного протока. Для новообразования характерен медленный экзофитный рост. По внешнему виду неоплазия напоминает папиллому, разрастание грибовидной формы или в виде соцветья цветной капусты. Реже выявляются эндофитные формы. При экзофитных формах рака большого дуоденального сосочка желтуха чаще ремиттирующая, при эндофитных – постоянная. Диаметр узла при его хирургическом удалении в среднем составляет 3 мм.
При микроскопическом исследовании выявляются клеточные скопления и отдельно лежащие эндокринные клетки веретенообразной, треугольной и цилиндрической формы. Число эндокринных клеток уменьшается по мере снижения уровня дифференцировки неоплазии. Обычно рак большого дуоденального сосочка прорастает общий желчный проток, возможно также поражение поджелудочной железы и стенки двенадцатиперстной кишки, лимфогенное и отдаленное метастазирование. Лимфогенные метастазы обнаруживаются у 21-51% больных. Отдаленные вторичные очаги выявляются достаточно редко. Обычно поражается печень, реже – кости, головной мозг, легкие и надпочечники.
Рак большого дуоденального сосочка может полностью обтурировать просвет желчного протока, реже выявляется стеноз. Даже при частичном сдавлении из-за отечности слизистой возникают грубые расстройства оттока желчи, становящиеся причиной развития механической желтухи. Появляется билиарная гипертензия, сопровождающаяся дилатацией желчевыводящих путей и протоков поджелудочной железы. Кишечная непроходимость развивается очень редко. При распространении процесса возможно прорастание стенки кишечника и распад неоплазии с развитием внутреннего кровотечения.
Симптомы рака фатерова сосочка
Первым проявлением болезни часто становится механическая желтуха, возникшая на фоне соматического благополучия. Вначале желтуха обычно перемежающаяся, нормализация биохимических показателей крови обусловлена уменьшением отека в области стенозированного желчного протока. При прогрессировании рака большого дуоденального сосочка желтуха становится более стойкой, изменение цвета кожи выявляется после интенсивных болей, сопровождающихся ознобами и проливными потами. Пациенты жалуются на выраженный зуд. Интермиттирующий характер желтухи на поздних стадиях (выявляется в 51% случаев) обусловлен распадом рака большого дуоденального сосочка, сопровождающегося временным восстановлением проходимости желчного протока.
При пальпации определяется гепатомегалия. У 60% пациентов под нижним краем печени прощупывается увеличенный желчный пузырь (симптом Курвуазье). При продолжительной обтурации желчевыводящих путей возникают цирроз печени и хронический панкреатит. При инвазии рака большого дуоденального сосочка в стенку кишечника и последующем распаде опухоли возможны кровотечения (острые массивные либо повторяющиеся незначительные) с развитием анемии. При региональном метастазировании отмечается изменение болевого синдрома.
Характерной особенностью рака большого дуоденального сосочка является ранняя потеря веса. Причиной похудания становятся стеноз либо обструкция панкреатических протоков, из-за которых в ЖКТ перестают поступать ферменты, необходимые для расщепления белков и жиров. Нарушение проходимости общего желчного протока еще больше усугубляет расстройства всасывания жиров и ухудшает всасываемость витаминов. Снижение веса и авитаминоз становятся причиной адинамии.
У больных раком большого дуоденального сосочка часто наблюдаются поносы, сопровождающиеся вздутием и болями в животе. Каловые массы зловонные, глинисто-серые. В запущенных случаях может выявляться жировой кал. При появлении регионарных метастазов отмечается изменение характера болевого синдрома. На поздних стадиях определяются истощение и расстройства функций органов, пораженных отдаленными метастазами.
Диагностика рака фатерова сосочка
Постановка диагноза сопряжена с существенными затруднениями из-за неспецифичности симптоматики. В процессе диагностики онколог ориентируется на жалобы, данные объективного осмотра, рентгенографии, чреспеченочной или внутривенной холангиографии, дуоденального зондирования, фиброгастродуоденоскопии и других исследований. При желтухе определяется высокий уровень билирубина с преобладанием прямой фракции, стеркобилин в кале отсутствует. На поздних стадиях рака большого дуоденального сосочка выявляется анемия.
Достаточно достоверным исследованием является дуоденальное зондирование, при проведении которого часто удается обнаружить кровь в дуоденальном содержимом. Иногда в ходе этого исследования выявляются клетки неоплазии и ферменты поджелудочной железы. Рентгенографическими признаками рака большого дуоденального сосочка являются неровность контуров либо дефект наполнения в зоне внутренней стенки двенадцатиперстной кишки, а также отсутствие проходимости либо деформация желчного протока в зоне, приближенной к фатеровому соску.
При проведении фиброгастродуоденоскопии обнаруживают опухолевидное образование и выполняют эндоскопическую биопсию подозрительного участка. В некоторых случаях диагноз рака большого дуоденального сосочка не удается установить при помощи стандартных методик, для уточнения характера патологии приходится проводить лапаротомию, рассекать фатеров сосок, осуществлять забор ткани, а затем принимать решение об объеме операции на основании данных срочного гистологического исследования. Дифференциальный диагноз осуществляют с гепатитом, раком головки поджелудочной железы и раком желчных путей.
Лечение рака фатерова сосочка
Основным способом лечения данной патологии является оперативное вмешательство, которое, в зависимости от распространенности процесса, может быть радикальным либо паллиативным. Группа паллиативных операций включает в себя около десяти различных вариантов анастомозов, позволяющих восстановить отток желчи в пищеварительный тракт либо (реже) предотвратить сдавление двенадцатиперстной кишки растущим раком большого дуоденального сосочка.
Радикальная операция является тяжелым и сложным вмешательством, поэтому проводится только после тщательного отбора пациентов в соответствии со стандартами, включающими в себя допустимую степень истощения, уровень белков в крови, определенные показатели пульса и жизненной емкости легких и т. д. Больным раком большого дуоденального сосочка проводят гастропанкреатодуоденальную резекцию. При наличии противопоказаний к радикальному вмешательству выполняют условно радикальные операции: папиллэктомию, дуоденэктомию либо экономную панкреатодуоденальную резекцию. Радиотерапия и химиопрепараты при раке большого дуоденального сосочка малоэффективны.
Бдс 12 перстной кишки что такое
Известно, что изменения структуры БДС могут видоизменяться с учетом возрастных особенностей. По данным Пушкарского В.В. (2004) при желчнокаменной болезни в пожилом и старческом возрастах преобладают атрофическо-склеротическая форма хронического папиллита (до 54 % случаев), в возрасте до 60 лет преобладают гиперпластические (аденоматозные, аденомиоматозные) изменения БДС.
Повышенное внимание к острым и хроническим воспалительным изменениям БДС не случайно. По мнению Едемского А.И. (2002) острый и хронический папиллит наблюдается у 100% больных, страдающих желчнокаменной болезнью и у 89,6 % пациентов с рецидивирующим панкреатитом. Хронические воспалительные изменения сосочка подразделяют на три формы: аденоматозный хронический папиллит, аденомиоматозный и атрофическо-склеротическая форма хронического папиллита.
Анализ эндоскопического биопсийного и операционного материала поступившего в патологоанатомическое отделение ГКБ № 31 за период с 2002 по 2004 гг. показал, что морфологический спектр патологических изменений БДС чрезвычайно широкий. В случаях патологии желчевыводящих путей и поджелудочной железы, а также в пожилом и старческом возрастах в БДС наблюдаются выраженные как гиперпластические и метапластические, так и атрофические изменения желез сосочка вследствии воспалительных процессов: на ранних этапах возникает отек, острая воспалительная инфильтрация, в дальнейшем развивается гипертрофия, а затем деформация и атрофия клапанов. Значительную часть (379 наблюдений 87%) занимают воспалительные процессы, преимущественно хронического течения. Часто хронические папиллиты сопровождаются гиперпластическими изменениями различных структур элементов слизистой оболочки: клапанов, переходной складки, папиллярных желез. Большая доля представлена гиперпластическими полипами устья и интраампулярной части БДС (174 наблюдения 46%). Железисто-кистозная гиперплазия встретилась в меньшем количестве наблюдений (23 случая 6%). Среди хронических папиллитов наиболее часто встречающаяся форма атрофическо-склеротическая, за данный период времени она встретилась в 67 наблюдениях (40%). Аденомиоз относится к группе гетеротопических процессов и считают, что он развивается вследствие пермещения гиперплазированных желез в мышечный слой сосочка. В зависимости от особенностей строения различают три, последовательно развивающиеся гистологические формы: узловатая, являющаяся ранней фазой развития, узловато-диффузная и далее диффузная фрорма аденомиоза. По нашим данным аденомиоз встретился за истекший период всего в 11 наблюдениях (2%).
Ряд аспектов, касающихся морфологических особенностей БДС в полной мере не разработан. К их числу относится гистогенетическая и цитологическая квалификация его эпителиальных структур. Вопрос о дуоденальной или протоковой природе эпителия сосочка остается дискуссионным (Медведева М.С., Саввина Т.В. 1993г). Между тем, гистогенетическая принадлежность эпителия определяет биологические
свойства опухолей и опухолеподобных изменений, ранние стадии которых могут симулировать дисфункции БДС. Источником злокачественного роста могут быть слизистая оболочка дистального отдела холедоха, конечных отделов панкреатического протока, двенадцатиперстной кишки, эпителий самого БДС (Блохин Н.Н. с соавт., 1981, Шалимов С.А., 1985г). Первые две формы большинство морфологов относят к протоковому или панкреатобилиарному типу рака фатерова соска, остальные же к кишечному (Howe J.R. 1998, Ficher H.P., et al., 2003). На долю последних приходится 53-63% всех ампулярных неоплазм, протоковые же составляют 20-27% (Howe J.R., et al.,1998). Доминирующим гистологическим типом злокачественной опухоли БДС является простая аденокарцинома различной степени дифференцировки, на долю которой приходится до 70% всех случаев, причем в большинстве случаев карцинома БДС является высокоили умеренно дифференцированной.
По нашим данным эпителиальные новообразования БДС представлены папиллярными аденомами (21 наблюдение) из них 8 случаев (38%) с малигнизацией по типу аденокарциномы, преимущественно умеренной степени дифференцировки, а также аденокарциномами различной степени дифференцировки (26 наблюдений, из них умереннодифференцированные21 случай). Кроме того, в одном случае была диагностирована зернистоклеточная опухоль БДС.
Таким образом, патология БДС как воспалительного, так и опухолевого генеза приводит часто к тяжелым осложнениям, требующим нередко экстренного оперативного лечения. Одновременно крайне важна квалифицированная морфологическая диагностика патологического процесса данного анатомического образования играющего в последующем ведущую роль в выборе тактики и обьема хирургического вмешательства.
Опухоль большого дуоденального сосочка как причина рецидивирующего холедохолитиаза.
М.А. Евсеев, А.Л. Владыкин, Ю.А. Бирюкова, В.Е. Никитин. Представлено клиническое наблюдение рецидивного холедохолитиаза, связанного с развитием опухоли большого дуоденального сосочка на фоне суб- декомпенсированного рубцового стеноза пилоробульбарного сегмента; описаны этапы инструментальной диагностики и интраоперационная тактика в процессе лечения. Хирургическая практика. 2015, №1.
Рецидивный и резидуальный холедохолитиаз как много десятилетий назад, так и сегодня является по-прежнему трудным для диагностики и лечения осложнением желчнокаменной болезни (ЖКБ). По сводным данным литературы частота резидуальных и вновь сформированных камней желчных протоков с течением времени не уменьшается и может достигать 29%. Причины возникновения рецидивного и резидуального холедохолитиаза разнообразны. Тем не менее ведущим этиопатогенетическим фактором данной патологии по всеобщему мнению является недостаточный объем до- и интраоперационного обследований желчных путей и, как следствие, не диагностированные в предоперационном периоде и на операции холедохолитиаз, патология терминального отдела холедоха, большого дуоденального сосочка и головки поджелудочной железы. Последние три причины определяют возникновение, как правило, не резидуальных, а рецидивных конкрементов в желчевыводящих протоках. В качестве примера рецидивного холедохолитиаза, обусловленного развитием злокачественной опухоли большого дуоденального сосочка, приводим следующее клиническое наблюдение.
Из анамнеза известно, что в 2013 году пациентка находилась на лечении в ГКБ № 5х города Москвы по поводу хронического калькулезного холецистита, холедохолитиаза, субкомпенсированного рубцово-язвенного стеноза пилоро-бульбарной зоны. В период госпитализации после безуспешных попыток выполнения ретроградной холангиопанкреатографии (РХПГ), эндоскопической папиллосфинктеротомии (ЭПСТ) и литоэкстракции пациентка была оперирована. Произведены срединная лапаротомия, холецистэктомия, холедохолитотомия, дренирование холедоха по Керу, пилоропластика по Гейнеке — Микуличу. Послеоперационный период протекал гладко, пациентка была выписана в обычные сроки, дренаж Кера удален через три недели.
Повторное возникновение желтухи с эпизодами гипертермии пациентка отметила в последней декаде декабря 2014 года, по поводу чего в срочном порядке 31. 12. 14 была госпитализирована в ГКБ № 1х города Москвы, где диагноз механической желтухи был верифицирован, но активных хирургических действий не предпринималось.
Пациентка покинула ГКБ № 1х и самостоятельно обратилась в хирургическое отделение ГКБ № 52. На момент госпитализации в ГКБ № 52 06. 01. 15 факт механической желтухи и холангита был подтвержден клинически, данными УЗИ (билиарная гипертензия, холедохолитиаз), лабораторно (прямой билирубин 432 мкмоль/л, общий билирубин 464 мкмоль/л), гектической лихорадкой, лейкоцитозом (до 14, 6 х 109/л) ; кроме того пациентка периодически отмечала возникновение чувства переполнения в эпигастрии при приеме твердой пищи, редко — рвоту съеденной пищей.
Пациентке выполнена фиброэзофагогастроскопия, при которой выявлен суб- декомпенсированный стеноз пилоробульбарного сегмента (аппарат 9 мм через зону стеноза провести не удалось, просвет двенадцатиперстной кишки не визуализирован), органической патологии со стороны пищевода и желудка выявлено не было. При экспертном УЗИ гепатобилиопанкреатической зоны наряду с дилатацией холедоха и множественным холедохолитиазом в области головки поджелудочной железы, но не в ее ткани, нечетко лоцировалось мягкотканное образование 2 х 2 см.
В экстренном порядке 06. 01. 15 пациентке под УЗ-контролем произведена чрезкожная чреспеченочная холангиостомия (ЧЧХС), дренаж 12 Fr через левый долевой проток установлен в гепатикохоледох, получена темная желчь с хлопьями фибрина. Пациентке проводилась комплексная дезинтоксикационная, антибактериальная терапия, дозированная билиарная декомпрессия, сбалансированная энтральная и парентеральная нутритивная поддержка. Через 7 суток на фоне снижения гипербилирубинемии до 62 мколь/л пациентке проведена чрездренажная холангиография, при которой выявлены множественные крупные конкременты общего желчного протока, дислоцированные от супрадуоденального до терминального его отделов, блок поступления контраста в двенадцатиперстную кишку; оценить состояние стенок интрапанкреатического и интрадуоденального отделов холедоха не представлялось возможным. В удовлетворительном состоянии без явлений интоксикации с функционирующим наружным желчным свищом (дебит желчи 600 мл/сут) пациентка была выписана для проведения амбулаторной реабилитации с рекомендацией последующей госпитализации через 14 суток для проведения радикального хирургического лечения.
25. 01. 15 пациентка вновь самостоятельно обратилась в ГКБ № 52 и была госпитализирована в хирургическое отделение. На момент повторной госпитализации состояние пациентки клинически и по данным лабораторных исследований было расценено как удовлетворительное, явления желтухи и холангита клинически регрессировали полностью. Дополнительно в плане обследования больной выполнена рентгеноскопия желудка с контрастом, при которой контраст задерживался в желудке более 6 часов, опрдлялись признаки суб- декомпенсированного стеноза пилоробульбарной зоны, вследствие чего добиться тугого заполнения контрастом просвета двенадцатиперстной кишки и оценить состояние ее слизистой не удалось.
При проведении компьютерной томографии органов брюшной полости и забрюшинного пространства визуализирован умеренно дилатированный холедох с равномерно утолщенными стенками и множественными крупными конкрементами в просвете, расширение вирсунгова протока на всем протяжении до 0, 9 см, мягкотканное образование стенки двенадцатиперстной кишки в области интактной головки поджелудочной железы 2, 5 х 2, 5 см с тенденцией к накоплению контраста в артериальную фазу.
Таким образом на основании комплексного обследования у пациентки диагностированы рецидивный холедохолитиаз, суб-декомпенсированный рубцовый стеноз пилоро-бульбарного сегмента, состояние после наружного дренирования желчных протоков, полный наружный желчный свищ, опухоль большого дуоденального сосочка (?). Учитывая установленный клинический диагноз, включающий как рецидивный холедохолитиаз, так и стеноз пилоробульбарного сегмента при невозможности консервативного разрешения данных патологических состояний, а также невозможность неинвазивной оценки состояния терминального отдела холедоха и исключения опухолевого процесса в данной зоне, принято решение о необходимости проведения оперативного вмешательства. Предполагаемый объем вмешательства: дистальная резекция 2/3 желудка по Ру с холедохолитотомией и билиодигестивным анастомозом — минимальный, гастропанкреатодуоденальная резекция (ГПДР) — максимальный.
После подписания информированного согласия пациентка была оперирована в плановом порядке. При выполнении верхне-срединной лапаротомии, проведения адгезиолизиса, ревизии органов брюшной полости и выполнении диагностической дуоденотомии установлен следующий интраоперационный диагноз: Рак большого дуоденального сосочка oT3N1M0 (IIB стадия), регионарная лимфаденопатия ретропанкреатических узлов; рецидивный холедохолитиаз, состояние после холецистэктомии, дренирования холедоха от 2013 года, состояние после ЧЧХС от 06. 01. 15; суб- декомпенсированный рубцовый стеноз пилоро-бульбарного сегмента, состояние после пилоропластики по Гейнеке-Микуличу от 2013г.
Учитывая интраоперационный диагноз принято решение о выполнении вмешательства в объеме ГПДР. Произведена гастропанкреатодуоденальная резекция с регионарной лимфаденэктомией. Реконструкция производилась с формированием панкреатико-гастроанастомоза, гепатико-энтероанастомоза на выключенной по Ру петле и поперечного функционального полуклапанного гастро-энтероанастомоза.
Ведение пациентки в послеоперационном периоде проводилось по программе ERAS (Enhansed Rehabilitation After Surgery) с ранним (на 2-е сутки) началом энтерального питания и активизацией больной. Ранний послеоперационный период у пациентки протекал гладко. На 7-е сутки послеоперационного периода пациентка после проведения контрастного исследования пищеварительного тракта и удаления холангиостомического дренажа выписана на амбулаторную послеоперационную реабилитацию с полным восстановлением пищеварительной функции. Рекомендовано проведение адъювантной полихимиотерапии под наблюдением врача-онколога, а также опроеделение возможности проведения таргетной биотерапии после иммуногистохимического анализа на р53 и KRAS.
Таким образом, причиной возникновения рецидивного холедохолитиаза у пациентки Р. послужило длительное и прогрессирующее нарушение пассажа желчи в терминальном отделе холедоха вследствие развития опухоли большого дуоденального сосочка. Интересность данного клинического наблюдения, на наш взгляд, обусловлена редким сочетанием трех патологических процессов — опухоли большого дуоденального сосочка, рецидивирующим холедохолитиазом и рубцовым стенозом пилоро-бульбарного сегмента. Последний сделал очевидно невозможной дооперационную верификацию опухолевого процесса и определения первопричины рецидива патологии билиарного тракта.
Проведенное в объеме гастропанкреатодуоденальной резекции оперативное вмешательство явилось радикальным методом лечения как с точки зрения имеющегося онкологического процесса, так и с точки зрения обеспечения максимально адекватного функционирования желудка, билиарного тракта и поджелудочной железы (рис. 7). Последний момент особенно интересен, поскольку формирование именно панкреатико-гастроанастомоза имеет целый ряд позитивных особенностей, среди которых наиболее важными являются: возможность сохранения большей части желудка (выполняется антрумрезекция) без опасности развития его острого эрозивно-язвенного поражения вследствие защитного ощелачивающего действия бикарбонатов панкреатического сока; отсутствие активации панкреатических ферментов в кислой среде желудка при отсутствии энтерокиназы; пространственное разделение билио- и панкреатикодигестивного анастомозов, что принципиально уменьшает риск несостоятельности последнего. Мы полагаем, что именно такой вариант реконструкции позволяет добиться максимально быстрой и эффективной реабилитации пациента в послеоперационном период, в том числе после вмешательств большого объема, что и продемонстрировало приведенное клиническое наблюдение.
Касаткин В. Ф. Пути улучшения непосредственных результатов панкреатодуоденальной резекции при периампулярном раке. Хирургия. 2008; 10; 10–15.
Bang BW, Lee TH, … Jeong S. Twenty-Second versus Sixty-Second Dilation Duration in Endoscopic Papillary Balloon Dilation for the Treatment of Small Common Bile Duct Stones: A Prospective Randomized Controlled Multicenter Trial. Clin Endosc 2015; 48 (1): 59-65
Parra-Membrives P, Díaz-Gómez D, Vilegas-Portero R, et al. Appropriate management of common bile duct stones: a RAND Corporation/UCLA Appropriateness Method statistical analysis. Surg Endosc 2010 May; 24 (5): 1187-94.
Статья добавлена 13 января 2016 г.