Ацинетобактер баумании чем лечить
Ацинетобактер баумании чем лечить
Acinetobacter spp. относится к микроорганизмам, свободно живущим в окружающей среде (сапрофиты), па различных объектах в лечебных учреждениях, в воде, пищевых продуктах. Помимо этого Acinetobacter spp. выделяется из различных биотопов (например, с кожи, слизистой оболочки) человека.
Присутствие Acinetobacter spp. в биоматериалах от пациента, находящегося в стационаре, может быть как следствием колонизации слизистых оболочек и кожи, так и причиной инфекционных осложнений различной локализации. У 25% взрослых людей имеет место колонизация кожи, а у 7% детей колонизированы верхние дыхательные пути. Acinetobacter spp., так же как и P. aeruginosa, способна месяцами находиться на различных объектах окружающей среды в жизнеспособном состоянии.
Кроме того, Acinetobacter spp. устойчива ко многим бактерицидным растворам, например к хлоргексидину.
По данным CDC (NNIS), за последние 20 лет значение неферментирующих грамотрицательных палочек рода Acinetobacter как возбудителей НКИ значительно позросло во всем мире. При хирургических вмешательствах Acinetobacter spp. выделяют из гнойных ран в 2,1 % случаев. Вид A. baumannii составляет 80% всех видов этого рода, ответственных за ЕКИ, и поэтому выделение любого другого вида этого рода дает основание предполагать, что имеет место коптам и нация исследуемого биоматериала.
Повторное выделение Acinetobacter spp. из любых биоматериалов важно для исключения контаминации или колонизации и, в конечном счете, для правильной трактовки полученных результатов микробиологических исследований. Следует заметить, что наиболее часто Acinetobacter spp. выделяют при пневмонии (Acinetobacter spp. составляет 6,9% всех возбудителей при этой локализации), особенно если ей предшествовала колонизация слизистых верхних дыхательных путей. Летальность при пневмонии, обусловленной Acinetobacler spp., составляет 40-64%.
Наряду с другими микробами-оппортунистами (такими, как S. maltophilia) Acinetobacter spp. отличается высокой резистентностью к большинству антимикробных препаратов, хотя имеются существенные различия по антибиотикорезистентности штаммов в разных странах и регионах. В настоящее время, по сообщениям различных авторов, большинство штаммов А. baumannii резистентно ко многим классам антимикробных препаратов. Фторхинолоны, тигециклин, цефтазидим, триметоприм/сульфаметоксазол, доксициклин, имипенем, меропенем, дорипенем, полимиксин В и колистин до недавнего времени считались активными против госпитальных штаммов A. baumannii.
Быстрое развитие резистентности A. baumannii к большинству антибиотиков (МDR-Acinetobacter) регистрируется во всем мире. Сульбактам имеет более высокую природную бактерицидную активность против MDR-Acinetobacter в сравнении с тазобактамом и клавулановой кислотой, в то же время отмечается увеличение резистентности и к сульбактаму. Комбинация имипенема с амикацином в исследованиях in vitro показала синергизм в отношении MDR-штаммов, тогда как in vivo эффект менее выражен. Комбинация фторхинолонов с амикацином приемлема, когда имеет место низкая МПК фторхинолонов для госпитальных штаммов A baumannii.
При выделении штаммов МDR-A. baumannii применяют комбинацию полимиксипа В с рифампицином (или с имипенемом, или с азитромицином). Имеется небольшое количество исследований по применению тигециклина для лечения инфекций, обусловленных A. baumannii, но уже сейчас использование этого антибиотика связывают с постепенным увеличением резистентности. По данным из Германии, резистентность к тигециклину среди A. baumannii составляет 6%, тогда как к кол истину — 2,8%.
По данным SENTRY 2001-2004 гг. (30 стран Европы), доля штаммов Acinetobacter spp., резистентных к имипенему, меропенему, ампициллину/сульбактаму и полимиксину В составляет 26,3, 29,6, 51,6 и 2,7% соответственно. Важно отметить, что даже в странах с низким уровнем резистентности феномен распространения MDR-, XDR- или PDR-штаммов A. baumannii пока неясен. Одним из факторов риска MDR-A. baumannii считается назначении карбапенемов и цефалоспоринов III поколения.
Кроме того, риск связан с искусственной вентиляцией легких (ИВЛ), длительным пребыванием в реанимации, оперативным вмешательством, контаминацией окружающих объектов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Acinetobacter baumannii

Acinetobacter baumannii широко распространены в природе, а также во внутрибольничной среде и обладают множественными механизмами резистентности к антибиотикам. Acinetobacter baumannii могут колонизировать желудочно-кишечный тракт, кожу пациента, рото- и носоглотку, конъюнктиву, влагалище и уретру.
В то же время Acinetobacter baumannii могут являться причиной пневмонии, трахеобронхита, сепсиса, инфекций мочевыводящих путей, эндокардита, раневой и хирургической инфекции, инфекций кожи и мягких тканей (включая некротизирующий фасциит), менингита, вентрикулита, абсцессов мозга, интраабдоминальных абсцессов, хориоамнионита, остеомиелита, артрита, синусита и перитонита.
Acinetobacter baumannii — возбудитель внутрибольничных инфекций
Проблема нозокомиальных (внутрибольничных) инфекций, вызываемых Acinetobacter baumannii, становится всё более актуальной из-за растущей резистентности данных микроорганизмов к антибактериальным препаратам. Резистентность Acinetobacter baumannii к цефтазидиму и ампициллину/сульбактаму за 5 лет увеличилась в 2–2,5 раза, к амикацину и ципрофлоксацину — в 8–9 раз. Встречаются штаммы, резистентные ко всем применяемым антибактериальным препаратам. Появление таких устойчивых внутрибольничных микроорганизмов связано с необоснованным и неограниченным использованием антибиотиков.
Acinetobacter baumannii вызывает 2-10 % всех грамотрицательных инфекций в Европе и США и до 1% всех внутрибольничных инфекций. В России Acinetobacter baumannii, наряду с Pseudomonas aeruginosa и Klebsiella pneumoniae, относится к трём самым часто происходящим и опасным возбудителям нозокомиальных инфекций. Во внутрибольничных условиях вспышки инфекций, вызываемые Acinetobacter baumannii в 60% случаев происходят во «взрослых» отделениях реанимации и интенсивной терапии. Оставшиеся 40% приходятся на отделения реанимации и интенсивной терапии новорожденных, ожоговые, нейрохирургические, хирургические, онкологические и гематологические отделения. Способствующими факторами являются: организация работы в этих отделениях – широкое использование инвазивных диагностических и лечебных мероприятий (катетеризация магистральных сосудов, искусственная вентиляция лёгких, длительная инфузионная терапия, энтеральное питание, методы внепочечного очищения крови), высокая концентрация больных с тяжелыми заболеваниями и сниженной иммунологической защитой, широкое и часто нерациональное использование антибактериальных и кортикостероидных препаратов, цитостатиков. Acinetobacter baumannii в большинстве случаев вызывает заболевания у тяжелобольных иммуноскомпрометированных пациентов (Ю.Л. Горбич, И.А. Карпов, 2012).
Acinetobacter baumannii относится к основными возбудителями раневых инфекций (Д.О. Вагнер).
Acinetobacter baumannii в систематике бактерий
Антибиотики, активные в отношении Acinetobacter baumannii
В течение многих лет основой терапии инфекций, вызванных Acinetobacter baumannii, были бета-лактамные антибиотики, часто в сочетании с аминогликозидами в случаях тяжелых инфекций. Однако большинство внутрибольничных Acinetobacter baumannii в настоящее время устойчивы к этим препаратам. Фторхинолоны, тетрациклины и глицилциклин, триметоприм-сульфаметоксазол, карбапенемы (за исключением эртапенема), полимиксины могут сохранять активность в отношении некоторых внутрибольничных штаммов. Однако в большинстве стран наблюдается быстрое нарастание резистентности к этим группам антибиотиков. В настоящее время наиболее клинически и финансово эффективным является использование монотерапии ампициллином/сульбактамом в дозах 24 г/сут или комбинированных режимов, включающих карбапенемы и ампициллин/сульбактам или карбапенемы и цефоперазон/сульбактам и нетилмицин. Последняя комбинация является экономически менее выгодной (Н.Д. Дмитриева и др., 2012).
По данным отечественного проекта «РЕЗОРТ», наибольшую активность в отношении 459 протестированных нозокомиальных штаммов Acinetobacter baumannii проявляли цефоперазон/сульбактам, имипенем и меропенем (2,2, 2,2 и 3,5% устойчивых изолятов соответственно), наименьшую – цефоперазон, гентамицин и пиперациллин (97,8, 89,1 и 91,7% соответственно) (Козлов С.Н., Белькова Ю.А. ).
Из представленных в данном справочнике антимикробных средств в отношении Acinetobacter baumannii (в общем) активны: левофлоксацин, нифурател, доксициклин. Acinetobacter baumannii устойчив к рокситромицину.
Ацинетобактер
Автор: врач – клинический фармаколог Трубачева Е.С.
Автор: врач – клинический фармаколог Трубачева Е.С.
Если еще каких-то 7 лет назад ацинетобактер была зверем, о котором знали реаниматологи крупных больниц да клинические фармакологи, то менее пяти лет назад ситуация кардинально изменилась – теперь про ацинетку знают все, кто в том или ином виде работает в стационарах. Она очень быстро заместила собой всю предыдущую внутрибольничную микрофлору и фактически вышла на первый план самых проблемных внутрибольничных микробов, заняв чуть ли не основную нишу ВБИ.
Автор сразу хотел бы предупредить, что речь здесь пойдет не столько об Acinetobacter baumannii, сколько о семействе ацинетобактеров, ибо клиническую значимость имеет не только вышеупомянутый возбудитель.
Ацинетобактеры являются представителями тройки основных опасных возбудителей согласно определению ВОЗ. Двух других представителей из этого списка мы уже обсудили: это синегнойная палочка и энтеробактерии (клебсиелла, кишечная палочка, энтерококки). Именно для этой могучей тройки в первую очередь и должны разрабатываться новые антибиотики, но пока с этим как-то не очень.
Микробиологические аспекты
Ацинетобактер (или ацинетка, как любит обзывать ее автор), является фактически «кровной родней» другого общеизвестного неферментера – синегнойной палочки. Но, в отличие от синегнойки, природно-устойчивого ацинетобактера вам могут принести прямо с улицы. То есть в природе имеются штаммы, и в очень большом количестве, которые изначально природно-устойчивы фактически ко всему арсеналу имеющихся в медицине антибиотиков. А еще таких же, но уже внутрибольничных мутантов не менее «удачно» выращивают в отделениях с высокой частотой использования антибактериальных препаратов. И это при том, что принести такого микроба в больницу, а также занести его в больного, может вообще любой человек, так как изначально ацинетка, как и синегнойка, является почвенным микробом, а потому горшки с цветами, садоводы-огородники, зимой растящие рассаду, летом ковыряющиеся на даче, а потом, нормально не отмыв руки, начинающие перевязывать раны или менять катетеры, да просто посетители с пылью на ботинках – все они в каждый момент времени приносят в больницы миллиарды подобных микробов. И это как раз то, о чем автор упоминал в разговоре о клебсиелле – вывести ацинетку, в отличие от синегнойки, несопоставимо труднее. Напомню, синегнойка предпочитает мокрую теплую грязь, поэтому ее проще отсечь от заноса в чистые отделения и внутри самой больницы проще выбить. А теперь представьте, чего будет стоить избавиться от пыли, комнатных растений, любителей-огородников и ломящихся, теперь уже даже в реанимации, посетителей. Практически нереально, если это только не ламинарный бокс.
Поэтому будем изучать врага в лицо
Общее представление о том, что из себя представляют дикие и непуганые антибиотиками ацинетобактеры, можно составить на EUCAST. Для тех, кто никогда не пользовался данным ресурсом, небольшая подсказка – тыкаем мышкой (или пальцем, смотря откуда читаете этот опус) в плашку «Species», выбираем один из 25-ти ацинетобактеров и наслаждаемся изучением. Общую антибиотикочувствительность семейства Acinetobacter spp. можно рассмотреть тут. Небольшое пояснение для тех, кто здесь впервые, – клинически значимыми минимальными подавляющими концентрациями (MIC), которыми можно и нужно пользоваться в клинической практике (а также как маркер того, какие антибиотики будут работать, а какие нет – их MIC указаны с чисто исследовательскими целями), являются показатели, отмеченные синими клеточками. На эти же показатели настроены аппараты для определения антибиотикочувствительности, с помощью которых продемонстрированы антибиотикограммы в наших статьях.
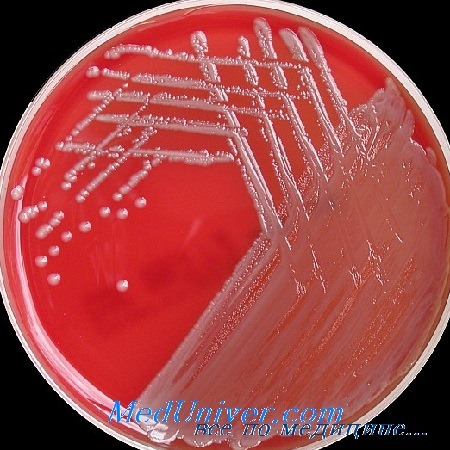
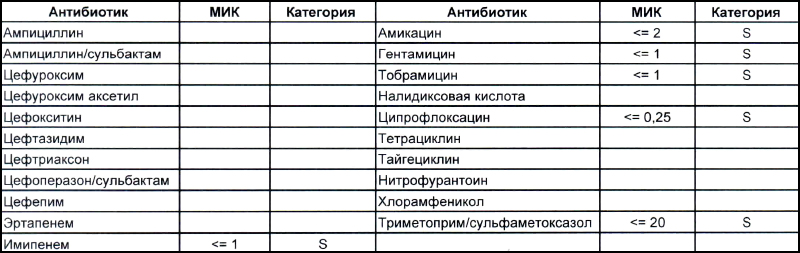
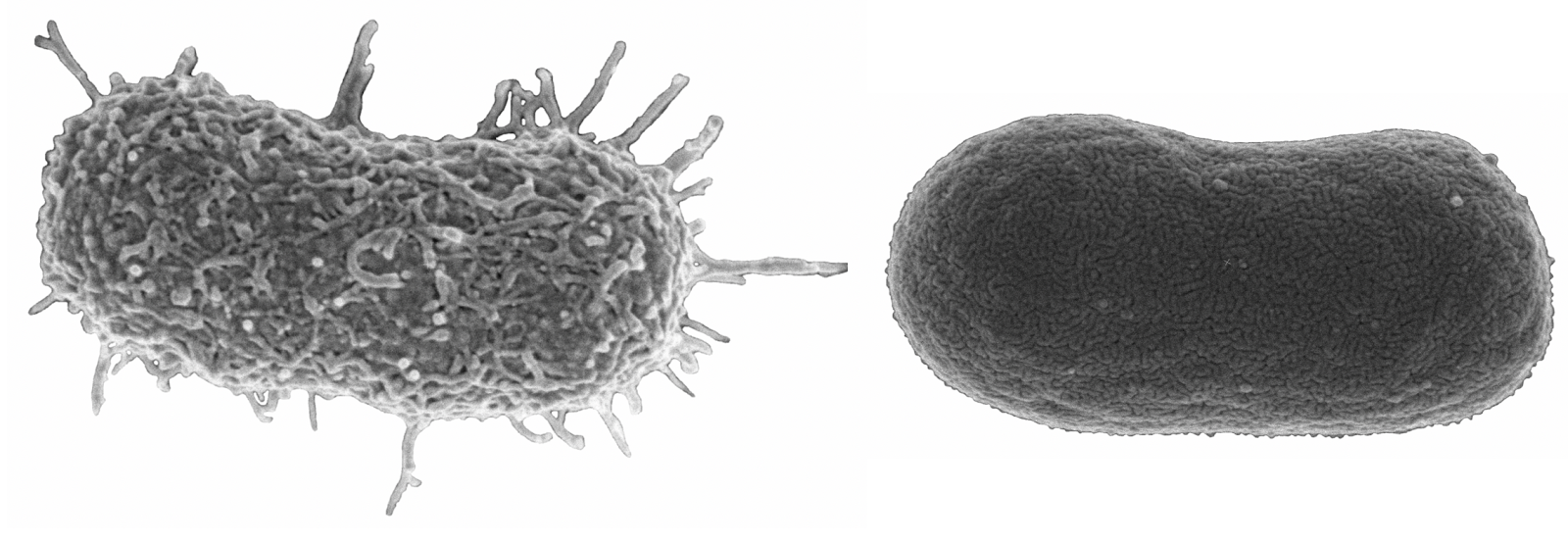
Теперь посмотрим на, можно сказать, типичных представителей семейства Acinetobacter spp. Необходимо отметить, что продемонстрированные ниже возбудители выделены из ран, полученных в результате ДТП в летнее время, причем у пациентов, которые длительное время не лечились антибиотиками, то есть оба зверя являются дикими.
На первом фото лечащему врачу повезло, так как ему достался возбудитель, чувствительный ко всему возможному арсеналу антибиотиков, которые в принципе могут повлиять на данный микроб.
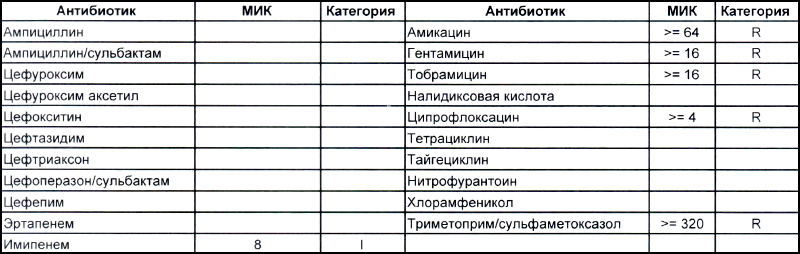
На второй антибиотикограмме возбудитель тоже получен из раны, ни разу не леченной антибиотиками, а также сам больной длительное время ничего антибактериального не употреблял. Данный случай очень хорошо демонстрирует то, что мы обсудили раньше, – только по антибиотикограмме в случае ацинеток трудно сказать, внутрибольничный возбудитель вызвал гнойно-воспалительный процесс или дикий уличный.
В научно-исследовательском институте, который может провести генетическое исследование возбудителя, смогут выяснить полностью, дикий это штамм или внутрибольничный, а мы, работающие на земле, скорее всего, не ответим на этот вопрос. Правда, у нас теперь СК все про всех знает, и автор уже давно ждет, когда очередного несчастного еще и в такого рода заражении обвинят.
Следует отметить, что обе эти картинки не отменяют факта наличия внутрибольничного заражения как первым штаммом (горшки с цветами помним?), так и вторым, в который под действием использующихся в больнице антибиотиков может выродиться первый. Ациентка, как и предыдущие обсуждаемые возбудители ВБИ, так же не имеет крылышек и ножек, ее точно так же переносят на руках и плохо обработанном медицинском оборудовании (эндоскопы, точнее, бронхоскопы, это просто бич крупных стационаров). Поэтому только внутриведомственный микробиологический надзор и работа над соблюдением санэпидрежима помогает удержать и эту зверюгу в хоть каких-то приемлемых рамках.
Клинические аспекты
Что способен вызвать ацинетобактер?
В общем, как вы можете видеть, ацинетка способна загубить на корню любой врачебный труд, так как инфекции, ей вызванные, имеют высокий процент летальности у пациентов, имеющих факторы риска развития подобной инфекции.
К факторам риска относятся:
Чем лечить?
Хороший вопрос. Точно такой же, как «чем лечить внутрибольничную клебсиеллу», которым мы задавались ранее.
Как вы могли убедиться, лечить ацинетку эмпирически (а это возможно только при тщательном внутрибольничном мониторинге), и даже с использованием диско-диффузионного метода, не очень-то и получится. Точнее, не получится совсем. Нужны аппаратные методы диагностики, чтобы точно знать, с чем вы имеете дело. И внутрибольничный мониторинг тоже крайне необходим, особенно если неферментеры сеются массово, чтобы знать — заполз ли возбудитель с улицы или уже свой зверинец развели. Во втором случае только мыть-мыть и еще раз мыть всю больницу полностью, а не только одно отделение, а также переходить на полностью одноразовые расходники, и к аппаратам ИВЛ тоже. Автор понимает, что при этих словах или в монитор захочется плюнуть, или помидором тухлым швырнуть, благо сезон пока не закончен.
Так как лечить?
В рамках клинических рекомендаций по той нозологии, которая у вашего пациента имеется, выложенных здесь, всегда только комиссионно, с привлечением клинических фармакологов и клинических микробиологов. И мойте руки после каждого подобного пациента очень тщательно — это ваша личная техника безопасности.
Выбор для Acinetobacter baumannii: умереть от бактериофага или от антибиотика
Acinetobacter baumannii — опасный противник. Известный своей устойчивостью к высыханию, истощению запаса питательных веществ и дезинфектантам, A. baumannii тяжело поддается уничтожению, когда бактерия приживается на медицинских объектах [1]. Способный избегать воздействия многих антибиотиков, A. baumannii представляет серьезную проблему для врачей и медперсонала, которые лечат зараженных пациентов и ухаживают за ними [2]. Всемирной организацией здравоохранения эта угроза признана, а A. baumannii получил статус важнейшего приоритета для исследований и разработки новых противомикробных препаратов [3]. В статье «Устойчивые к бактериофагам Acinetobacter baumannii получили повторную чувствительность к противомикробным препаратам» авторами продемонстрировано, что фаги могут дать второе дыхание для применения антибиотиков, которые уже есть в распоряжении врачей.
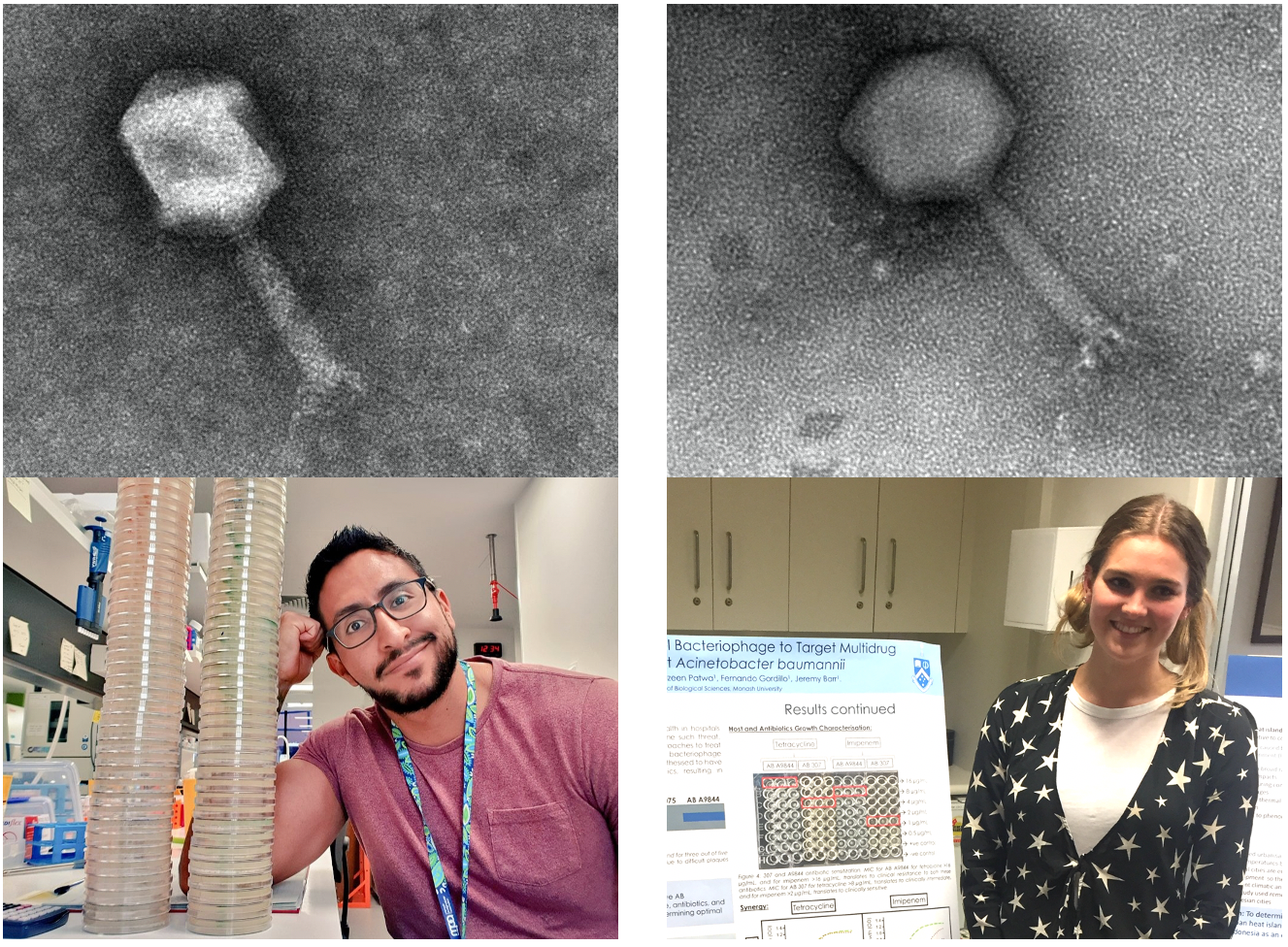
Идея, лежащая в основе этого проекта, возникла после того, как первый автор, Джереми Барр, ныне заведующий лабораторией в Школе биологических наук университета Монаша в Австралии, принял участие в первом клинически успешном применении фаговой терапии против системного A. baumannii, зарегистрированного в США [4, 5]. После последовательного приема смесей фагов командой ученых были осуществлены три, казалось бы, не связанных между собой наблюдения. Во-первых, изолят A. baumannii, полученный от пациента, приобрел устойчивость к смеси фагов. Во-вторых, он потерял устойчивость к антибиотику миноциклину. В-третьих, было выявлено, что бактерии потеряли полисахаридную капсулу. Могут ли быть связаны эти обнаруженные явления? И если да, то как? Это и стало отправной точкой в исследовании ученых.
Чтобы собрать вместе детали головоломки, ученые использовали два филогенетически отдаленных клинических штамма A. baumannii и два разных бактериофага, выделенных из неочищенных сточных вод. Как сказал один из авторов, Фернандо Гордиллио Альтамирано, эта работа является свидетельством того, как часто его любовь к микробиологии подвергалась проверке на прочность при работе с образцами неочищенных сточных вод (их помещали в инкубатор на ночь, добавляя в пробирки богатую питательными веществами среду). Фернандо Альтамирано приносит коллегам свои извинения за то, что запах смесей из сточных вод часто вынуждал их покидать лабораторию. Выделение фагов может оказаться сложной задачей, и, похоже, Фернандо Альтамирано положил начало тенденции в качестве награды в их исследовательской лаборатории давать фагам имена людей, которые их выделяют. В статье присутствуют изображения фагов øFG02 (Фернандо Альтамирано) и øCO01 (Коди Оливьера).
Исследователи обнаружили, что открытые ими фаги используют полисахаридные молекулы капсулы A. baumannii в качестве своего основного рецептора. Ученые пришли к такому выводу после наблюдения следующего:
То, что казалось простым процессом, на самом деле оказалось самым сложным шагом в исследовании. Ученые выявили, что с бактерией A. baumannii сложно проводить генетические манипуляции, а многочисленные попытки трансформации (естественной, химической и электропорацией) оказались безуспешными. Успешные же попытки экспериментов ученые связывают с фактором везения и настойчивостью соавторов Джона Форсайта и Рузин Патва.
Бактериальная капсула — основной фактор вирулентности A. baumannii, защищающий ее от иммунной системы, снижая проницаемость для антибиотиков [6]. Опираясь на фактические сведения, ученые полагают, что толстая капсула исследуемых штаммов дикого типа также играет роль в их очень низкой степени трансформации. В любом случае, исследователи были взволнованы, узнав, что капсуло-дефицитный, устойчивый к фагам A. baumannii стал повторно чувствительным к системе комплемента человека и пострадал от снижения до минимальных ингибирующих концентраций семи антибиотиков, в первую очередь β-лактамов, но также и миноциклина. Выделенные учеными фаги поставили A. baumannii перед дилеммой: умереть от фага или от антибиотика. Результаты исследования подчеркивают важность для терапии идентификации бактериальных рецепторов, которые используются любым фагами; они также вдохновили ученых на статью о перспективах, в которой они размышляют на эту тему [7].
Только в течение последнего десятилетия среди патогенных штаммов микробов, таких как Pseudomonas aeruginosa [8], Enterococcus faecalis [9], Staphylococcus aureus [10] и Klebsiella pneumoniae [11], было выявлено подобное взаимодействие между механизмами устойчивости к фагам и бактериальной адаптацией. Авторы данной работы добавляют в этот список бактерий A. baumannii, что еще раз подчеркивает многогранный потенциал фаговой терапии в борьбе с антибиотикорезистентностью.
Инфекции, вызываемые Acinetobacter
, MD, FACP, Charles E. Schmidt College of Medicine, Florida Atlantic University;
, MD, FACP, Wellington Regional Medical Center
Acinetobacter – грамотрицательные аэробные бациллы или коккобациллы, принадлежащие к семейству Moraxellaceae. Они встречаются повсеместно и могут выживать на сухих поверхностях в течение месяца, обычно обнаруживаются на коже медицинских работников, увеличивая вероятность колонизации пациентов и контаминации медицинского оборудования. Существует много видов Acinetobacter; все они могут вызвать заболевание человека, однако на долю Acinetobacter baumannii (АВ) приходится около 80% инфекций (1 Общие справочные материалы Вид Acinetobacter – это грамотрицательные организмы, которые могут вызывать гнойные инфекции в любой системе организма; эти бактерии часто являются оппортунистами у госпитализированных пациентов. Прочитайте дополнительные сведения ).
Общие справочные материалы
1. Wong D, Nielsen TB, Bonomo RA, et al: Clinical and pathophysiological overview of Acinetobacter infections: A century of challenges. Clin Microbiol Rev 30(1):409–447, 2017. doi: 10.1128/CMR.00058-16.
Болезни, вызываемые Acinetobacter (АВ)
Наиболее распространенными проявлениями заболеваний, вызванных Acinetobacter, являются:
Инфекции AB, как правило, выявляют у пациентов, госпитализированных в критическом состоянии. Внебольничные инфекции (преимущественно, пневмония) чаще возникают в тропическом климате. Уровень смертности, связанный с инфекцией AB, составляет 19–54%.
Acinetobacter часто колонизирует места трахеостомы и может вызывать внебольничный бронхиолит и трахеобронхит у здоровых детей и трахеобронхит у взрослых с ослабленным иммунитетом. Приобретенные в больнице пневмонии, вызванные Acinetobacter, часто многодолевые и осложненные. Характерны вторичная бактериемия и септический шок, что предопределяет неблагоприятный прогноз.
Вид Acinetobacter может также вызывать раневые инфекции и гнойные инфекции (например, абсцессы) в любой системе организма, включая легкие, мочевыводящие пути, кожу и мягкие ткани; возможна бактериемия.
В редких случаях эти микроорганизмы вызывают менингит (прежде всего после нейрохирургических процедур), флегмону или флебит у пациентов с постоянным венозным катетером, глазные инфекции, эндокардит нативного или искусственного клапана, остеомиелит, септический артрит или абсцессы поджелудочной железы и печени.
Значимость Acinetobacter изолятов из клинических образцов, таких как секрет из органов дыхания у интубированных пациентов или из открытых ран, определить трудно, потому что они часто представлены колониями.
Факторы риска
Резистентность к препарату
В последнее время появились штаммы АВ с множественной лекарственной устойчивостью (МЛУ), в частности, в отделениях интенсивной терапии у пациентов с иммуносупрессией, пациентов с серьезными первичными заболеваниями, а также пациентов, получавших лечение антибиотиками широкого спектра действия после инвазивных процедур. Распространение штаммов АВ в отделениях интенсивной терапии было связано с медицинским персоналом, у которых выявлена высокая колонизация данного микроорганизма, а также с зараженным оборудованием общего использования и зараженными растворами для парентерального питания. Кроме того, возросло число случаев мультирезистентности, вызванной АБ, среди военнослужащих, которые были ранены и проходили лечение в Ираке, Кувейте и Афганистане.
Лечение ассоциированных инфекций
Обычно, эмпирическая комбинированная лекарственная терапия при тяжелых инфекциях
Для пациентов с установленным инородным телом (например, катетер, шов), удаление инородного тела плюс местная обработка обычно существенны. Трахеобронхит после эндотрахеальной интубации может разрешится с помощью одной гигиены легких Пациенты с осложненным течением заболевания должны лечиться антибиотиками с последующей санацией.
У AB давно регистрируется множественная резистентность к антибактериальным препаратам. Инфекция AB с множественной лекарственной устойчивостью определяется как штаммы, которые устойчивы к ≥ 3 классам антибактериальных препаратов; некоторые изоляты являются стойкими ко всем антибиотикам. До получения результатов чувствительности к антибиотикам в качестве стартовой терапии можно использовать карбапенемы (например, меропенем, имипенем, дорипенем), колистин или фторхинолоны вместе с аминогликозидами, рифампицином, или с обеими. У сульбактама (ингибитора бета-лактамазы) имеется свойственная ему бактерицидная активность против многих штаммов инфекции АБ данного типа. Тигециклин, антибиотик класса глицилциклинов также эффективен; однако отмечено ограничение его активности и появлении резистентности во время терапии. Миноциклин, как и новый сидериофор-цефалоспориновый антибиотик, цефидерокол обладает активностью in vitro (1 Справочные материалы по лечению Вид Acinetobacter – это грамотрицательные организмы, которые могут вызывать гнойные инфекции в любой системе организма; эти бактерии часто являются оппортунистами у госпитализированных пациентов. Прочитайте дополнительные сведения ).
Инфекции легких (при среднетяжелых формах) могут реагировать на монотерапию. Раневые инфекции также можно лечить одним препаратом, например миноциклиномом.
Тяжелые формы АБ инфекций лечат, используя комбинированную терапию – как правило, карбапенемы (имипенем или меропенем) или препарат ампициллин/сульбактам в комплексе с аминогликозидом; при условии устойчивости к лекарственным препаратам, единственными доступными вариантами могут быть тигециклин или комбинация колистина и миноциклина.
Чтобы предотвратить распространение возбудителя, необходимо применять меры по предотвращению контакта (ручная стирка, барьер) и соответствующие меры по проветриванию и гигиене, связанной с пациентами, колонизированными или зараженными инфекцией такого рода.
Справочные материалы по лечению
1. Munier AL, Biard L, Rousseau C, et al: Incidence, risk factors, and outcome of multidrug-resistant Acinetobacter baumannii acquisition during an outbreak in a burns unit. J Hosp Infect 97(3):226–233, 2017. doi: 10.1016/j.jhin.2017.07.020.
Ключевые моменты ацинетобактериальных инфекций
A. baumannii (АВ) является причиной около 80% инфекций, вызванных Acinetobacter, часто встречается у больных в критическом состоянии, находящихся в стационаре.
Наиболее распространенным местом локализации инфекции является дыхательная система, однако некоторые виды Acinetobacter также могут вызвать гнойную инфекцию в любой другой органной системе.
Мультирезистентные штаммы АВ стали проблемой; проводить множественную лекарственную терапию следует после проведения исследований на чувствительность.