Атеросклероз печени что такое
Что такое атеросклероз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Зафираки Виталия Константиновича, кардиолога со стажем в 20 лет.
Определение болезни. Причины заболевания
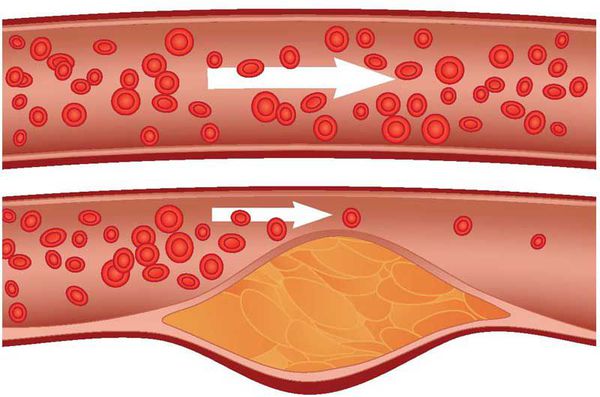
Атеросклероз — системное заболевание, первоначально поражающее сосуды, но не все, а только артерии, в стенках которых накапливается холестерин и его эфиры, образующие характерные для этого заболевания бляшки. [1]
Чем опасен атеросклероз
В дальнейшем, по мере того, как снижается способность пораженных атеросклерозом кровеносных сосудов доставлять необходимое для работы внутренних органов количество крови, поражаются и сами эти органы. Это происходит либо медленно и постепенно — в силу роста атеросклеротических бляшек, либо остро — при развитии тромбоза сосуда. Тромбоз сосудов может приводить к инфаркту миокарда, инсульту, гангрене нижней конечности.
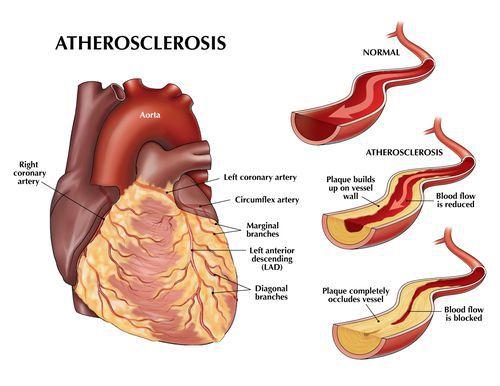
В медицине сложилась странная ситуация, когда для поражения атеросклерозом ряда органов имеются названия соответствующих «болезней», хотя фактически болезнь одна и та же: атеросклероз, и только преимущественная локализация процесса может быть разной. В частности, при наличии симптомов поражения артерий сердца (коронарных) говорят об ишемической болезни сердца (ИБС), при симптомном поражении артерий, кровоснабжающих нижние конечности — об атеросклерозе артерий нижних конечностей («перемежающаяся хромота»), а, например, при разрыве атеросклеротической бляшки и тромбозе одного из сосудов, кровоснабжающих головной мозг — об ишемическом атеротромботическом инсульте.
Факторы риска атеросклероза
Возникновение и развитие атеросклероза нельзя свести к какому-то одному причинному фактору — обычно это переплетение причин. Однако среди всех причин можно выделить те, которые связаны с генетическими особенностями человека, [2] и те, которые обусловлены образом жизни. [3]
В случаях, связанных с «генетическими поломками», никаких других причин для развития атеросклероза может и не потребоваться, а болезнь может иметь весьма злокачественный характер, когда, к примеру, инфаркт миокарда или инсульт случаются на третьем-четвертом десятилетии жизни, а сама жизнь значительно укорачивается. [2]
Холестерин и атеросклероз
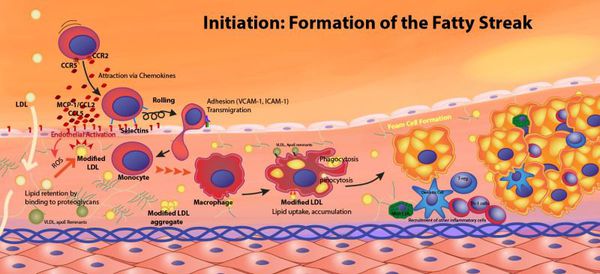
«Генетическими поломками» вызвана так называемая семейная гиперхолестеринемия, при которой перемещающиеся в крови комплексы липидов, содержащие холестерин, плохо захватываются тканями (прежде всего, печенью). В результате концентрация в крови этих частиц и, соответственно, холестерина, возрастает, и избыточный холестерин, а также его эфиры оказываются в конечном счете в стенке артерий. Конечно, процесс этот гораздо сложнее и в действительности является многоэтапным, но конечный результат его — образование атеросклеротических бляшек в стенках сосудов.
Повышение концентрации содержащих холестерин частиц в крови может гораздо чаще происходит не в силу генетических поломок, а вследствие нездорового образа жизни.
Сам по себе холестерин — жизненно необходимое вещество, и каждая наша клетка способна его синтезировать по мере надобности. А вот когда способности организма использовать и утилизировать свой холестерин снижаются, вот тогда его концентрация в крови возрастает, со всеми дальнейшими последствиями. Снижают способность утилизировать свой собственный холестерин такие факторы, которые изменяют химический состав липидных частиц, в состав которых входит и холестерин. Это, например, курение, сахарный диабет, хроническое воспаление. Эти же факторы повреждают стенки сосудов, облегчая тем самым проникновение в них содержащих холестерин липидных частиц крови.
Симптомы атеросклероза
Атеросклероз долгое время (годы и десятилетия) протекает без симптомов. Причем исподволь поражаются обычно многие сосуды, поскольку атеросклероз — системное заболевание. Если в каком-то участке сосудистого русла обнаружена атеросклеротическая бляшка — скорее всего, бляшки имеются и в других сосудистых бассейнах. Появление симптомов связано прежде всего с проявлениями снижения кровотока в пораженном сосуде. Если такое поражение связано с хроническим ограничением кровотока, возникают симптомы хронической ишемии (последствий снижения кровотока) соответствующего органа.
Атеросклероз коронарных артерий
Если атеросклеротические бляшки значительного размера ограничивают кровоток в сосудах сердца, развивается так называемая «стенокардия напряжения» — боль в грудной клетке или дискомфорт (тяжесть, жжение, сдавливание в груди) при физической нагрузке — ходьбе, беге, подъеме тяжестей.
Атеросклероз артерий нижних конечностей
Если то же самое происходит в артериях нижних конечностей, развивается симптоматика, которая получила название «перемежающаяся хромота», при которой во время ходьбы появляется боль, жжение или резкая усталость в мышцах ног. Эти симптомы довольно быстро проходят, если остановиться, но возникают через некоторое время опять при продолжении ходьбы.
Атеросклероз сосудов головного мозга
Наиболее серьёзными проявлениями атеросклероза сосудов головного мозга является ишемический инсульт и транзиторная ишемическая атака.
Симптомы инсульта и транзиторной ишемической атаки могут быть сходными, но при транзиторной ишемической атаке они проходят в течение 24 часов, а при инсульте — более стойкие. Симптомы в основном проявляются нарушениями со стороны двигательной и/или чувствительной сферы:
Атеросклероз почечной артерии
Атеросклероз почечных артерий может приводить к артериальной гипертензии, в том числе устойчивой к лечению.
Патогенез атеросклероза
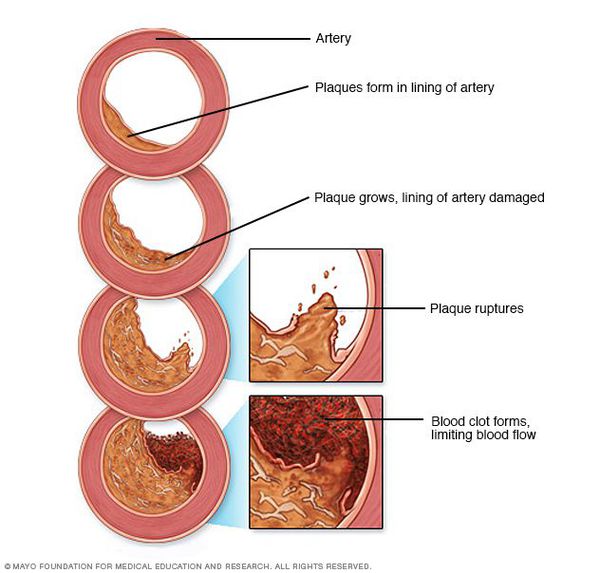
Рост атеросклеротических бляшек — процесс, растянутый на долгие годы и десятилетия. Если бляшка в стенке сосуда достигает значительных размеров (около 70% просвета сосуда или более того), она может создавать существенные препятствия для кровотока и для кровоснабжения соответствующего органа — например, сердца или мозга. Бляшки, небольшие по размерам, тоже небезопасны — при разрыве таких бляшек (это возможно в случаях, когда истончается по разным причинам их «покрышка») в месте разрыва возникает образование тромба, который может полностью перекрыть просвет сосуда. [5] В этом случае из-за резкого ограничения кровотока возникает гибель значительного количества клеток органа, кровоснабжаемого данным сосудом — инфаркт (например, инфаркт миокарда или инфаркт мозга — инсульт, возникающий при атеросклерозе сосудов головного мозга).
Классификация и стадии развития атеросклероза
Выделяют две стадии развития атеросклероза: субклиническую и симптомную.
Длительное время атеросклероз протекает бессимптомно, эта стадия называется «субклиническим атеросклерозом». На этом этапе с помощью инструментальных методов диагностики можно обнаружить атеросклеротические бляшки, часто в той или иной степени суживающие просвет сосуда.
Появление симптомов (например, стенокардия напряжения, перемежающаяся хромота, ишемический инсульт и др.) соответствует понятию «симптомный атеросклероз» или «атеросклеротическое сердечно-сосудистое заболевание» и симптомной стадии атеросклероза.
Осложнения атеросклероза
В тех случаях, когда объем кровотока по пораженной артерии снижается быстро — а это происходит в случае разрыва атеросклеротической бляшки и формирования в этом участке тромба — столь же быстро развиваются симптомы, связанные с поражением соответствующего органа: инфаркт миокарда, инсульт, гангрена нижней конечности и др.
Диагностика атеросклероза
В той или иной степени атеросклеротические бляшки в стенках артерий имеются у большинства взрослых людей, ведущих современный «западный» образ жизни, однако далеко не у всех этот процесс достигает того этапа, когда появляются клинические симптомы. [6] Если клинических симптомов, которые можно связать со снижением кровотока по тем или иным артериям, нет, врач тем не менее оценивает риск атеросклероза и смерти от заболеваний, связанных с ним, с помощью выявления так называемых факторов риска атеросклероза. [3] К наиболее важным из них относятся мужской пол, возраст (с каждым прожитым десятилетием риск заболеваний, связанных с атеросклерозом, увеличивается), повышенное артериальное давление, повышенный уровень холестерина (особенно холестерина липопротеинов низкой плотности), курение, сахарный диабет, ожирение, ряд генетических поломок и др. Риск смерти от заболеваний, связанных с атеросклерозом, на ближайшие 10 лет можно индивидуально для себя рассчитать с помощью электронного калькулятора. [3] Высоким риск считается, если он превышает 5%. 5% — вроде бы немного. Однако надо учитывать, что это риск именно смерти. Риск нефатальных заболеваний, грозящих развиться в течение этого срока, в 3-5 раз выше. Причем фактический риск обычно выше расчетного, поскольку калькулятор учитывает всего лишь 5 основных факторов риска, а их гораздо больше. Например, наличие сахарного диабета увеличивает расчетный риск у мужчин в 3 раза, а у женщин — в 5 раз!
Поскольку важнейшим фактором риска атеросклероза любой локализации является повышенный уровень холестерина в крови (особенно холестерина липопротеинов низкой плотности), обычно выполняют исследование крови, называемое «липидограмма» (входит в понятие «биохимический анализ крови»). Это подразумевает не только измерение концентрации общего холестерина, но и его распределение по двум (а теперь доступно и по трем) фракциям липопротеинов: холестерин липопротеинов низкой плотности и холестерин липопротеинов высокой плотности. Кроме того, липидограмма подразумевает измерение концентрации триглицеридов (жиров) в крови. В результате точнее можно оценить риск заболеваний, связанных с атеросклерозом, и наметить мишени для лечебных воздействий. Нарушения, выявленные в липидограмме, не являются сами по себе синонимом заболевания «атеросклероз», но увеличивают риск этого заболевания тем в большей степени, чем тяжелее выявленные биохимические нарушения.
Сами атеросклеротические поражения артерий для своего выявления требуют проведения различных инструментальных исследований в зависимости от того, атеросклероз какой локализации предполагает врач. Наиболее доступная локализация для выявления атеросклероза — сонные артерии. Для этого выполняют их ультразвуковое исследование (триплексное сканирование брахиоцефальных артерий). Это исследование позволяет оценить состояние сосудистой стенки, экстраполируя эти данные более или менее успешно на всё артериальное сосудистое русло. Подразумевается, что если атеросклеротические бляшки есть в сонных артериях, с высокой вероятностью они имеются и в других сосудах, поэтому такому пациенту скорее всего потребуется медикаментозное снижение уровня холестерина и воздействие на другие факторы риска атеросклероза (например, артериальное давление, масса тела, курение). [7]
Довольно просто оценить наличие атеросклеротических бляшек и в сосудах ног. Это делается с помощью того же ультразвукового метода. Бляшки, находящиеся в сосудах сердца, увидеть сложнее. Однако для принятия решения о лечении имеют значение только те бляшки в коронарных сосудах, которые значительно перекрывают кровоток, вызывая симптомы — в случае хронического поражения этих сосудов речь идет о «стенокардии напряжения», которую выявляют путем анализа имеющихся клинических проявлений (в типичном случае это боль или дискомфорт в грудной клетке, возникающие при ходьбе, беге или поднятии тяжести и проходящие за несколько минут в покое) и выполнением исследования с физической нагрузкой в ходе которого регистрируют электрокардиограмму, эхокардиограмму или сцинтиграфическое изображение сердца с целью выявить объективные признаки ишемии, т. е. временного несоответствия между доставкой крови к миокарду и потребностей в ней при нагрузке. В случаях, когда врач решает, что имеются показания для проведения операции на сосудах сердца, выполняют коронароангиографию — рентгенологическое исследование сосудов сердца с введением контрастного вещества, в ходе чего можно непосредственно увидеть просвет сосудов сердца и имеющиеся в этих сосудах сужения, с целью наметить план операции и выбрать ее вариант. [8]
Лечение атеросклероза
Следует отделять, с одной стороны, те мероприятия, которые направлены на профилактику атеросклероза и затормаживание темпов его развития/прогрессирования, и, с другой стороны — мероприятия по лечению заболеваний, в основе которых лежит атеросклеротическое поражение артерий.
Какой врач лечит атеросклероз сосудов
В зависимости от того, со стороны какого органа имеются симптомы, следует обратиться:
Обратим ли атеросклероз сосудов
В наши дни пока еще нет возможности исправить те «поломки» на уровне генов, благодаря которым у некоторых людей ускоряется развитие атеросклероза. Поэтому с целью остановить или затормозить его развитие лечебные и профилактические воздействия при атеросклерозе направлены в основном на то, чтобы снизить негативное воздействие факторов риска атеросклероза, в том числе — добиться снижения уровня холестерина в крови, и прежде всего, того самого «плохого» холестерина липопротеинов низкой плотности. [4] Снижение уровня холестерина в крови и, самое главное, поддержание его на оптимальном уровне в течение многих лет способно остановить прогрессирование атеросклероза и даже отчасти обратить его вспять. [9] Эти мероприятия проводятся как в рамках оздоровления образа жизни, так и в виде медикаментозного лечения. Впрочем, большинство людей обычно не готово к серьезным изменениям в своем образе жизни и больше уповают на какие-то внешние воздействия, которые над ними могли бы произвести врачи, либо на мероприятия в рамках самолечения. На этот счет существует огромное количество заблуждений и мифов, неэффективных якобы «лечебных» мер, препаратов и биодобавок.
Медикаментозное лечение атеросклероза
Из числа лекарственных препаратов с доказанной эффективностью, способных затормозить развитие и прогрессирование атеросклероза, а также в определенной мере вызвать обратное его развитие, наибольшую доказательную базу имеют статины [4] (аторвастатин, розувастатин, питавастатин, симвастатин). Статины не только снижают уровень общего холестерина и холестерина, содержащегося в липопротеинах низкой плотности, но и, благодаря этому, при длительном применении статины способны остановить или замедлить рост атеросклеротических бляшек, снизить риск инфаркта миокарда и инсульта, а также увеличить продолжительность жизни при заболеваниях, связанных с атеросклерозом. Для того, чтобы рассчитывать на такие эффекты, статины надо принимать в течение ряда лет и в правильных дозах, которые были установлены в тех клинических исследованиях, которые обнаружили положительные эффекты статинов.
Существуют и другие лекарственные препараты, которые улучшают биохимические показатели крови, отражающие липидный профиль, и благодаря этому снижают риск заболеваний и осложнений, связанных с атеросклерозом. Помимо статинов, это эзетимиб (эзетрол), препятствующий всасыванию пищевого холестерина в кишечнике, а также недавно появившиеся кумабы — антитела к обнаруженному в 2003 году ферменту, сокращенно называемому PCSK9 (эволокумаб и алирокумаб зарегистрированы в России). Упрощая, можно сказать, что этот фермент — PCSK9 — регулирует скорость поглощения холестерина, содержащегося в крови, клетками печени. [10] Правда, кумабы в настоящее время весьма дороги, но это единственный их недостаток. Существуют и другие группы лекарств, способные влиять на липидный профиль в сторону его улучшения, но их значение существенно меньше.
Оперативное лечение. Как подготовиться к операции
Главное перед операцией — это по возможности достигнуть компенсации тех серьёзных хронических заболеваний, которые имеются (сахарный диабет, хроническая обструктивная болезнь лёгких, хроническая сердечная недостаточность и др.). Это задача лечащего врача. Хотя в неотложных ситуациях операция проводится в срочном порядке по жизненным показаниям. За несколько дней до плановой операции лечащим врачом могут быть отменены некоторые лекарства, снижающие свёртываемость крови.
Диета
В основном, рекомендуется свести к минимуму продукты, которые содержат в больших количествах насыщенные жиры и трансжиры. Опознавательным признаком этих жиров является твёрдая консистенция при комнатной температуре.
Народные методы лечения атеросклероза
Ни красное вино, ни свиное сало, ни настойка чеснока, ни лазерное облучение крови, ни мониторная очистка кишечника, равно как и огромное количество других «лечебных» мер, не способны лечить атеросклеротическое поражение сосудов.
Прогноз. Профилактика
Для лечения и профилактики атеросклероза имеет значение воздействие на все основные причинные факторы (факторы риска) его развития:
В тех случаях, когда развитие атеросклероза достигает того этапа, при котором появляются клинические симптомы того или иного заболевания, связанного с атеросклерозом, начинают лечить само это заболевание, или точнее будет сказать, атеросклеротическое поражение того или иного органа: сердца, мозга, почек, нижних конечностей. Причем нередко это лечение может быть хирургическим. [11] Обычно такое лечение состоит в хирургических воздействиях, локально восстанавливающих проходимость пораженных атеросклерозом артерий. Например, при поражении сосудов сердца это может быть малотравматичная операция по установке в месте сужения специального внутрисосудистого каркаса — стента, которая проводится через прокол в сосуде, а может быть и «большая» операция коронарного шунтирования со вскрытием грудной клетки и наложением путей обходного кровотока в сердце — шунтов. При этом атеросклероз как системное заболевание остается, и хирургическое лечение никоим образом не отменяет необходимость лечить его — прежде всего, корректируя факторы риска, среди которых крайне важным является нарушенное соотношение фракций липопротеинов, содержащих холестерин.
Сосудистые заболевания печени
» data-image-caption=»» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Сосудистые-заболевания-печени.jpeg?fit=825%2C550&ssl=1″ />
Заболевания сосудов печени — относительно редкие болезни, при них может нарушаться кровоток в печени, что приводит к ряду серьезных осложнений. В этой статье рассматриваются основные вопросы, связанные с патогенезом, клинической картиной и лечением.
Обструкция печеночной артерии
Определение
Это осложнение множества различных патологических состояний, приводящих к частичному или полному нарушению кровотока по этому сосуду.
Эпидемиология
Обструкция печеночной артерии встречается относительно редко и точных эпидемиологических данных по этому поводу нет. Тромбоз печеночной артерии, приводящий к обструкции, может быть осложнением (примерно 2% трансплантатов печени).
Патогенез
Обструкция печеночной артерии может быть вызвана атеросклерозом, тромбозом, эмболией, инфильтрацией печени или травмой. Это происходит в ходе истинной полицитемии, узелкового артериита, эндокардита и, как упоминалось выше, у небольшого процента пациентов после трансплантации печени.
Непроходимость может возникнуть в результате:
Клиническая картина
У многих пациентов обструкция печеночной артерии протекает бессимптомно и выявляется только при вскрытии. Из-за двойной васкуляризации печени, окклюзия просвета печеночной артерии, не является синонимом инфаркта печени (эмболизация печеночной вены, является, признанным методом лечения рака печени).
Тем не менее, одновременная и полная непроходимость печеночной артерии и воротной вен, почти всегда заканчивается летальным исходом. Клинически инфаркт печени проявляется болью в правой верхней части живота, тахикардией и падением артериального давления. В редких случаях может развиться острая печеночная недостаточность.
Диагностика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%94%D0%B8%D0%B0%D0%B3%D0%BD%D0%BE%D1%81%D1%82%D0%B8%D0%BA%D0%B0-1.jpg?resize=450%2C300&ssl=1″ alt=»Диагностика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Диагностика-1.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Диагностика
Лабораторные исследования показывают повышение активности трансаминаз и увеличение протромбинового времени. Визуализирующие тесты играют важную роль в диагностике:
Допплерография
В случае тромбоза печеночной артерии, после трансплантации печени, клинические симптомы обычно появляются в течение нескольких дней после сеанса, а тесты показывают быстрое повышение активности трансаминаз и усиление холестаза. Это связано с быстро прогрессирующей ишемией желчевыводящих путей.
Пациентам с трансплантацией печени проводится тромбэктомия или повторная трансплантация. При окклюзиях другой этиологии может применяться тромболитическая терапия (стрептокиназа или рекомбинантный активатор плазминогена), или антикоагулянтная терапия (гепарин).
Тромбоз воротной вены
Кровоток в воротной вене может быть нарушен в результате тромбоза или инфильтрации опухоли. Клинически тромбоз воротной вены подразделяется: на острый и хронический. Этиология обоих состояний схожа, хроническая форма,- это чаще все продолжение острой формы. Однако методы лечения у них разные.
Факторы риска
Факторы риска тромбоза воротной вены обычно подразделяются на местные и общие. Наиболее частые местными факторы риска: рак брюшной полости и цирроз печени.
Тогда как наиболее распространенные общие факторы риска — это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции. Следует помнить, что диагностика местной причины тромбоза воротной вены не исключает одновременного наличия одной или нескольких общих причин.
Тромбоз воротной вены при миелопролиферативном синдроме
Тромбоз воротной вены — это клинический симптом миелопролиферативного заболевания. Поскольку портальная гипертензия приводит к отклонениям в анализе крови, (таким как анемия и тромбоцитопения), у большинства пациентов нет изменений в периферической крови, характерных для миелопроферативного синдрома, поэтому, диагноз расширяется до определения мутации гена JAK2 (киназа Януса 2 типа) и в таких ситуациях биопсия костного мозга находит полное оправдание.
Дифференциация
В соответствии с рекомендациями Американской ассоциации по изучению заболеваний печени, при диагностике тромбоза воротной вены на основании визуализационных исследований (УЗИ, КТ, в первую очередь следует исключить следующее:
Клинические формы
Острый тромбоз воротной вены — это внезапное образование сгустка частично или полностью закупоривающего воротную вену.
Клиническая картина
Выраженность клинических симптомов зависит от степени окклюзии воротной вены. Острый тромбоз проявляется:
Диагностика
Лабораторные тесты
Лабораторные исследования показывают увеличение показателей острой фазы. Чаще всего сохраняется функция печени, что объясняется компенсаторным кровотоком из печеночной артерии и коллатеральным кровообращением по мелким венозным сосудам в воротах печени. Однако, у некоторых пациентов наблюдается умеренное повышение уровня трансаминаз.
Визуальные исследования
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%92%D0%B8%D0%B7%D1%83%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5-%D0%B8%D1%81%D1%81%D0%BB%D0%B5%D0%B4%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F.jpg?resize=450%2C300&ssl=1″ alt=»Визуальные исследования» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Визуальные-исследования.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Визуальные исследования
Визуальная диагностика имеет решающее значение для постановки диагноза:
Фармакотерапия
Антикоагулянтное лечение. Методом выбора является быстрое введение низкомолекулярного гепарина, предотвращающего инфаркт кишечника и значительно улучшает прогноз. Терапия пероральными антикоагулянтами (варфарин или не так часто, применяемый аценокумарол) возможна, если клиническое состояние пациента стабильно и хирургическое вмешательство не планируется.
Консервативное лечение дает шанс полной реканализации сосуда примерно у 40% пациентов. Оно должно длиться не менее 3 месяцев, хотя следует отметить, что полное восстановление тромбоза наблюдалось даже после 6 месяцев терапии. В случаях тромбофилии, для которой не существует радикальной терапии, антикоагулянтное лечение, скорее всего, следует использовать до конца жизни.
Антимикробное лечение. При появлении признаков инфекции требуется антибактериальная терапия.
Инвазивное лечение. Инвазивные процедуры, такие как: тромболизис стрептокиназой или тканевым активатором плазминогена, вводимыми непосредственно в воротную вену или в верхнюю брыжеечную артерию, не показывают более высокой эффективности, чем антикоагулянты, и имеют гораздо более высокий риск серьезных осложнений.
Конечно, в случае инфаркта кишечника, методом выбора будет хирургическая резекция некротических фрагментов кишечника. Это лечение можно сочетать с удалением сгустка из просвета сосуда.
Хронический тромбоз воротной вены
Это клиническое состояние, при нем в результате тромбоза воротной вены развивается коллатеральное кровообращение, соединяющее вены до и после сгустка, образуя сеть сосудов, известную как кавернозная трансформация.
Клиническая картина
Чаще всего хронический тромбо, диагностируется при поиске причины симптомов портальной гипертензии, проявляющейся кровотечением из варикозно расширенных вен пищевода или увеличением селезенки. Пациенты с хроническим тромбозом воротной вены переносят кровотечение из варикозно расширенных вен пищевода лучше, чем пациенты с циррозом, что в основном связано с хорошо сохраненной функцией печени.
Иногда сеть сосудов кавернозной трансформации может сужать желчные протоки, что приводит к портальной билиопатии, приводящей к симптомам холестаза и холангита. Иногда трудно отличимым от первичного склерозирующего холангита.
Физикальное обследование показывает характерное расширение поверхностных сосудов брюшной полости. Минимальная энцефалопатия наблюдается примерно у половины пациентов с хроническим тромбозом, что, однако, может ухудшить точность или способность управлять автомобилем.
Диагностика
Биохимия печени обычно в норме. Визуализирующие исследования, такие как УЗИ, КТ или МРТ, показывающие многочисленные коллатеральные сосуды в области воротной вены и невидимый (неконтрастный) фрагмент воротной вены, играют решающую роль в диагностике, (как при остром тромбозе). Иногда при допплеровском исследовании коллатеральные сосуды имитируют воротную вену, увеличение поджелудочной железы или опухоль желчевыводящих путей.
Нет хорошо задокументированных исследований эффективности бета-адреноблокаторов для первичной профилактики или бандажирования, при вторичной профилактике кровотечения из варикозно расширенных вен пищевода у пациентов с тромбозом воротной вены.
Аналогичная проблема существует при лечении этих пациентов антикоагулянтами. Кажется логичным, сначала лечить варикозное расширение вен пищевода с помощью бандажа пациентам, у которых был эпизод кровотечения, а затем начать антикоагулянтную терапию. Имеются сообщения о том, что хроническая антикоагулянтная терапия снижает риск рецидива тромбоза, без увеличения риска кровотечения из варикозного расширения вен. Пациентам с развивающимся симптомом портальной билиопатии, осложненной холангитом, оправдан эндоскопический стеноз.
Прогноз
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?fit=480%2C320&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D0%B3%D0%BD%D0%BE%D0%B7.jpg?resize=450%2C300&ssl=1″ alt=»Прогноз» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Прогноз.jpg?w=480&ssl=1 480w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Прогноз
Типичные осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии — это редкая причиной смерти у пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Тромбоз воротной вены у пациентов с циррозом печени
Тромбоз воротной вены у пациентов с циррозом печени коррелирует со степенью декомпенсации органа.Тромбоз может развиться у 1/4 пациентов, требующих трансплантации печени. Рак печени может быть причиной тромбоза у пациентов с циррозом.
Клиническая картина
Наиболее частые клинические симптомы тромбоза:
В этой группе чаще выявляются мутации фактора V Лейдена, гена протромбина или метилентетрагидрофолатредуктазы (MTHFR), чем у пациентов с циррозом печени без тромбоза.
К сожалению, никаких рекомендаций по лечению антикоагулянтами у этих пациентов не разработано. Рекомендуется принимать индивидуальные решения. Однако, у подавляющего большинства пациентов, ожидающих трансплантации печени, после начала антикоагулянтной терапии воротная вена восстанавливается.
Тромбоз воротной вены после трансплантации печени
Это осложнение может возникнуть у 2-3% пациентов и часто связано с разницей в диаметре воротной вены донора и реципиента, а также со спленэктомией, выполняемой во время операции по трансплантации.
Синдром обструкции синуса печени
Определение
Это процесс, нарушающий кровообращение в печени в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи печени. У некоторых пациентов в этот процесс также вовлекаются центральные вены.
Эпидемиология
В развитых странах синдром синусоидальной обструкции (SOS), ранее называвшийся (VOD) веноокклюзионная болезнь, является наиболее частым осложнением абляции костного мозга, при его подготовке к трансплантации, (в этом контексте, следует использовать термин — трансплантация гемопоэтических стволовых клеток). Острая обструкция синуса печени — это третья по значимости причина смерти пациентов, перенесших трансплантацию костного мозга.
Другие причины SOS включают:
Клиническая картина
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9A%D0%BB%D0%B8%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F-%D0%BA%D0%B0%D1%80%D1%82%D0%B8%D0%BD%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Клиническая картина» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Клиническая-картина.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Клиническая картина
Клинические симптомы могут имитировать синдром Бадда-Киари и включают наиболее распространенные:
Выделяют три степени тяжести симптомов: легкую, среднюю и тяжелую.
Если заболевание стало результатом применения циклофосфамида, первые признаки появляются через 10-20 дней после начала лечения. При других схемах миелоабляции симптомы могут развиться позже. На практике синдром обструкции синусовых сосудов печени диагностируется у пациентов:
Диагностика
Балтиморские критерии
Балтиморские критерии полезны при постановке диагноза. Синдром обструкции печеночного синуса подтверждается при соблюдении следующих условий:
Дифференциация
Дифференциальный диагноз должен включать:
Дополнительные исследования
В сомнительных случаях диагноз подтверждается если:
При допплеровском исследовании печеночных сосудов можно наблюдать изменение направления кровотока в воротной вене.
Профилактика
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%9F%D1%80%D0%BE%D1%84%D0%B8%D0%BB%D0%B0%D0%BA%D1%82%D0%B8%D0%BA%D0%B0.jpg?resize=450%2C300&ssl=1″ alt=»Профилактика» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Профилактика.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Профилактика
Для профилактики закупорки сосудов синуса печени используются менее агрессивные, чем стандартные схемы миелоаблативной терапии, с применением флударабина, более низкие дозы бусульфана или дозы облучения.
Наибольший риск закупорки сосудов синуса печени связан с назначением циклофосфамида и облучением в дозе> 12 гр. Смертность у пациентов с синдромом обструкции синуса печени, получавших такое лечение может составлять 15-20%.
Кроме того, в профилактике используются:
Руководящие принципы Американской ассоциации по изучению заболеваний печени (AASLD) не рекомендуют какие-либо из этих методов лечения, поскольку рандомизированные испытания не подтвердили их эффективность. Антикоагулянтная терапия, также может привести к опасным для жизни кровотечениям.
Симптоматическое лечение перегрузки жидкостью включает:
Из-за отсутствия достаточных данных не рекомендуется использовать дефибротид, тканевый активатор плазминогена или TIPS (трансъюгулярный внутрипеченочный портосистемный шунт).
Трансплантация печени может быть терапевтическим вариантом у пациентов с незлокачественными заболеваниями, например, аутоиммунными заболеваниями.
Прогноз
Плохой прогноз определяется:
Тромбоз печеночной вены (синдром Бадда-Киари)
Тромбоз печеночной вены (синдром Бадда-Киари)
» data-medium-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A2%D1%80%D0%BE%D0%BC%D0%B1%D0%BE%D0%B7-%D0%BF%D0%B5%D1%87%D0%B5%D0%BD%D0%BE%D1%87%D0%BD%D0%BE%D0%B9-%D0%B2%D0%B5%D0%BD%D1%8B-%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC-%D0%91%D0%B0%D0%B4%D0%B4%D0%B0-%D0%9A%D0%B8%D0%B0%D1%80%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Тромбоз печеночной вены (синдром Бадда-Киари)» width=»450″ height=»300″ srcset=»https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=450%2C300&ssl=1 450w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=825%2C550&ssl=1 825w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?resize=768%2C512&ssl=1 768w, https://i2.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Тромбоз-печеночной-вены-синдром-Бадда-Киари.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Тромбоз печеночной вены (синдром Бадда-Киари)
Определение
Нарушение кровотока, возникающее на любой стадии оттока крови из печени, от мелких печеночных вен, до места соединения главной вены с правым предсердием.
Разделение
Синдром Бадда-Киари делится на:
Причины
Клинически заболевание может иметь вид:
Существуют значительные расхождения между клинической картиной и длительностью тромбоза. Например, у пациентов с симптомами острого тромбоза очень часто встречаются признаки длительного заболевания, такие, как выраженный фиброз и цирроз.
Общие клинические симптомы включают:
Заболевание протекает бессимптомно примерно у 20% пациентов с развивающимся коллатеральным кровообращением.
Диагностика
Биохимические исследования
Биохимические тесты выявляют нарушения разной степени тяжести, в зависимости от клинического состояния. Асцитная жидкость имеет характеристики транссудата.
Изображение венозных сосудов
При допплеровском исследовании печеночные вены демонстрируют расширение в сочетании с отсутствием или изменением направления кровотока. Кроме того, могут быть расширенные коллатеральные сосуды, соединяющие печеночную вену с меж реберной и диафрагмальной венами. Магнитно-резонансная томография с контрастным веществом позволяет точно визуализировать обструкцию в просвете сосудов или источник внешнего давления на печеночные вены или нижнюю полую вену.
Гипертрофия хвостатой доли
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%93%D0%B8%D0%BF%D0%B5%D1%80%D1%82%D1%80%D0%BE%D1%84%D0%B8%D1%8F-%D1%85%D0%B2%D0%BE%D1%81%D1%82%D0%B0%D1%82%D0%BE%D0%B9-%D0%B4%D0%BE%D0%BB%D0%B8.jpg?resize=450%2C300&ssl=1″ alt=»Гипертрофия хвостатой доли» width=»450″ height=»300″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=825%2C550&ssl=1 825w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?resize=768%2C512&ssl=1 768w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Гипертрофия-хвостатой-доли.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Гипертрофия хвостатой доли
У большинства пациентов с синдромом Бадда-Киари наблюдается увеличение хвостатой доли. Это связано с тем, что хвостатая доля имеет венозное соединение с нижней полой веной, независимо от печеночных вен. Таким образом, в случае обструкции печеночных вен, по хвостатому отростку протекает гораздо больше крови, что приводит к его компенсаторной гипертрофии.
Регенеративные узелки
У пациентов с синдромом Бадда-Киари все визуальные исследования могут показать макро регенеративные узелки, демонстрирующие усиление артериальной фазы, и могут морфологически напоминать гепатоцеллюлярную карциному.
Эти узелки имеют иную этиологию, чем регенеративные, при циррозе печени. Их дифференциация от гепатоцеллюлярной карциномы может быть трудной. Многочисленные небольшие узелки указывают на довольно доброкачественные поражения, в то время, как единичные, увеличивающиеся поражения, могут указывать на рак.
Патоморфологическое обследование
При типичных симптомах синдрома Бадда-Киари в биопсии печени нет необходимости, более того, зачастую она невозможна по техническим причинам (нарушения свертываемости, асцит). Гистопатологическое исследование показывает расширение пазух с признаками застоя и фиброза в центральной части долек. Иногда в крошечных венах можно увидеть сгустки крови.
Мероприятия по порядку:
Антикоагулянтное лечение
Согласно рекомендациям AASLD, во время диагностики синдрома Бадда-Киари следует начать антикоагулянтную терапию (низкомолекулярные гепарины), а затем перейти на пероральные антикоагулянты, поддерживая нормализованный индекс активности протромбина (INR) в диапазоне 2- 3. Только противопоказания или серьезные осложнения, дают право прекратить лечение антикоагулянтами.
Чрескожная ангиопластика
Ангиопластика и протезирование печеночной вены следует рассматривать у всех пациентов с симптомами, чьи результаты визуализационных исследований показывают, что такое вмешательство возможно, например, в случае сегментарного стеноза или тромбоза.
Если антикоагуляция не улучшается, рассматривается возможность портальной системной трансъюгулярной внутрипеченочной фистулы (TIPS), очевидно, с предварительным подтверждением проходимости воротной вены.
TIPS у пациентов с синдромом Бадда-Киари — технически, очень сложная процедура, иногда она требует введения проводника непосредственно из просвета нижней полой вены, поэтому выполняется только в нескольких медицинских центрах в мире.
Пересадка печени
Показанием к трансплантации печени может быть мгновенная недостаточность органов. Трансплантация также должна рассматриваться, когда хирургия портальной системной трансцервикальной внутрипеченочной фистулы невозможна или неэффективна.
Прогноз
Независимые прогностические факторы при синдроме Бадда-Киари — это компоненты шкалы Чайлда-Тюркотта-Пью. Прогноз для этого синдрома значительно улучшился за последнее десятилетие и часто больше зависит от прогрессирования основного заболевания, (например, миелодиспластического синдрома), чем от симптомов печеночной недостаточности. Около 80% пациентов выживают через пять лет после трансплантации печени.
Резюме
» data-medium-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/%D0%A0%D0%B5%D0%B7%D1%8E%D0%BC%D0%B5.jpg?resize=450%2C300&ssl=1″ alt=»Резюме» width=»450″ height=»300″ srcset=»https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=450%2C300&ssl=1 450w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=825%2C550&ssl=1 825w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?resize=768%2C512&ssl=1 768w, https://i1.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2021/06/Резюме.jpg?w=900&ssl=1 900w» sizes=»(max-width: 450px) 100vw, 450px» data-recalc-dims=»1″ /> Резюме
Причиной обструкции печеночной артерии могут быть: атеросклероз, тромбоз, эмболия, инфильтрация печени, травмы, заболевания сосудов. Обструкция также может быть осложнением трансплантации печени.
Из-за двойной васкуляризации печени окклюзия печеночной артерии не является синонимом инфаркта органа. Визуализирующие исследования играют важную роль в диагностике: допплерография, компьютерная томография с контрастным веществом и магнитно-резонансная томография.
Тромбоз воротной вены подразделяется на острый и хронический. Оба состояния имеют схожую этиологию и чаще всего второе будет продолжением первого. Однако, методы лечения различаются. Наиболее частые факторы риска тромбоза воротной вены — это миелопролиферативные нарушения, а также врожденная и приобретенная недостаточность факторов, модулирующих каскад коагуляции.
Общие осложнения хронического тромбоза воротной вены, связанные с симптомами портальной гипертензии, являются редкой причиной смерти пациентов, умирающих от последствий портальной билиопатии или прогрессирования миелопролиферативного заболевания до острого лейкоза или миелофиброза.
Синдром заложенности носовых пазух печени приводит к нарушениям кровообращения в ней, в результате токсического повреждения эндотелиальных клеток, выстилающих пазухи.
Это наиболее частое осложнение миелоаблативного лечения при подготовке пациентов к трансплантации костного мозга.
Балтиморские критерии полезны в диагностике. Профилактика основана на менее агрессивных режимах миелоаблативной терапии, чем при стандартной терапии.
Тромбоз печеночных вен (синдром Бадда-Киари) может проявляться, как фульминантная, острая или хроническая печеночная недостаточность. В курс лечения входят: антикоагулянтная терапия, чрескожная ангиопластика, TIPS и трансплантация печени. Благодаря такому режиму лечения до 90% пациентов живут больше 5 лет.
Добавить комментарий Отменить ответ
Вы должны быть авторизованы, чтобы оставить комментарий.