Артерия люзория что это
Артерия люзория что это
Аберрантная правая подключичная артерия (a. lusoria), аномально отходящая от дуги аорты, пересекает среднюю линию между позвоночником и пищеводом, сдавливая последний. При рентгенологическом исследовании выявляется поперечно или косо расположенный дефект наполнения линейной или желобоватой формы, ширина которого зависит от калибра аномально расположенного сосуда и степени его давления на стенку пищевода.
Этот дефект наполнения всегда располагается на уровне нижнего края дуги аорты и в зависимости от проекции исследования может иметь вид борозды, полулуния или штыка. Для a. lusoria характерно также отсутствие или слабая выраженность свойственного норме аортального вдавления на переднелевои стенке пищевода.
Праволежащая аорта, как и a. lusoria, вызывает деформацию пищевода, сопровождающуюся характерной рентгенологической картиной: дуга аорты расположена справа, вследствие чего обусловленное ею вдавление пищевода находится не на переднелевои, а на заднеправой его стенке. Форма и размеры этого вдавления в прцессе исследования меняются. Дисфагия выражена незначительно; обычно она усиливается с появлением атеросклероза, сопровождающегося уплотнением, расширением и удлинением аорты.
Увеличение левого предсердия при митральном пороке сопровождается деформацией и смещением ретрокардиального сегмента пищевода вправо и кзади. Дисфагии при этом обычно не отмечается. Характер девиации пищевода учитывается при распознавании митрального стеноза. В зависимости от локализации и величины аневризмы аорты может наблюдаться различной степени деформация и смещение пищевода, нередко в сочетании с деструкцией тел позвонков. При аневризме дуги аорты пищевод смещается вправо или влево, а при поражении нисходящего ее отдела — кпереди и влево или вправо.
При атеросклерозе аорты полуовальной формы вдавление стенки пищевода всегда имеет ровные и четкие контуры. Форма и размеры его в процессе исследования меняются, рельеф слизистой оболочки имеет нормальный вид. При этом пищевод обычно смещается кпереди и влево (серповидное искривление). Эти изменения могут сопровождаться болями и перемежающейся дисфагией; иногда они служат поводом для дифференцирования от опухолей пищевода.
Наличие самостоятельной пульсации патологического образования, синхронной с пульсацией аорты или камер сердца, а также изменение его величины при функциональных пробах Вальсальвы и Мюллера значительно облегчают диагностику внепищеводных процессов, относящихся к сердцу или крупным сосудам средостения. После того как установлен конкретный диагноз болезни, необходимо выяснить, не вовлечена ли в данный патологический процесс и стенка пищевода, а также исключить возможные при этом осложнения.
— Вернуться в оглавление раздела «Лучевая медицина»
Аберрантная правая подключичная артерия: расставляем акценты
Медицинский центр «Униклиника», г. Киев
Вступление
Аберрантная правая подключичная артерия (aberrant right subclavian artery, ARSA, arteria lusoria) является наиболее распространённой аномалией сосудов дуги аорты. Будучи нередкой пренатальной находкой, она представляет собой источник волнений и тревоги как для пациентов, так и для сопровождающих докторов. В этой статье предпринята попытка коротко систематизировать имеющиеся данные с целью оптимизации консультирования супружеской пары относительно имеющейся аномалии, а также приведены примеры визуализации нормальной и измененной анатомии.
История исследования
Первые анатомические описания различных типов аортальных дуг и сосудистых колец относятся к XVIII в. и принадлежат Hanault (1735) и Bajford (1794). В 1948 году J. Б. Edwards предложил теорию «гипотетической двойной дуги аорты» как исходную модель для теоретического объяснения образования аномалий дуги аорты. Суть теории состоит в том, что аномалии системы дуги аорты являются результатом либо регрессии и исчезновения эмбриональных сосудистых структур, в норме сохраняющихся, либо сохранения структур, в норме регрессирующих.
Анатомия
Аберрантная правая подключичная артерия отходит от левой стороны дуги аорты, проходит позади пищевода в 80% случаев, между пищеводом и трахеей в 15% наблюдений, спереди трахеи только в 5% случаев. В ряде случаев она начинается от дивертикула Коммереля (частота от 14 до 60%).
Эпидемиология
По мнению М. de Leval (1983), аномальная правая подключичная артерия наблюдается у 0,5% населения. По данным ряда других больших аутопсийных исследований, частота аберрантной подключичной артерии варьирует от 0,2% до 2,5% (Nakatani Т. с соавт., 1998). Современные данные отмечают частоту порядка 1,5% среди эуплоидной популяции. Отмечается небольшое преобладание данной аномалии у женщин [2, 3, 4].
Симптоматика
Изолированная аберрантная правая подключичная артерия может не проявлять себя клинически и часто является второстепенной находкой при аутопсийном исследовании.
Аномалии дуги аорты без сочетания с другими врожденными или приобретенными пороками сердца и сосудов, как правило, не сопровождаются нарушениями гемодинамики, в связи с чем часто протекают бессимптомно и обычно остаются не диагностированными. Как изолированный порок аномалии дуги аорты встречаются при формировании сосудистого кольца вокруг пищевода и трахеи и в этом случае проявляются симптомами компрессии трахеи и пищевода [2, 4]. Респираторная симптоматика включает в себя затрудненное приступы удушья, кашель, затяжные бронхолегочные заболевания. Эзофагальные симптомы проявляют себя затрудненным болезненным глотанием, поперхиванием, срыгиванием и даже рвотой. К другим возможным симптомам, которые проявляются в раннем младенческом возрасте, относятся акроцианоз, отставание в физическом развитии, недостаточная масса тела. Указанные симптомы компрессии присутствуют только у 7–10% пациентов, в 90–93% случаев клинически ARSA может себя не проявлять [1, 2, 3].
Лечение
В подавляющем большинстве случаев данная аномалия не требует никаких вмешательств и не нарушает качества жизни, однако у симптомных пациентов вмешательство является рациональным в ряде случаев. Большое количество работ посвящено хирургическому лечению аберрантной правой подключичной артерии при ее клинической манифестации. По мнению ряда авторов, выбор хирургического доступа при данной патологии зависит от наличия или отсутствия аневризмы аберрантной подключичной артерии, экстренности операции и опыта хирурга. Большинство авторов считает, что при наличии выраженных клинических симптомов компрессии показана хирургическая коррекция аномалии, заключающаяся в пересечении a. lusoria в I сегменте. Однако, избавляя больных от симптомов компрессии пищевода, такая операция создает условия для развития симптомов вертебробазилярной недостаточности за счет появляющегося позвоночно-подключичного синдрома обкрадывания головного мозга. Некоторые исследователи отмечают, что наименее инвазивная операция, такая как экстраторакальная имплантация артерии lusoria в общую сонную артерию, является эффективным методом коррекции данной аномалии, избавляющим пациентов от симптомов компрессии трахеи и пищевода [2, 4, 5].
Значение ARSA в пренатальной диагностике
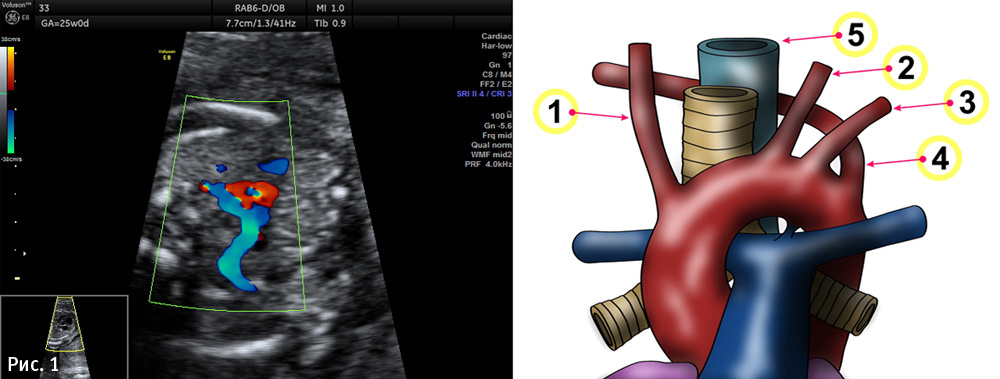
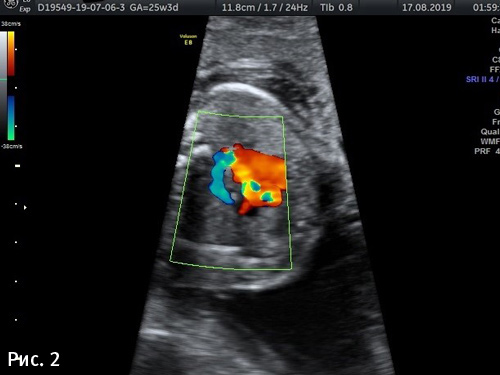
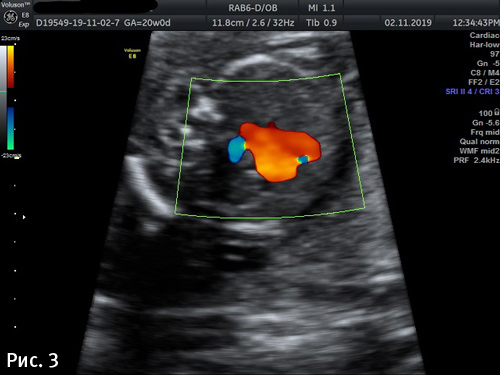
При эхокардиоскопии плода ARSA визуализируется в срезе «через три сосуда и трахею». Отмечается как сосуд, отходящий от дуги аорты в месте слияния ее с аортальным протоком, и идущий к правой руке плода позади трахеи (рис. 2 и 3). Для сравнения, на рис. 1 и видео 1 нормальный ход правой подключичной артерии. Чтобы улучшить визуализацию, настройки скорости цветного доплера необходимо скорректировать в диапазоне от 15 до 30 см/с (видео 2).
Видео 1- видеоролик показывает ход нормальной правой подключичной артерии впереди трахеи (типичная форма «S»)
Видео 2- видеоролик, демонстрирующий ход аберрантной правой подключичной артерии позади трахеи.
Об идентификации ARSA у плодов с синдромом Дауна впервые сообщили в 2005 г. Chaoui et al. Согласно постнатальным исследованиям, 16–35% детей с трисомией 21 имеют данную аномалию, в то время как у эуплоидных детей ее частота составляет 1,4–1,5%. Кроме того, опубликованы данные про наличие ARSA у 18.2% плодов с трисомией 18 [6, 7]. Самой частой микроделецией, с которой ассоциирована аномалия, является делеция 22q11, которая обнаруживается в 8% наблюдений при изолированной находке ARSA; в сочетании с другими врожденными пороками сердца синдром – в 46% случаев [1].
Проведение кариотипирования плода, когда ARSA является изолированной находкой, все еще остается спорным вопросом [5, 6]. Однако, в 20–30% случаев ARSA ассоциациирована с другими анатомическими аномалиями, потому кариотипирование (в идеале с микроматричным анализом) показано при обнаружении других эхоскопических маркеров или в группе высокого/промежуточного риска анеуплоидий.
Учитывая, что аберрантная правая подключичная артерия в 5–24% случаях сочетается с пороками сердца, то в первую очередь необходимо исключить их. К наиболее часто сочетаемым с ARSA порокам относятся: стеноз аорты, атриовентрикулярный канал, декстракардия, расширенный артериальный проток, двойной выход из правого желудочка, персистирующая левая верхняя полая вена, рабдомиома, тетрада Фалло, атрезия трикуспидального клапана, дефект межжелудочковой перегородки [5, 6, 7].
Резюме
Литература:
Все снимки и видео получены в МЦ «Униклиника»
Снимок 1- цветное допплеровское изображение показывает ход нормальной правой подключичной артерии впереди трахеи (типичная форма «S»).
Видео 1- видеоролик показывает ход нормальной правой подключичной артерии впереди трахеи (типичная форма «S»).
Рисунок 1: 1- правая общая сонная артерия; 2-левая общая сонная артерия; 3- левая подключичная артерия; 4-правая подключичная артерия (расположенная ретроэзофагеально); 5-пищевод.
Снимок 2- ARSA как сосуд, отходящий от дуги аорты в месте слияния ее с аортальным протоком, и идущий к правой руке плода позади трахеи.
Видео 2- видеоролик, демонстрирующий ход аберрантной правой подключичной артерии позади трахеи.
Снимок 3 – еще один случай четкой визуализации ARSA
Артерия люзория что это
ВАРИАНТНАЯ АНАТОМИЯ ДУГИ АОРТЫ: ARTERIA LUSORIA
д.м.н., профессор, заведующий кафедрой оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ (Воронежский государственный медицинский университет) им. Н.Н. Бурденко Минздрава России
к.м.н., ассистент кафедры оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ (Воронежский государственный медицинский университет) им. Н.Н. Бурденко Минздрава России
к.м.н., доцент кафедры оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ (Воронежский государственный медицинский университет) им. Н.Н. Бурденко Минздрава России
к.м.н., ассистент кафедры оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ (Воронежский государственный медицинский университет) им. Н.Н. Бурденко Минздрава России, врач-хирург БУЗ ВО ВОКБ №1(Воронежская областная клиническая больница №1).
При топографо-анатомическом препарировании фиксированного трупа мужчины, умершего в возрасте 62 лет, обнаружена аберрантная правая подключичная артерия. Она располагалась позади ветвей дуги аорты и органов шеи. Близкое расположение правой аберрантной подключичной артерии с многочисленными органами, кровеносными сосудами и нервными стволами может стать причиной различных осложнений при хирургических вмешательствах.
Ключевые слова: дуга аорты, аберрантная правая подключичная артерия, сосудистые аномалии.
Материалы и методы
Исследован фиксированный труп мужчины, умершего в возрасте 62 года. Проводилось топографо-анатомическое препарирование передней области шеи и средостения. Доступ к органам и сосудам шеи выполнялся двумя горизонтальными и одним вертикальным разрезами[7][8]. Верхний горизонтальный разрез соединял верхушки сосцевидных отростков височной кости и проводился вдоль нижнего края нижней челюсти. Нижний горизонтальный разрез соединял основания акромиальных отростков лопаток и проводился по верхнему краю ключиц и рукоятки грудины[2][4]. Вертикальный разрез соединял горизонтальные и соответствовал срединной линии. Для осмотра переднего средостения выполнялась срединная стернотомия[7].
Результаты исследования и их обсуждение
Рис. 1. Топография аберрантная правой подключичной артерии.
Обозначения: 1 – дуга аорты, 2 – правая общая сонная артерия, 3 – трахея, 4 – пищевод, 5 – левая общая сонная артерия, 6 – левая подключичная артерия, 7 – аберрантная правая подключичная артерия ( arteria lusoria ).
Полученные в проведенном исследовании данные несколько расходятся с литературными. Так, на изученном секционном материале диаметр поверхностной надчревной артерии на уровне паховой связки составил 1.7±0.2 мм, а вены – 2.1±0.4 мм. Из этого следует, что диаметр исследованных кровеносных сосудов соответствует требованиям пластических хирургов по выполнению микрососудистых анастомозов.
1. Выявлен и описан достаточно редкий вариант дуги аорты – аберрантная правая подключичная артерия. В данном случае аномальный сосуд отходил от дуги аорты дистальнее места отхождения левой подключичной артерии и направлялся слева направо через ретровисцеральное клетчаточное пространство шеи.
2. Новые данные в лечении гнойных ран у больных микрохирургического профиля / / Д.В. Судаков, А.В. Черных, Е.И. Закурдаев, А.Н. Тихонов // Центральный научный вестник. 2017. Т. 2. № 1 (18). С. 9-11.
3. Оценка информативности показателей клинического обследования пациентов с сахарным диабетом 2 типа и гнойными ранами / Д.В. Судаков, Е.В. Стародубцева, О.В. Судаков, В.Н. Снопков // Системный анализ и управление в биомедицинских системах. 2013. Т. 12. № 4. С. 1163-1165.
4. Опыт аутотрансплантации икроножным нервом магистральных нервных стволов предплечья на фоне укушенных ран верхних конечностей / Д.В. Судаков, А.В. Черных, Н.В. Якушева, А.Н. Тихонов // Центральный научный вестник. 2017. Т. 2. № 1 (18). С. 12-14.
5. Построение прогноза эффективности аутотрансплантации икроножным нервом в микрохирургии верхних конечностей у больных сахарным диабетом 2 типа / Д.В. Судаков, А.В. Черных, Н.В. Якушева, Н.О. Васильев // В сборнике: Актуальные вопросы современной медицины. Сборник научных трудов по итогам III международной научно – практической конференции. 2016. С. 122-124.
6. Проблема антибиотикорезистентности в микрохирургии / Д.В. Судаков, А.В. Черных, Е.И. Закурдаев, А.Н. Тихонов // Центральный научный вестник. 2017. Т. 2. № 1 (18). С. 15-17.
7. Редкий случай гигантской скользящей пахово-мошоночной грыжи мочевого пузыря / А.В. Черных, Е.Н. Любых, Ю.В. Малеев, Е.И. Закурдаев, А.Н. Шевцов, В.В. Спицин //Журнал анатомии и гистопатологии. 2013. Т. 2. № 3 (7). С. 67-69.
8. Судаков Д.В. Анализ состава микробной флоры у больных сахарным диабетом 2 типа после аутотрансплантации икроножным нервом поврежденных магистральных нервов предплечья / Д.В. Судаков, А.В. Черных, Н.В. Якушева // В сборнике: Современная медицина: актуальные вопросы и перспективы развития. Сборник научных трудов по итогам международной научно-практической конференции. Инновационный центр развития образования и науки. 2016. С.134-138.
9. Судаков Д.В. Моделирование процесса лечения гнойных ран у пациентов с сахарным диабетом / Д.В. Судаков // Системный анализ и управление в биомедицинских системах. 2013. Т. 12. № 1. С. 327-330.
10. Судаков Д.В. Построение прогноза эффективности использования кистевого внеочагового компрессионно – дистракционного аппарата Илизарова в микрохирургии / Д.В. Судаков, А.В. Черных, Н.В. Якушева // В сборнике: Современная медицина: актуальные вопросы и перспективы развития. Сборник научных трудов по итогам международной научно-практической конференции. Инновационный центр развития образования и науки. 2016. С.138-143.
11. Черных А.В., Витчинкин В.Г., Якушева Н.В., Малеев Ю.В., Закурдаев Е.И., Болотских В.А., Спицын В.В. Высокое отхождение лучевой и локтевой артерий // Журнал анатомии и гистопатологии. – 2014. – Т. 3, № 3. – С. 63-65.
12. Черных А.В., Закурдаев Е.И., Якушева Н.В., Витчинкин В.Г., Малеев Ю.В., Закурдаева М.П., Андрианова К.А., Лазарева О.А. Прикладные аспекты вариантной анатомии нижней надчревной артерии // Журнал анатомии и гистопатологии. – 2016. – Т. 5, № 4. – С. 74-78.
Сведения об авторах:
Черных Александр Васильевич – доктор медицинских наук, профессор, заведующий кафедрой оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ им.Н.Н. Бурденко Минздрава России. operhir@vsmaburdenko.ru
Закурдаев Евгений Иванович – кандидат медицинских наук, ассистент кафедры оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ им.Н.Н. Бурденко Минздрава России. operhir@vsmaburdenko.ru
Якушева Наталья Владимировна – кандидат медицинских наук, доцент кафедры оперативной хирургии с топографической анатомией ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России. operhir@vsmaburdenko.ru
VARIANT ANATOMY OF THE AORTIC ARCH: ARTERIA LUSORIA
Chernyh A.V., Zakurdaev E.I., Yakusheva N.V., Sudakov D.V.
When topographic anatomical dissection of a fixed cadaver of a man, who died at the age of 62 years, found an aberrant right subclavian artery. It was located behind the branches of the aortic arch and organs of neck. The proximity of the aberrant right subclavian artery with multiple organs, blood vessels and nerve trunks can cause a variety of complications during surgery.
Keywords: aortic arch, aberrant right subclavian artery, vascular abnormalities.
Клиническая анатомия и особенности невозвратного гортанного нерва в хирургии щитовидной железы. Клинический случай
Полный текст:
Аннотация
В последние десятилетия отмечается значительный успех в хирургии щитовидной железы, однако частота развития пареза гортани вследствие повреждения возвратного гортанного нерва остается высокой. Детальное изучение разных вариантов топики нерва – одно из направлений, дающих возможность снизить его травматизацию. Невозвратный нижний гортанный нерв является редкой анатомической особенностью, которая выявляется при операциях на щитовидной железе в 0,3–1% случаев. Несмотря на такую редкую встречаемость, к сожалению, атипичное расположение невозвратного гортанного нерва создает предпосылки для его ятрогенного повреждения. В статье проведен анализ литературы, описаны причины возникновения, связь с аномалией магистральных сосудов и клиническое значение. Описаны два случая выявления невозвратного нижнего гортанного нерва в хирургической клинике ФГБУ РНЦРР МЗ РФ.
Ключевые слова
Для цитирования:
Галушко Д.А., Асмарян А.Г., Пасько М.А. Клиническая анатомия и особенности невозвратного гортанного нерва в хирургии щитовидной железы. Клинический случай. Клиническая и экспериментальная тиреоидология. 2016;12(3):31-36. https://doi.org/10.14341/ket2016331-36
For citation:
Galushko D.A., Asmaryan H.G., Pasko M.A. Clinical anatomy and features non-recurrent inferior laryngeal nerve in thyroid surgery. Case report. Clinical and experimental thyroidology. 2016;12(3):31-36. (In Russ.) https://doi.org/10.14341/ket2016331-36
Актуальность
Возвратный нижний гортанный нерв (ВНГН) является парным нервом, иннервирующим мышцы гортани и голосовые связки. Повреждение этого нерва может привести к парезу или параличу голосовой складки на той же стороне, что проявляется осиплостью голоса. Если повреждение двустороннее, в результате смыкания паралитических голосовых связок может полностью закрыться голосовая щель, что обычно проявляется афонией и опасной для жизни одышкой, которая требует немедленного выполнения трахеостомии. Несмотря на значительные успехи в хирургии щитовидной железы, по некоторым данным литературы, частота развития пареза гортани вследствие повреждения возвратного гортанного нерва может доходить до 20%. В среднем это осложнение развивается у 2,9% больных при первичных и 8,2% – при повторных операциях. Практически всеми исследователями было продемонстрировано, что визуализация ВНГН во время хирургического вмешательства значительно снижает риск повреждения нерва [1]. Чтобы достигнуть этого, нужно иметь твердые знания нормальных и различных форм топики ВНГН.
ВНГН традиционно называют так вследствие того, что, отходя от блуждающего нерва, он, как правило, формирует петлю, поворачивая вверх, проходя под подключичной артерией справа и под дугой аорты слева, и поднимается вверх, располагаясь в борозде между пищеводом и трахеей. Возвратный нерв отдает чувствующие и двигательные ветви к мышцам пищевода и подходит к гортани. На уровне нижнего края перстневидного хряща возвратный нерв успевает отдать почти все свои чувствующие волокна. Остается лишь небольшая чувствующая ветвь, которая иннервирует слизистую оболочку в области угла и двух передних третей пластинок щитовидного хряща ниже голосовых складок. Двигательная часть нижнего гортанного нерва вступает в гортань сзади от сочленения малого рожка щитовидного хряща с дугой перстневидного и снабжает двигательными ветвями все внутренние мышцы гортани, за исключением передней перстнещитовидной мышцы, которая получает иннервацию от верхнего гортанного нерва.
Есть разные теории, объясняющие, почему этот нерв имеет возвратную природу. Самая популярная из них – теория эволюциониста Ричарда Довкинса, который, исследуя расположение сердца у рыбоподобных предков современных четвероногих, показал, что с появлением и удлинением шеи меняется расположение сердца. Последнее в эволюционном развитии “спускается” все ниже и ниже. У человеческого эмбриона нервная трубка на начальных этапах развития имеет тесную связь с жаберными дугами. Из IV–VI жаберных дуг формируются щитовидный, перстневый, черпаловидные хрящи гортани, констрикторы гортани и пищевода. Кровоснабжение данных анатомических образований осуществляется за счет соответствующих IV–VI дуг жаберных артерий. ВНГН переплетается вокруг пятой дуги, далее в процессе онтогенеза данные дуги опускаются в каудальном направлении, “унося” с собой нижний гортанный нерв вниз. Слева пятая дуга представляет собой дугу аорты и артериальный проток. Справа пятая и шестая дуги исчезают, и петля нерва окружает IV дугу, из которой формируется подключичная артерия [2, 3]. Такое анатомическое расположение ВНГН характерно для большинства млекопитающих, так, наибольшая длина нерва отмечается у жирафа, достигая 4 метров.
У пациентов, у которых наблюдаются аномалии развития подключичных артерий, нижний гортанный нерв отходит от блуждающего нерва на уровне гортани – невозвратный нижний гортанный нерв (ННГН). Первое упоминание о ННГН датируется 1823 г., когда патологоанатом Д.В. Стедман описал случай аутопсии, где правый нижний гортанный нерв отходил от блуждающего нерва на уровне гортани [4]. Также в записях было описание аномалии отхождения правой подключичной артерии. Последняя отходила от дуги аорты слева отдельным стволом. Первый описанный случай аномалии подключичной артерии датируется более ранним периодом. Бейфорд в 1787 г. опубликовал случай дисфагии, обусловленный сдавлением пищевода аномальной правой подключичной артерией, назвав ее дисфагией люзория (lusoria – от латинского lusus nature – игры природы, загадки природы) [5]. Эта аномалия сосудистой системы, по разным сообщениям, встречается у 0,5–2% населения [6]. Описаны три анатомических варианта расположения данной артерии: позади пищевода (85% наблюдений), между пищеводом и трахеей (10% случаев), впереди трахеи (5% случаев). В большинстве случаев клинические проявления отсутствуют, и только у 5–7% пациентов проявляются симптомы, которые могут возникать при сдавлении a. lusoria пищевода и трахеи, – дисфагия, боль в грудной клетке, затруднение дыхания. Чрезвычайно редко встречаются случаи, когда a. lusoria отходит от аневризматически расширенной дуги аорты, которая получила название «дивертикул Коммереля» [6–8].
Невозвратный нижний гортанный нерв – более редкая аномалия, которая наблюдается в 0,3–0,9% случаев на правой стороне и в 0,004% – слева, хотя большинство исследователей утверждают, что истинных левосторонних невозвратных нервов не бывает и в описанных случаях имеет место транспозиция внутренних органов (situs inversus) [9, 10]. Различают два варианта расположения невозвратного гортанного нерва. При первом типе расположения ННГН отходит непосредственно от блуждающего нерва, располагается вместе с верхними щитовидными сосудами. При втором варианте расположения нерв лежит параллельно нижней щитовидной артерии (тип 2А – над стволом и тип 2B – под или между ветками нижней щитовидной артерии). При этом некоторые авторы сообщают о наличии еще одной атопии – медиального расположения блуждающего нерва (медиальнее общей сонной артерии), считая это “сигнальной лампочкой” для выявления невозвратного нерва [3, 11, 12].
Клинический случай №1
В клинику обратилась женщина 46 лет, у которой по месту жительства по данным УЗИ был выявлен узел правой доли щитовидной железы. При комплексном обследовании в РНЦРР у нее был установлен диагноз: папиллярный рак правой доли щитовидной железы T1N0M0. Пациентке была выполнена тиреоидэктомия с центральной шейной лимфодиссекцией. Интраоперационно был выявлен правый невозвратный нижний гортанный нерв – вариант 2А (рис. 1).
Рис. 1. Интраоперационный вид ННГН справа.
Нерв длиной около 4 см практически под прямым углом отходил от правого блуждающего нерва. Он мобилизован на всем протяжении и прослежен до впадения в гортань. Слева возвратный нижний гортанный нерв располагался в типичном для себя анатомическом месте (рис. 2).
Рис. 2. Интраоперационный вид ВНГН слева.
В послеоперационном периоде больная была дополнительно обследована: выполнена компьютерная томография шеи и органов грудной клетки с ангиографией (рис. 3 а, б) и прямая ангиография (рис. 4), по данным которых подтверждено наличие у пациентки аномалии развития ветвей аорты. Правая подключичная артерия отходит от уровня перешейка аорты по ее задней поверхности самостоятельным стволом, проходя между аортой и позвоночным столбом на уровне третьего позвонка, – a. lusoria. От правой подключичной артерии отходит правая позвоночная артерия. Правая общая сонная артерия отходила от аорты одним устьем вместе с левой общей сонной артерией, что наглядно демонстрируется на ангиограммах в виде симптома “бычьих рогов”. Послеоперационный период у больной протекал гладко, без осложнений. Фонация голосовых связок не была изменена.
Рис. 3. Результаты компьютерной томографии шеи и органов грудной клетки с ангиографией: а – аорта (вид сзади); б – предпозвоночное расположение правой подключичной артерии.
Рис. 4. Ангиография (селективное контрастирование сонных, левой и правой подключичных артерий).
Клинический случай №2
Пациент М., 54 г. Узлы в щитовидной железе выявлены при УЗИ в 2013 г. При контрольном УЗИ в 2015 г. отмечена отрицательная динамика в виде увеличения узла правой доли в размерах с 9 до 13 мм. В РНЦРР проведено комплексное обследование: произведена тонкоигольная аспирационная пункция, морфологически подтвержден папиллярный рак щитовидной железы. Регионарного и отдаленного метастазирования не выявлено. Также у пациента в анамнезе лечение по поводу рака левой молочной железы Т1N0М0: выполнена радикальная резекция левой молочной железы и проведена лучевая терапия. Непродолжительное время лечение антиэстрогенными препаратами. 13.10.2015 выполнена тиреоидэктомия с микрохирургическим невролизом возвратных гортанных нервов. Интраоперационно: при мобилизации выявлен правый невозвратный нижний гортанный нерв (вариант 2В). Выполнен невролиз правого ННГН: прослежен от правого блуждающего нерва на уровни гортани до впадения в гортань, сохранен (рис. 5).
Рис. 5. Интраоперационный вид. Белая стрелка – невозвратный нижний гортанный нерв.
В послеоперационном периоде проводились дополнительные исследования – по данным ангиографии и компьютерной томографии подтверждено наличие сосудистой аномалии в виде a. lusoria. Послеоперационный период у больной протекал гладко, без осложнений. Фонация голосовых связок не была изменена. Проведенные дополнительные исследования подтвердили наличия a. lusoria. По данным МСКТ-ангиографии правая подключичная артерия (a. lusoria) отходит отдельным стволом позади и левее от места отхождения левой подключичной артерии, расположение ее предпозвоночное позади пищевода, отмечается сдавление пищевода (рис. 6 а, б, в).
Рис. 6. Результаты рентгенологического исследования: а – МСКТ расположения a. lusoria; б – компьютерная ангиография (вид спереди); в – компьютерная ангиография (вид сзади).
По данным ангиографии – ангиографическая картина a. lusoria. Справа налево от дуги аорты отходят устья правой и левой общих сонных артерий, левой подключичной артерии и правой подключичной артерии (последние два практически на одном уровне) (рис. 7).
Рис. 7. Ангиография.
Обсуждение
Анатомическое расположение НВГН значительно увеличивает риск его ятрогенного повреждения при выполнении тиреоидэктомии. Возможна травма нерва при выполнении тракции щитовидной железы и трахеи; во время лимфодиссекции; также нерв может быть ошибочно принят за сосуд, при этом перевязан или сожжен. Анализ литературных данных показывает высокую чувствительность компьютерной томографии для выявления сосудистой аномалии у больных, что в какой-то мере может служить предоперационным методом диагностики ННГН. Однако редкость встречаемости такой анатомической особенности не дает возможности рекомендовать метод как обязательный в предоперационном обследовании. Но при назначении этого обследования по другим показаниям в обязательном порядке должны быть изучены варианты кровоснабжения и топическая анатомия крупных сосудов, в частности подключичных и сонных артерий. Некоторые авторы сообщают о пользе проведения ультразвукового триплексного сканирования сосудов головы и шеи, при этом отмечая, что визуализация этих аномалий очень трудна и зависит от уровня подготовки специалиста. И поэтому, к сожалению, единственным достоверным методом выявления невозвратного нерва остается интраоперационный. Надо отметить, что, несмотря на многочисленные рекомендации начинать поиски невозвратного гортанного нерва только после неудачной попытки обнаружения возвратного гортанного нерва в типичном для него месте, мы придерживаемся мнения тех авторов, которые рекомендуют в каждом случае идентифицировать все структуры зоны медиальнее сонной артерии до доли щитовидной железы (так называемый transversus path – поперечный путь). Особое внимание стоит уделять области нижней щитовидной артерии и медиальной вены щитовидной железы.
Заключение
Агрессивные вмешательства в области головы и шеи, которые могут поставить под угрозу целостность гортанных нервов, являются частью повседневной хирургической практики. Твердые знания нормальной морфологии и не самых частых вариантов топики нижних гортанных нервов, включая его невозвратный вариант, могут помочь врачам минимизировать риск ятрогенного повреждения этого нерва.
Согласие пациента. Все пациенты добровольно подписали информированное согласие на публикацию персональной медицинской информации в рамках настоящей статьи.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.